Clear Sky Science · sv
ConvAHKG: Åtgärdsbaserad hybridkunskapsgraf med en tvåkanalig konvolutionell metod för läkemedelsomplacering
Hitta nya användningsområden för gamla läkemedel
Att ta ett helt nytt läkemedel till marknaden kan ta mer än ett decennium och kosta flera miljarder dollar, och många kandidater fallerar längs vägen. Denna studie undersöker en smartare genväg: att använda data och artificiell intelligens för att upptäcka nya sjukdomar som befintliga, redan godkända läkemedel kan behandla säkert. Författarna presenterar ett ramverk, kallat ConvAHKG, som väver ihop många slags biomedicinsk information till en enhetlig uppkopplad karta och sedan använder ett modernt neuralt nätverk för att identifiera lovande läkemedels–sjukdom-matchningar — vilket erbjuder en snabbare, billigare väg till nya terapier.
En rik karta över hur läkemedel och sjukdomar interagerar
I hjärtat av detta arbete finns en "hybridkunskapsgraf", en jätte-karta som kopplar samman läkemedel, sjukdomar, proteiner, biverkningar, kemiska strukturer och biologiska vägar. Istället för att bara lagra enkla ja–nej-länkar (till exempel "läkemedel A behandlar sjukdom B") registrerar kartan hur ett läkemedel verkar på ett protein — om det aktiverar, hämmar eller binder till det — och hur proteiner är involverade i sjukdomar, såsom att fungera som biomarkörer eller förändras i aktivitet. Grafen innehåller över 11 000 entiteter och 59 typer av relationer, inklusive detaljerad information om läkemedelsklassificeringar, biverkningar, protein–protein-kontakter och kemiska substrukturer. Genom att fånga dessa många lager av kontext kan grafen återspegla mer av den verkliga biologiska komplexiteten bakom behandlingseffekter och negativa reaktioner. 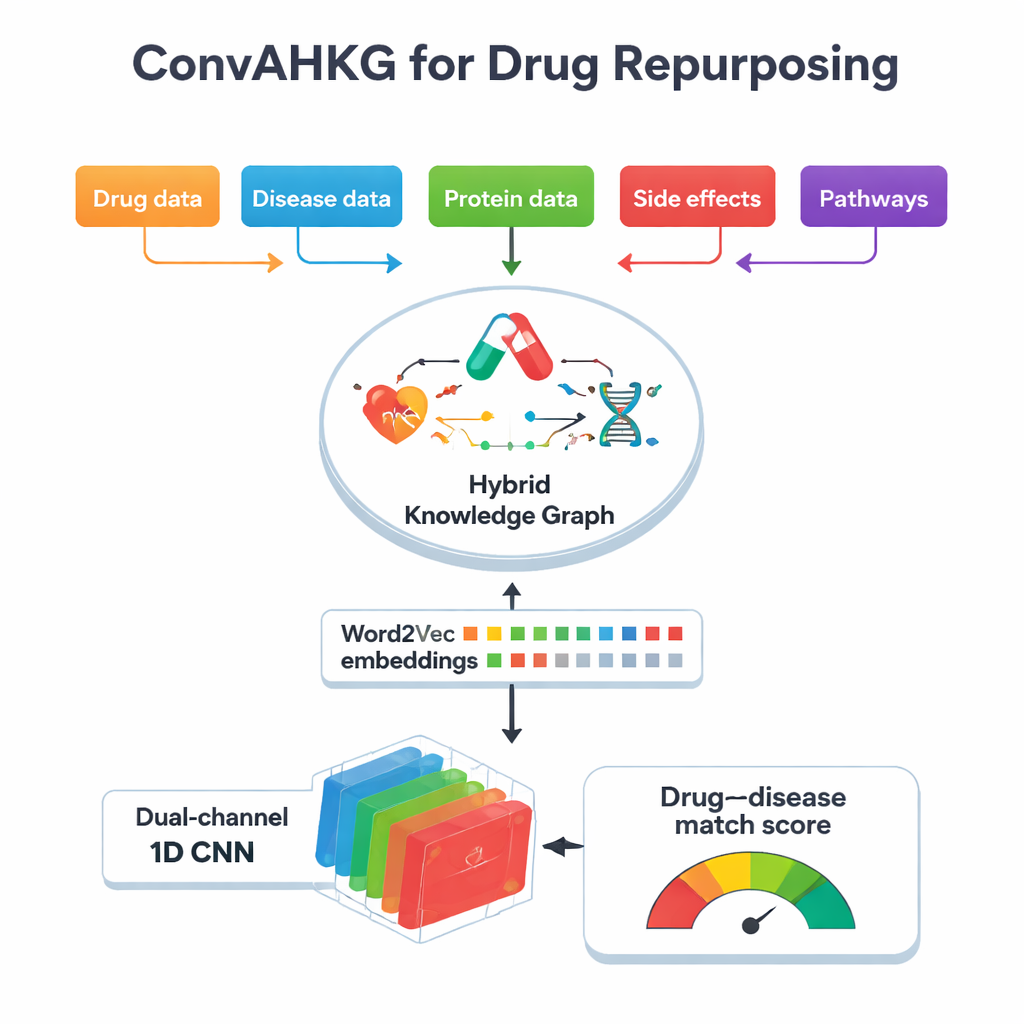
Lära datorn biologins språk
För att göra denna komplexa karta användbar för maskininlärning omvandlar teamet varje koppling i grafen till en enkel treparts "mening": ett huvud (såsom en sjukdom), en relation (såsom biomarkör) och en svans (såsom ett protein). De applicerar sedan Word2Vec, en metod ursprungligen utvecklad för naturlig språkbehandling, för att lära numeriska "inbäddningar" för varje läkemedel, sjukdom och protein. Objekt som ofta förekommer tillsammans i dessa meningar hamnar nära varandra i detta matematiska rum, ungefär som ord som delar liknande betydelser i text. Detta tillvägagångssätt är betydligt enklare och snabbare än många graf-specifika inbäddningstekniker, samtidigt som det fångar subtila mönster. I tester mot flera populära inbäddningsmetoder för kunskapsgrafer matchade eller överträffade Word2Vec deras prediktiva förmåga samtidigt som det använde mycket mindre beräkningstid.
En dubbel neural väg för ja/nej-beslut om behandling
När varje läkemedel och sjukdom översatts till en numerisk vektor matar ConvAHKG dem in i ett tvåkanaligt endimensionellt konvolutionellt neuralt nätverk. En kanal bearbetar läkemedelsvektorn och den andra bearbetar sjukdomsvektorn med en följd av konvolutionsfilter som upptäcker lokala mönster och bredare motiv, inspirerade av utformningar från bildigenkänning såsom InceptionNet och AlexNet. Efter denna separata bearbetning slås de två strömmarna samman och passerar genom flera fullt anslutna lager som ger ut en enda sannolikhet: representerar detta läkemedel–sjukdomspar en sannolikt effektiv behandling, eller snarare en skadlig biverkan? För att hantera att kända positiva par är mycket mer sällsynta än negativa introducerar författarna en viktad förlustfunktion som straffar missade sanna behandlingar hårdare, vilket förbättrar prestanda i dessa svårfunna fall. 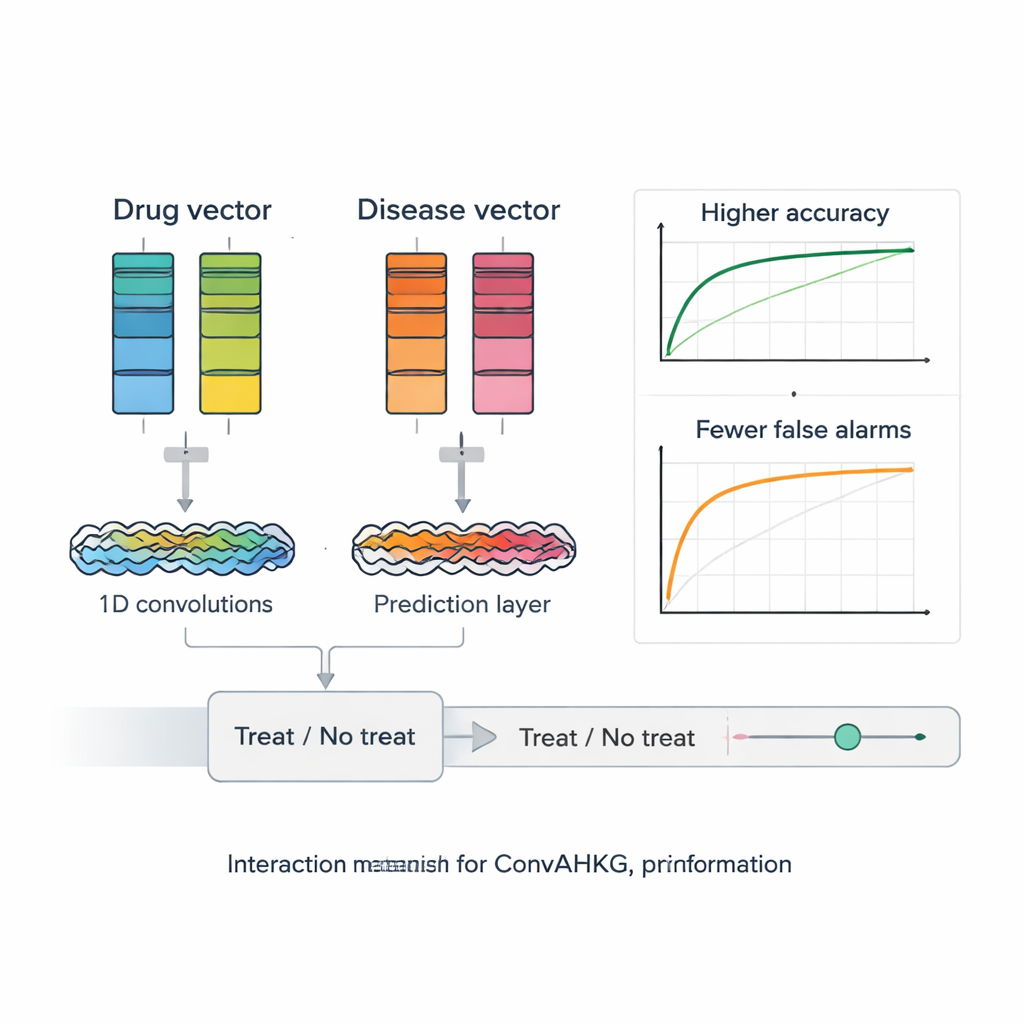
Slår befintliga metoder och hittar cancerkandidater
Forskarna testar sitt ramverk rigoröst mot flera toppmoderna verktyg för läkemedelsomplacering som använder matrisfaktorisering, grafneuronätverk och djupa autoenkodare. ConvAHKG når ett areaunder ROC-kurvan (AUC) på 0,9836 och ett areaunder precision–recall-kurvan på 0,9686, och överträffar alla konkurrerande tillvägagångssätt på samma benchmark-dataset. De applicerar sedan modellen på icke-småcellig lungcancer, den vanligaste och dödligaste formen av lungcancer i världen. ConvAHKG lyfter fram flera läkemedel som tidigare inte märkts som behandlingar för denna sjukdom, inklusive antikroppen trastuzumab, som riktar sig mot proteinet HER2 och redan har stöd i kliniska data för lungcancer, liksom andra biologiska medel och till och med det klassiska antibiotikumet bensylpenicillin. Dockningssimuleringar antyder att bensylpenicillin kan binda starkt till DNA och till topoisomeras II alfa, ett enzym som ofta är förhöjt i dessa tumörer, vilket ger en möjlig anticancer-mekanism som nu motiverar laboratorietester.
Varför detta är viktigt för patienter
Enkelt uttryckt fungerar ConvAHKG som en välinformera matchmaker mellan befintliga läkemedel och sjukdomar, genom att använda en detaljerad karta över biologiska handlingar och en kraftfull mönsterigenkänningsmotor för att förutsäga vilka gamla läkemedel som kan fungera i nya sammanhang. Genom att behandla säkerhetstestade läkemedel som återanvändbara byggstenar snarare än endamålsverktyg kan detta ramverk påskynda upptäckten av behandlingar för tillstånd som lungcancer, särskilt där konventionell läkemedelsutveckling är för långsam eller kostsam. Även om förutsägelserna fortfarande kräver noggrann experimentell och klinisk validering visar studien att kombinationen av rik biologisk kunskap och modern AI kraftigt kan begränsa sökutrymmet, vilket snabbare kan föra potentiellt livräddande behandlingar inom räckhåll.
Citering: Khodadadi AghGhaleh, M., Abedian, R., Zarghami, R. et al. ConvAHKG: Action-based hybrid knowledge graph with a dual-channel convolutional approach for drug repurposing. Sci Rep 16, 7592 (2026). https://doi.org/10.1038/s41598-026-38656-8
Nyckelord: läkemedelsomplacering, kunskapsgraf, djupinlärning, lungcancer, läkemedelsupptäckt