Clear Sky Science · sv
Fotoninducerad protonöverföring i vattens olika strukturer: en EPR‑metod för att lösa ett klassiskt problem
Varför protonernas dolda resor är viktiga
Varje gång du andas, tänker eller omvandlar solljus till användbar energi i en solcell är små positivt laddade partiklar som kallas protoner i rörelse. Hur dessa protoner färdas genom vatten är ett århundraden gammalt pussel, först formulerat av vetenskapsmannen Theodor Grotthuss 1806. Denna nya studie använder en smart kombination av ljus och magnetiska mätningar för att iaktta protoners rörelser i vatten med olika strukturer, från salta och trånga lösningar till iskalla, glasslika blandningar och till och med inne i ett membranprotein. Arbetet erbjuder ett nytt sätt att pröva klassiska idéer om protonrörelse och att undersöka miljöer som är svåra att studera med andra metoder.
Ett nytt sätt att se protoner röra sig
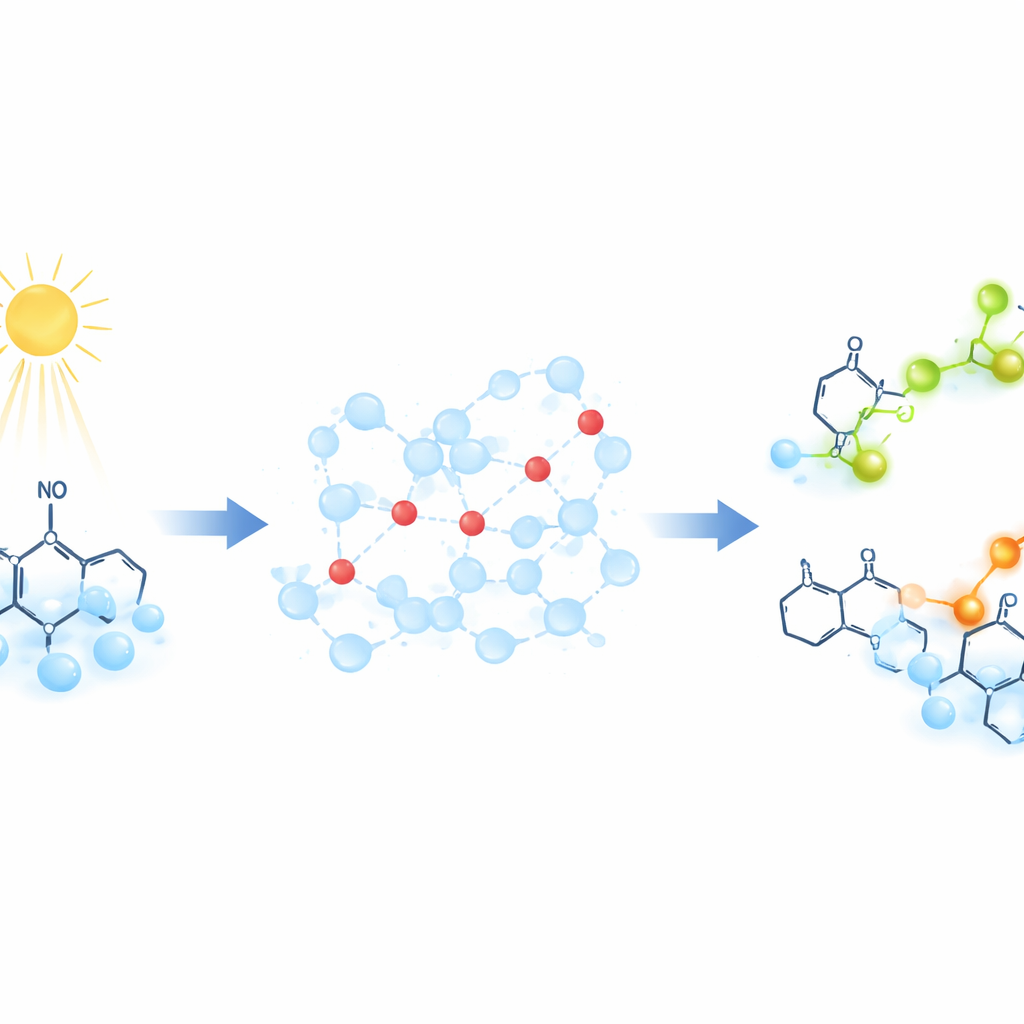
I stället för att följa protonerna direkt använder forskarna speciella ‘‘provmolekyler’’ som ändrar sin magnetiska signatur när de fångar upp en proton. Dessa prober är stabila organiska radikaler vars oparade elektron ger en välavgränsad signal i elektronparamagnetisk resonans (EPR), en teknik som detekterar hur oparade elektroner reagerar på ett magnetfält. För att starta protonrörelsen på kommando lyser teamet på en förening kallad 2‑nitrobenzaldehyd. Denna ljusdrivna reaktion frigör en skur av protoner på mindre än en miljarddels sekund och sänker plötsligt lösningens pH. När protonerna sprider sig genom vattnet och binder till proberna skiftar EPR‑signalen på ett tidsberoende sätt, vilket gör det möjligt för forskarna att följa hur snabbt protonöverföringen sker.
Hur vattnets omgivning saktar ner eller snabbar upp flödet
Vatten finns sällan ensamt; det är vanligtvis trångt med lösta salter eller andra molekyler som subtilt omorganiserar dess vätebindningsnätverk. Gruppen testade hur sådana tillsatser påverkar protonrörelsen genom att jämföra rent vatten med lösningar som innehåller kaliumklorid, urea eller guanidiniumklorid, alla i höga koncentrationer. Genom att passa EPR‑förändringarna till enkla kinetiska modeller extraherade de uppenbara hastigheter för protonöverföring. De fann att i 6 molar guanidiniumklorid var protonöverföringen ungefär 40 gånger långsammare än i rent vatten, medan 8 molar urea bara gav en måttlig inbromsning och kaliumklorid gav ett mellanresultat. Eftersom hastigheten för protonernas reaktion med proberna begränsas av hur de rör sig genom vätebindningsnätverket, pekar dessa skillnader på betydande förändringar i hur vatten är strukturerat kring de tillsatta jonerna och molekylerna.
Protonrörelse i glassigt is och inne i proteiner
Metoden är inte begränsad till vanligt flytande vatten. Författarna studerade också en vatten–glycerolblandning kyld till 160 kelvin, där den bildar en styv glasfas. Fri diffusion av molekyler är i princip frusen, men EPR‑signalen visade ändå att proberna protonerades efter ljusexponering. Detta tyder på att protonöverföring kan ske utan klassisk diffusion, möjligen genom kvanttunnelering längs en kedja av vätebindningar — en tanke som ligger i linje med moderna förfiningar av Grotthuss‑idén. För att utforska biologisk relevans fäste teamet en pH‑känslig radikal vid en specifik plats på membranproteinet bakteriorodopsin, vid gränsen mellan proteinet och det omgivande vattnet. När de utlöste protonfrigörelse med ljus observerade de ett tidsberoende EPR‑svar från denna märkta plats, vilket demonstrerar att deras metod kan övervaka protonleverans till en definierad position på en proteinyta.
Kopplingen mellan struktur, vatten och protonmotorvägar
För att bättre förstå varför den proteinbundna proben betedde sig mycket likt en i bulkvatten körde forskarna datorsimuleringar av bakteriorodopsin i ett membran och av en liten peptid i lösning. De beräknade hur vattenmolekyler omger nitroxylgruppen på spinmärkningen och fann nästan identiska lokala hydreringsmönster i båda fallen, med endast mild avskärmning av membranmiljön. Detta innebär att, åtminstone för den studerade platsen, har protoner tillgång genom ett vattenlager som liknar vanligt flytande vatten. Författarna visar också att deras prober kan användas i tidsupplösta EPR‑experiment, vilket öppnar dörren för att spåra både proton‑ och elektronrörelser tillsammans i reaktioner där de två är tätt sammankopplade.
Vad detta arbete berättar i enkla termer
I korthet förvandlar denna studie ljus till ett skarpt startskott för protonrörelse och använder sedan känsliga magnetiska prober för att se hur snabbt dessa protoner når olika mål. Genom att jämföra enkla saltslösningar, täta denaturanter, glasslika blandningar och ett membranprotein visar forskarna att protonflödet starkt formas av hur vattenmolekyler är ordnade och av den omgivande miljön. Deras metod stöder inte bara idén att protoner hoppar längs nätverk av vätebindningar, utan visar också att denna hoppning kan fortgå även när vanlig molekylär rörelse nästan är frusen. Detta nya verktyg kan hjälpa forskare att dissekera hur protoner rör sig i enzymer, energikonverterande system och nya material, och för oss närmare att kontrollera dessa små men kraftfulla laddningsbärare.
Citering: Barbon, A., Savitsky, A., Grigoriev, I. et al. Photoinduced proton transfer in differently structured water: an EPR approach to solving a classic problem. Sci Rep 16, 7983 (2026). https://doi.org/10.1038/s41598-026-38650-0
Nyckelord: protonöverföring, vattens struktur, elektronparamagnetisk resonans, vätebindningsnätverk, bakteriorodopsin