Clear Sky Science · sv
DNMT3A p.R882C-orsakad proliferation och anti-apoptotiska effekter i pankreascellslinjer
Varför denna forskning är viktig för pankreascancer
Pankreascancer är ökänd för att upptäckas sent, sprida sig snabbt och svara dåligt på behandling. De flesta patienter diagnostiseras med pankreasductalt adenokarcinom (PDAC), en särskilt aggressiv form av sjukdomen. Denna studie granskar en liten förändring i en enda gen, kallad DNMT3A, och ställer en stor fråga: kan denna subtila förändring hjälpa till att förklara varför vissa pankreascancer växer snabbare och står emot celldöd? Att förstå sådana förändringar skulle kunna öppna dörren för tidigare upptäckt och mer precisa, riktade behandlingar.
Titt närmare på en dödlig cancer
PDAC står för mer än 90 % av pankreascancerfallen och har en femårsöverlevnad på under 13 %. Den drivs ofta av välkända cancergener som KRAS och TP53, men många patienter har ändå ingen nytta av dagens målinriktade behandlingar. Nyare arbete tyder på att inte bara genmutationer utan även ”epigenetiska” förändringar—kemiska markeringar på DNA som styr vilka gener som är aktiva—spelar en central roll i denna cancer. DNMT3A är ett av huvudenzymen som skriver dessa kemiska markeringar, och dess defekter har redan kopplats till blodcancerformer som akut myeloisk leukemi.
Jakten på farliga DNA-förändringar
Forskarna samlade tumörprover och intilliggande icke‑cancerös vävnad från tre patienter med måttligt till dåligt differentierat PDAC. De använde hel‑exomsekvensering, en teknik som läser alla proteinkodande regioner i genomet, och tillämpade sedan strikta datorfilter för att skilja ofarliga DNA‑varianter från sådana som sannolikt påverkar cellbeteendet. Av hundratals förändringar begränsade de listan till 68 högriskförändringar. Bland dessa utmärkte sig en sällsynt variant i DNMT3A, känd som p.R882C, eftersom den nästan aldrig förekommer i stora populationsdatabaser och konsekvent bedömdes som skadlig av flera prediktionsverktyg.
Vad denna mutation gör inne i cellerna
DNMT3A är ett 912‑aminosyrors protein som hjälper till att etablera DNA‑metyleringsmönster—kemiska taggar som fungerar som "på"- eller "av"-brytare för gener. p.R882C‑förändringen sitter i en avgörande arbetsregion av DNMT3A, där den kan störa enzymets aktivitet. Med hjälp av 3D‑datormodeller fann teamet att proteinets övergripande form inte förändrades dramatiskt, vilket tyder på att problemet kan ligga i hur enzymet fungerar snarare än hur det veckas. För att testa detta konstruerade de pankreascellinjer (PANC‑1 och PaTu 8988t) som producerar antingen normalt DNMT3A eller p.R882C‑versionen, och jämförde dem med celler som bar en tom kontrollvektor.
Snabbare tillväxt, ökad rörlighet, mindre celldöd
Överraskande nog förändrade inte p.R882C‑mutationen hur mycket DNMT3A som producerades på RNA‑ eller proteinnivå; mängden enzym förblev ungefär densamma. Men dess närvaro hade slående effekter på cellbeteendet. I koloni‑bildnings‑ och tillväxttester bildade celler med mutant DNMT3A fler kolonier och visade starkare tillväxtsignaler än de med den normala versionen. Sår‑läknings‑ och Trans‑well‑tester, som mäter hur snabbt celler förflyttar sig, visade att celler med mutationen migrerade snabbare. När teamet undersökte programmerad celldöd (apoptos) med flödescytometri hade celler med p.R882C‑mutationen avsevärt färre döende celler, både i tidiga och sena apoptosstadier, vilket indikerar en stark överlevnadsfördel.
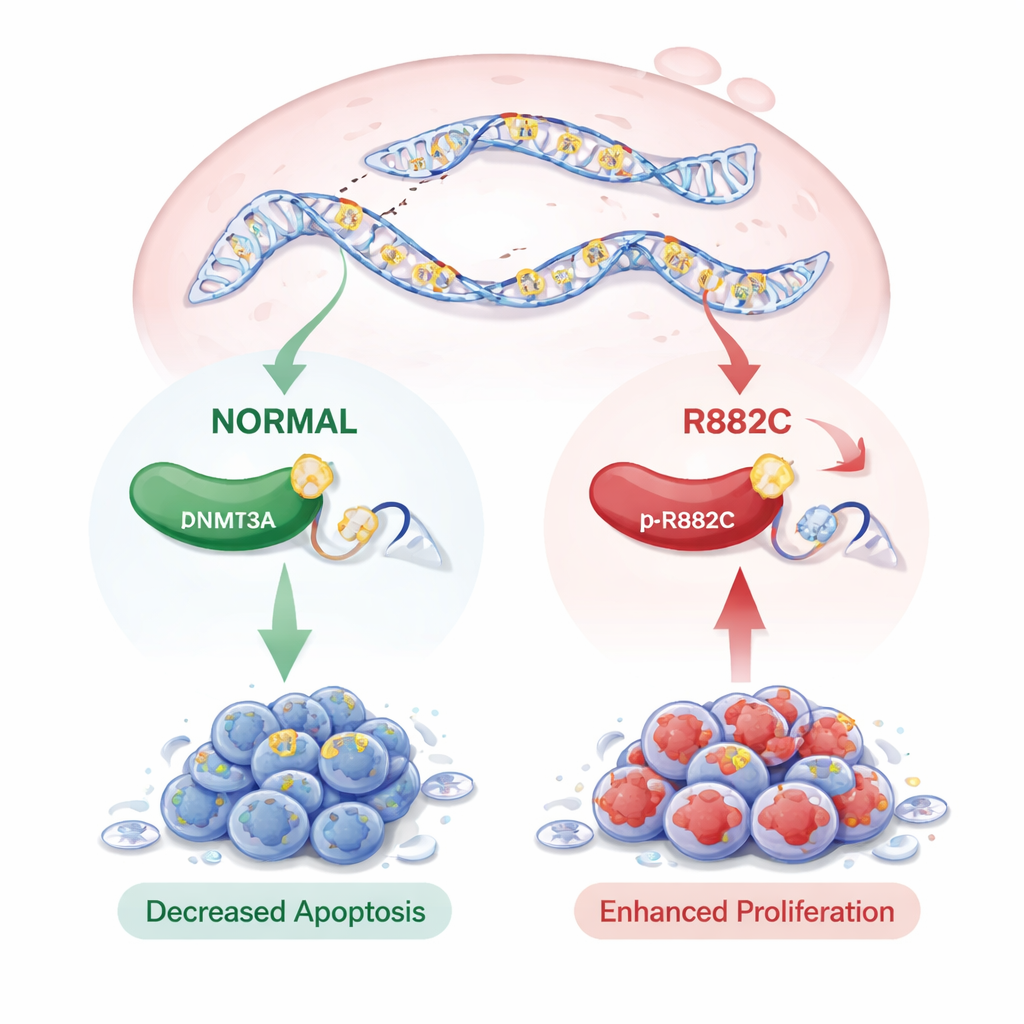
Vad detta kan innebära för framtida vård
Sammanvägt tyder resultaten på att den sällsynta DNMT3A p.R882C‑mutationen hjälper pankreascellslinjer att växa snabbare, röra sig lättare och motstå självdestruktion—egenskaper som kan bidra till cancerprogression. Även om mutationen inte ökar DNMT3A‑nivåerna, ändrar den sannolikt enzymets aktivitet och mönstret av DNA‑markeringar över genomet, vilket liknar vad som setts i vissa blodcancerformer. Författarna noterar att denna förändring är ovanlig och ännu inte visat tydliga samband med patientöverlevnad i offentliga databaser, delvis eftersom tillgängliga studier är små och ofta inte inkluderar DNMT3A. Att ändå identifiera denna mutation i PDAC lyfter fram en potentiellt viktig ny aktör i sjukdomen och väcker möjligheten att DNMT3A p.R882C i framtiden skulle kunna fungera som markör för risk eller som mål för mer skräddarsydd behandling.
Citering: Qu, Z., Mao, J., Qian, Y. et al. DNMT3A p.R882C driven proliferation and anti-apoptotic effects in pancreatic cancer cells. Sci Rep 16, 7659 (2026). https://doi.org/10.1038/s41598-026-38613-5
Nyckelord: pankreascancer, DNMT3A-mutation, PDAC, DNA-metylering, målinriktad terapi