Clear Sky Science · sv
Genomredigering över Dictyostelia-arter möjliggör jämförande funktionell genetik av sociala amöbor
Hur enskilda celler slår sig ihop
Det mesta av tiden lever amöbor som små ensamvargar som kryper runt i jorden och äter bakterier. Men några av dem, kallade sociala amöbor, kan plötsligt gå samman till en flercellig kropp med ett primitivt ”huvud” och en ”stam”. Denna ombytbara livsstil ger forskare ett ovanligt fönster in i hur enkla celler lär sig samarbeta och specialisera sig — viktiga steg i utvecklingen av komplexa livsformer. Den nya studien beskriver ett verktyg för genomredigering som äntligen låter forskare undersöka dessa beteenden inte bara i en vanlig laboratorieart utan över flera avlägsna amöbarter.
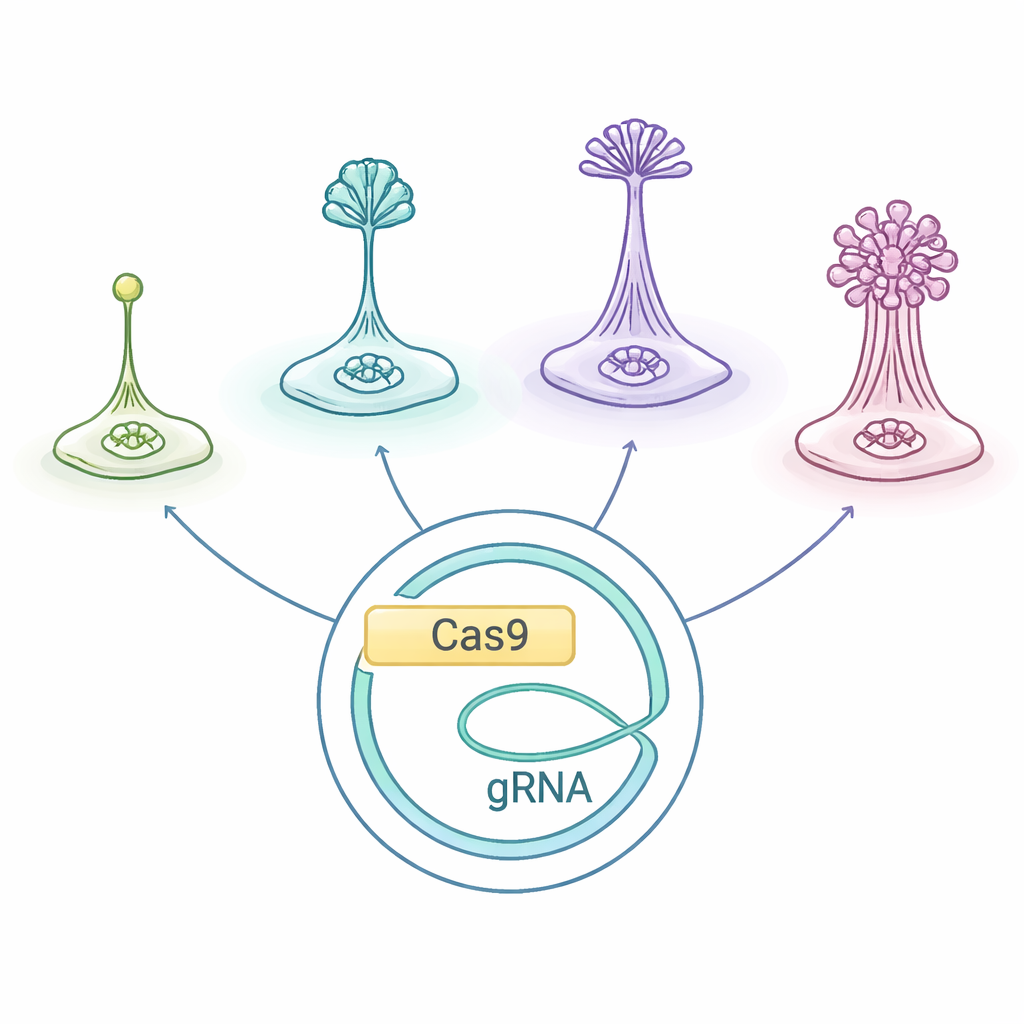
Små varelser med stora sociala liv
Sociala amöbor, samlade under Dictyostelia, lever som enskilda celler när det finns gott om föda. När de svälter börjar de sända kemiska nödropssignaler och krypa mot varandra, samlas till en kulle som bygger en miniatyr ”fruktkropp”: en pelare av uppoffrande skaftceller som höjer hårda sporer i luften. Olika Dictyostelia-linjer bygger dessa strukturer på olika sätt och med olika uppsättningar celltyper, vilket gör dem till ett naturligt laboratorium för att fråga hur flercellig kropp och arbetsfördelning utvecklas.
En modellart räckte inte
Hittills har nästan allt molekylärt arbete koncentrerats till en enda art, Dictyostelium discoideum, eftersom dess gener är relativt lätta att modifiera. Det lämnade mer än etthundra andra kända arter — några som representerar tidigare grenar i Dictyostelia-släktskapet — i stort sett outforskade. Dessa försummade arter har särpräglade livshistorier, signalsystem och kroppsplaner. För att förstå hur flercellighet förändrats över tiden behöver forskare kunna manipulera samma gener i många av dessa arter och jämföra resultaten sida vid sida.
Att föra CRISPR till en mångsidig amöbfamilj
Forskarna anpassade ett CRISPR/Cas9-genredigeringssystem som ursprungligen optimerats för D. discoideum och testade om det fungerar över Dictyostelia-trädet, inklusive både tidigt avgrenade och mer härledda arter. De använde ett plasmid — en extra cirkulär DNA-bit — som bär instruktionerna för Cas9s ”molekylära sax”, guide-RNA:t som pekar Cas9 mot en vald gen, och en drogresistensmarkör. Att introducera denna plasmid i olika amöbor gjorde det möjligt för teamet att klippa två välstuderade gener, kallade stlA och pkaC, vilka är viktiga för signalerna som samordnar aggregering och korrekt bildning av fruktkroppar. I jordamöban Polysphondylium violaceum gav denna strategi pålitligt mutanter med tydliga utvecklingsdefekter, vilket visar att det lånade systemet kan fungera utanför den vanliga modellen.
Testa gener över arter
Nästa steg var att gå vidare till mer avlägset besläktade arter, inklusive Heterostelium pallidum från Grupp 2 och Cavenderia fasciculata från Grupp 1 — linjer som skildes tidigare i evolutionen. Med samma plasmiddesign störde de pkaC-genen i båda arterna och fann att mutanterna inte lyckades aggregera och bygga normala fruktkroppar, vilket speglade de allvarliga defekter som ses i D. discoideum. Eftersom CRISPR-mutationer som skapats med denna metod inte lämnar kvar klumpiga selektionskassetter var de framtagna stammarna ”markör-fria”. Det gjorde det enkelt att återföra en version av genen från D. discoideum och testa om den kunde ersätta den lokala varianten. I samtliga fall kunde den främmande pkaC rädda det tidiga aggregeringssteget men inte den senare formningen av en mogen fruktkropp — ett bevis för att den grundläggande signalverktygslådan är delad, medan finjusterad kontroll av tid och position har utvecklats på art-specifika sätt.
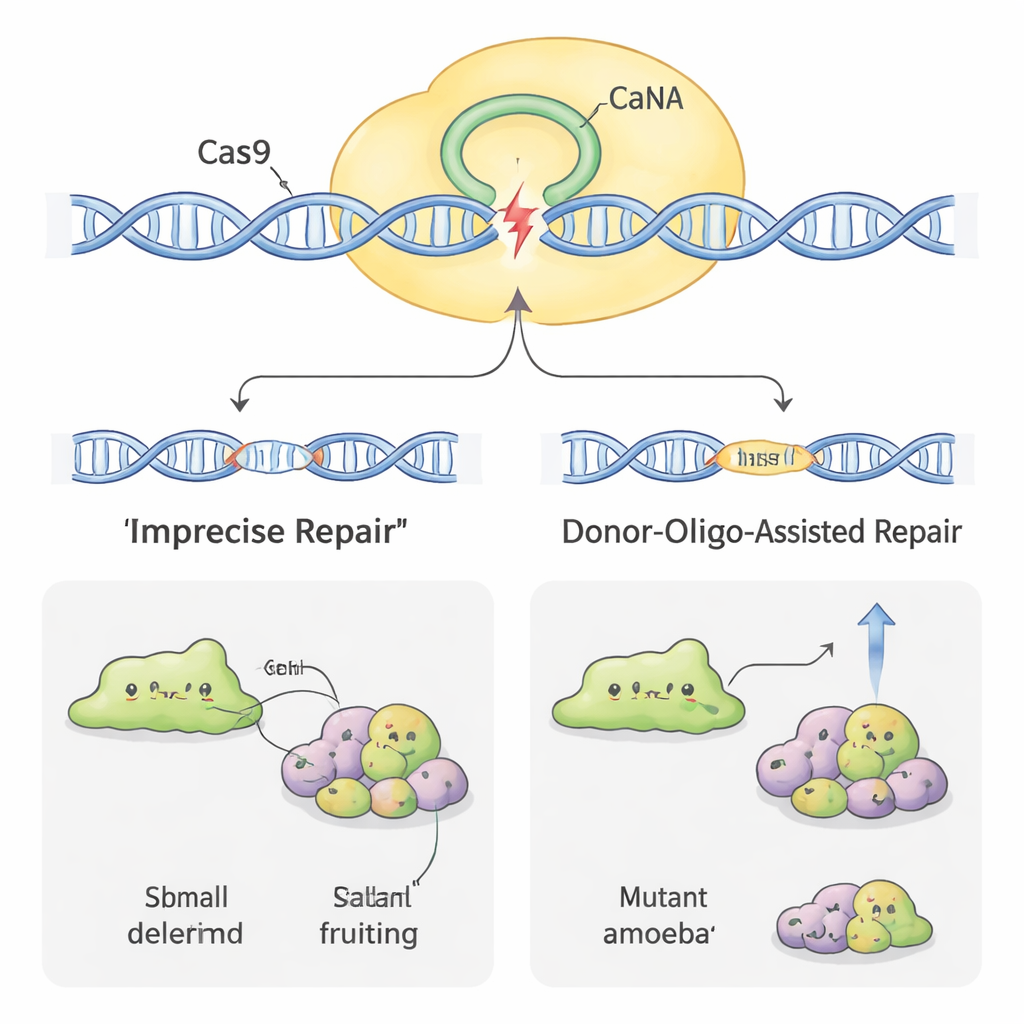
Göra redigering mer effektiv
Inte alla amöbor lät sig redigeras lika lätt. I vissa arter, såsom H. pallidum, var den initiala framgångsfrekvensen mycket låg. För att öka effektiviteten lånade forskarna en annan taktik: att lägga till korta ”donor”-DNA-snuttar tillsammans med CRISPR-plasmiden. Dessa donorer bär en liten tagg och en stoppsignal omgiven av korta regioner som matchar målgenen. När cellen reparerar Cas9-klippet med donorn som mall bryts genen på ett igenkännbart sätt. I D. discoideum ökade detta andelen defekta kloner och gjorde det till och med möjligt för teamet att få fram mutanter utan att använda kontinuerlig drogselektion. I den mer motsträviga H. pallidum ökade kombinationen av donor-DNA och några dagars drogbehandling mutationsfrekvenserna med nästan en storleksordning, och gjorde tidigare sällsynta händelser nära nog rutin.
Öppnar ett fönster mot komplexitetens ursprung
För en icke-specialist kan detaljer om plasmiddesigner och reparationsmallar låta tekniska, men vinsten är bred: en flexibel CRISPR-verktygslåda som fungerar över flera grenar i den sociala amöbafamiljens träd. Med den kan forskare nu jämföra hur samma gen formar utveckling i olika arter, och hur subtila förändringar i genreglering eller proteinstruktur hjälper till att skapa nya celltyper och kroppsplaner. Med andra ord förser detta arbete forskare med de genetiska verktygen som behövs för att i levande detalj iaktta hur evolutionen knappte och justerade encelliga organismer för att bygga kooperativa flercelliga samhällen.
Citering: Oishi, S., Doi, S., Sekida, T. et al. Genome editing across Dictyostelia species enables comparative functional genetics of social amoebas. Sci Rep 16, 7457 (2026). https://doi.org/10.1038/s41598-026-38605-5
Nyckelord: sociala amöbor, CRISPR-genomredigering, evolution av flercellighet, Dictyostelium, celldifferentiering