Clear Sky Science · sv
Aktiverade T‑celler inducerar apoptos i A549-lungadenokarcinomceller via TRPV4‑medierat kalciuminflöde
Varför denna forskning spelar roll för lungcancer
Lungcancer är fortfarande en av de dödligaste cancerformerna, delvis därför att tumörer ofta utvecklar resistens mot standardbehandlingar som cytostatika och strålning. Under de senaste åren har utnyttjandet av kroppens eget immunsystem gett nytt hopp. Denna studie undersöker en nyans av den idén: den visar hur en specifik typ av immuncell, så kallade aktiverade T‑celler, kan driva lungcancerceller mot självförstörelse genom att tvinga in kalcium via en molekylär ”grind” känd som TRPV4. Att förstå denna väg kan hjälpa forskare att utforma mer kraftfull och precis immunterapi.
Immunförsvarets soldater möter lungtumörceller
Forskarlaget fokuserade på humana lungadenokarcinomceller kända som A549‑celler, en ofta använd modell för icke‑småcellig lungcancer. De parade dessa cancerceller med Jurkat‑T‑celler, en modell för kroppens cytotoxiska T‑celler som normalt söker upp och förstör infekterade eller maligna celler. Genom att kemiskt aktivera Jurkat‑cellerna efterliknade teamet det högaktiva tillstånd som T‑celler har under ett verkligt immunsvar. De blandade sedan aktiverade eller inaktiva T‑celler med lungcancerceller i olika proportioner och observerade vad som hände under en till tre dagar, med särskilt fokus på hur många cancerceller som överlevde och hur många som genomgick programmerad celldöd, apoptos.
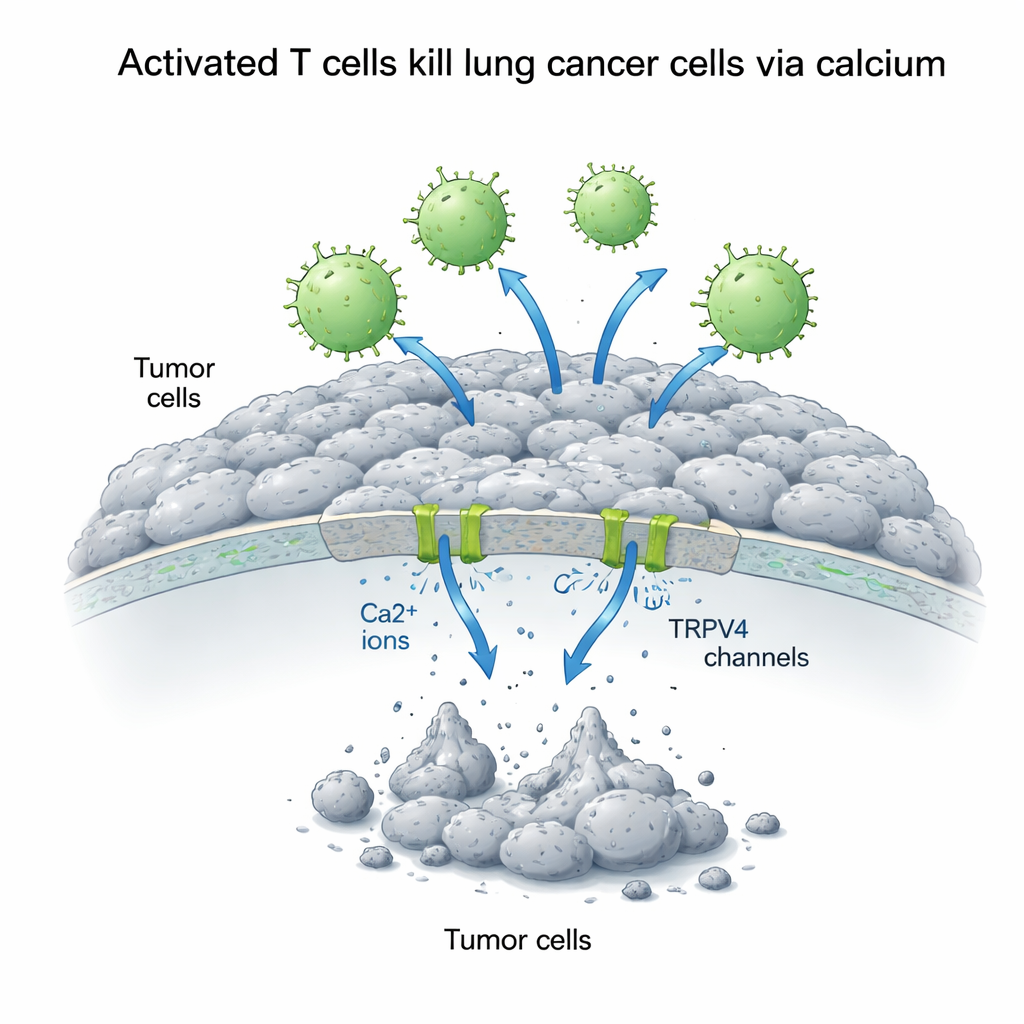
Kalcium som ett tveeggat signalämne för cancerceller
Kalcium inne i celler fungerar som en mångsidig signalomkopplare som antingen kan främja tillväxt eller utlösa död, beroende på hur det hanteras. Forskarna ökade mängden kalcium utanför A549‑cellerna och mätte hur detta påverkade samspelet mellan T‑celler och tumörceller. Överraskande nog gjorde extra kalcium ensam att lungcancercellerna växte bättre, vilket tyder på att kalcium under lugna förhållanden driver överlevnadsvägar. Men när aktiverade T‑celler var närvarande vände sig bilden: högre extracellulärt kalcium förstärkte dramatiskt T‑cellernas dödande. Över 72 timmar sjönk cancercellernas överlevnad till mindre än en tredjedel av normal när både aktiverade T‑celler och extra kalcium kombinerades, medan inaktiva T‑celler hade liten effekt och till och med kunde stödja tillväxt när kalcium tillsattes.
En kalcium"grind" kopplad till stress och celldöd
För att förstå hur denna växling från tillväxt till död sker undersökte teamet TRPV4, en proteinkanalsom i cellmembranet som tillåter kalcium att flöda in. Med proteinanalys fann de att TRPV4‑nivåerna steg kraftigt när A549‑celler exponerades för tillsatt kalcium, oavsett om T‑celler var närvarande eller inte, och var högst när kalcium och aktiverade T‑celler kombinerades. Samtidigt visade cancercellerna tydliga tecken på oxidativ stress: balansen försköts bort från skyddande antioxidanter (lägre total antioxidantkapacitet) och mot skadliga oxidanter (högre total oxidativ status). Flödescytometri, en teknik som märker celler med fluorescerande färgämnen, bekräftade att aktiverade T‑celler orsakade en kraftig ökning i både tidiga och sena stadier av apoptos, särskilt när kalcium var rikligt. Tillsammans tyder dessa observationer på en händelsekedja där TRPV4‑kanaler släpper in mer kalcium, vilket sedan driver kemisk stress inuti cellen och skjuter den mot död.
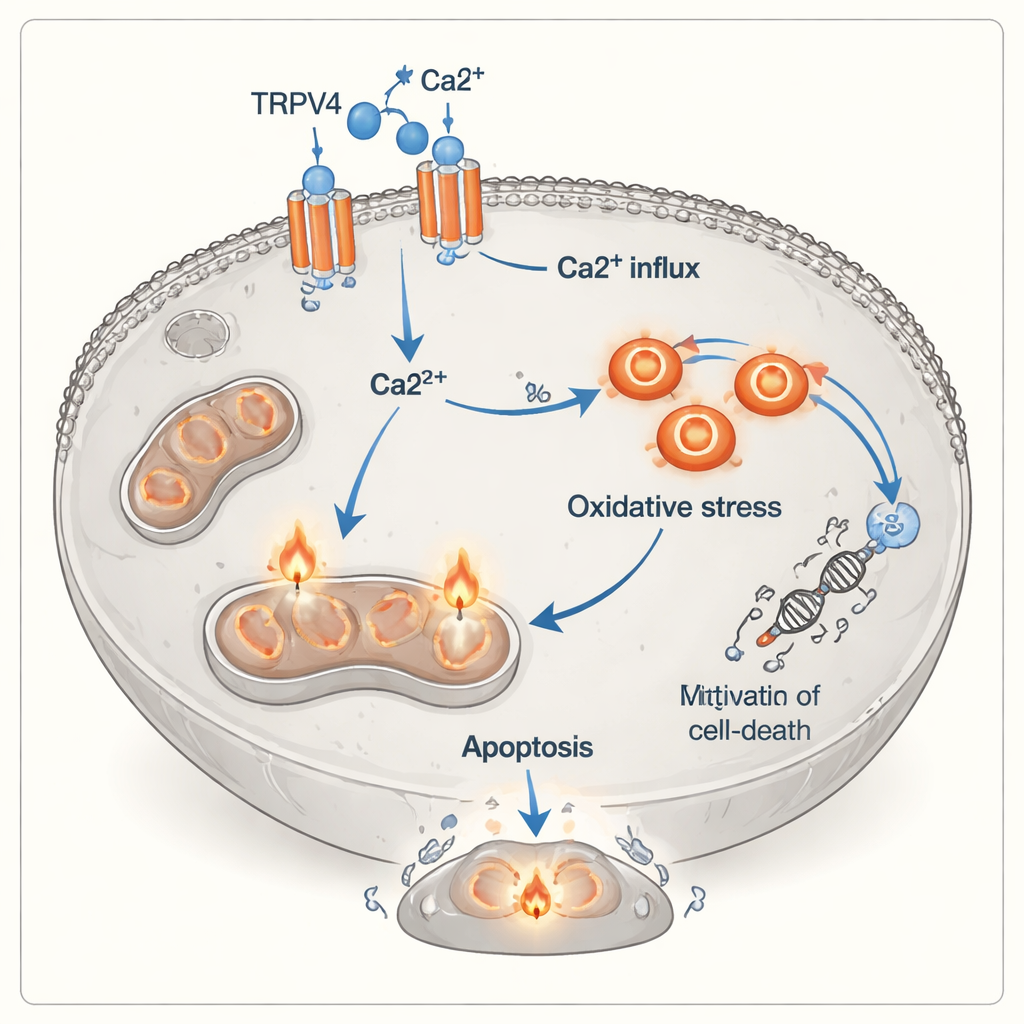
En ny dimension i hur immunceller dödar tumörer
Traditionellt förstör cytotoxiska T‑celler sina mål genom att frigöra toxiner eller genom att aktivera dödsreceptorer på cancercellens yta. Denna studie föreslår att det finns en annan, mer indirekt väg: signaler från aktiverade T‑celler — inklusive inflammatoriska molekyler och nära cell‑till‑cellkontakt — verkar göra lungcancerceller mer beroende av TRPV4 och mer sårbara för kalciumöverbelastning och oxidativ skada. I denna syn fungerar TRPV4 som en sensibiliserande brytare som förvandlar annars tillväxtfrämjande kalcium till en dödlig signal. Även om experimenten utfördes i odlingsskålar och med en enda cancercellinje, lyfter de fram en potentiellt viktig länk mellan immunangrepp, jonkanaler och tumörcellernas interna stressmaskineri.
Vad detta kan betyda för framtida behandlingar
För icke‑specialister är slutsatsen att framgången för immunterapi kanske inte bara beror på att göra T‑celler starkare, utan också på att göra cancerceller lättare att döda. Genom att rikta in sig på TRPV4 eller relaterade kalciumkanaler skulle läkare en dag kunna förstärka T‑cellernas förmåga att eliminera lungtumörer eller finjustera behandlingar för att undvika skada på frisk vävnad. Arbetet befinner sig fortfarande i ett tidigt skede, och författarna understryker behovet av ytterligare experiment i djur och mer komplexa modeller. Ändå lägger upptäckten av en TRPV4–kalcium–oxidativ stress‑axel till ett lovande nytt mål i verktygslådan för att förbättra immunbaserade terapier mot lungcancer.
Citering: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
Nyckelord: immunterapi mot lungcancer, T‑celler, kalciumsignalering, TRPV4‑kanal, oxidativ stress