Clear Sky Science · sv
Optimering av galectin-3-bindande ämnen genom in situ-syntes av flera föreningar och nativer masspektrometri
Varför detta är viktigt för framtida läkemedel
Många moderna läkemedel fungerar genom att fästa vid proteiner i våra kroppar, men att hitta en liten molekyl som binder starkt och selektivt till exakt rätt plats är långsamt, kostsamt och ofta frustrerande. Denna studie presenterar ett snabbare sätt att finjustera sådana molekyler direkt i närvaro av målproteinet och därefter identifiera vinnarna med en mycket känslig vägningsteknik. Författarna demonstrerar sitt angreppssätt på galectin-3, ett protein kopplat till cancerutveckling, och får fram en lovande läkemedelslik kandidat som binder lika starkt som några av de bästa befintliga föreningarna, men i en oväntad ficka på proteinytan.

Ompröva hur vi söker bättre läkemedelskandidater
Traditionell optimering av läkemedel liknar ett dyrt gissningsspel. Kemister ändrar en startförening steg för steg, testar varje version och hoppas förbättra hur väl den binder till målproteinet. Men proteinytor är flexibla, vattenmolekyler stör och bindningstillfället kan omforma proteinet, vilket gör datorbaserade förutsägelser opålitliga. Även när en högupplöst struktur finns tillgänglig finns ingen garanti för att en föreslagen ändring faktiskt hjälper. Befintliga "målstyrda" metoder försöker låta proteinet välja sina egna partners från en pool byggstenar, men dessa angreppssätt förlitar sig fortfarande på komplex analys och indirekta signaler för att avgöra vilken förening som verkligen binder bäst.
Låt proteinet välja, och väg sedan vinnarna
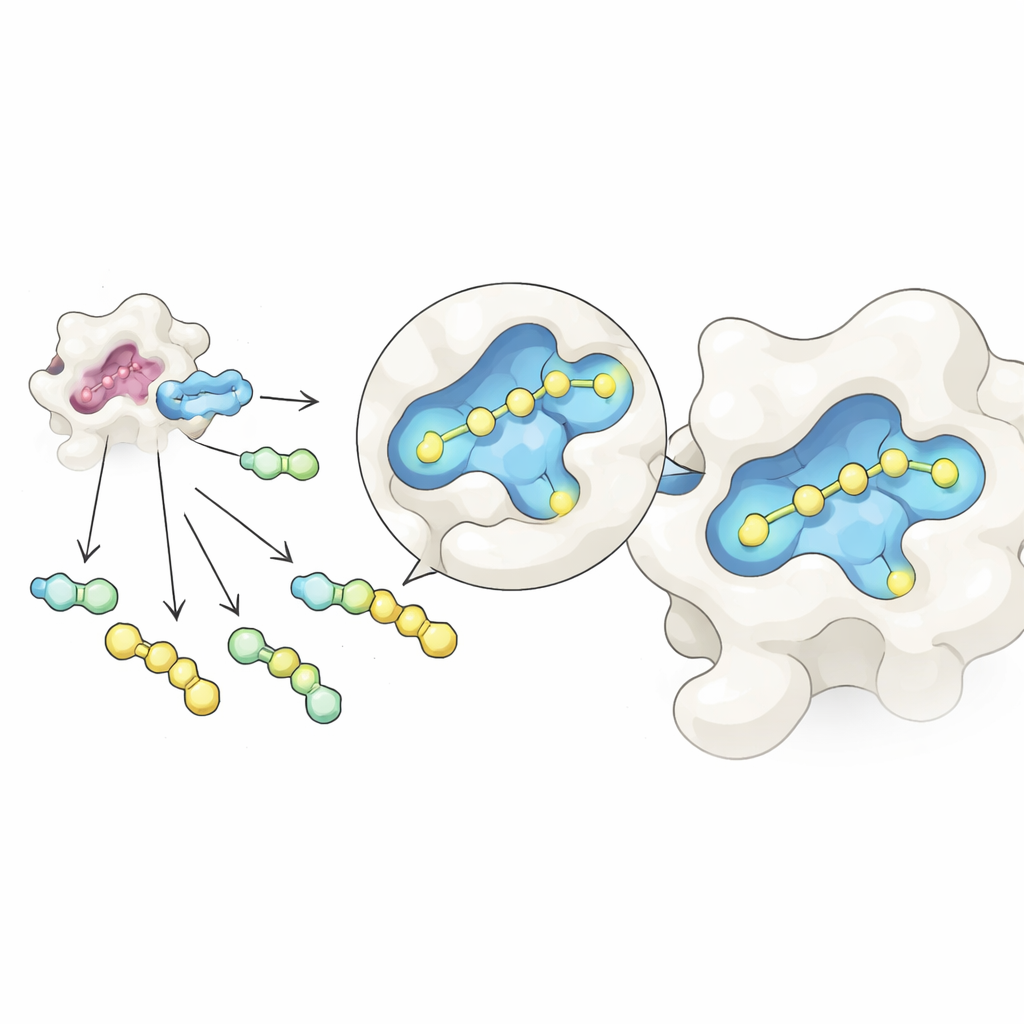
Forskarna kombinerade två idéer i ett effektivt arbetsflöde. För det första använde de en reversibel kemisk reaktion som kopplar en gemensam sockerbaserad kärna till många olika sidogrupper i ett enda rör och bildar en blandning av besläktade molekyler. Genom att noggrant justera utgångsandelarna når produkterna en jämvikt styrd av enkla koncentrationsregler, vilket hjälper till att utjämna deras mängder trots skillnader i rå reaktivitet. För det andra utsatte de denna blandning för galectin-3 och undersökte den med nativer masspektrometri, en form av masspektrometri som håller protein–molekylpar intakta i en skonsam, vattenliknande lösning. Eftersom varje kandidat har en distinkt massa kan instrumentet direkt upptäcka vilka molekyler som faktiskt är bundna till proteinet, utan några märken eller referensmarkörer.
Från täta blandningar till en framträdande binder
Med detta upplägg skapade teamet dussintals galectin-3-bindare genom att fästa olika sidogrupper på en sockerstomme inspirerad av en känd hämmare, GB1107. De delade upp 35 olika hydrazidbitar i hanterbara grupper, bildade alla kombinationer in situ och tillsatte sedan galectin-3. Nativer masspektrometri framhävde de föreningar som oftast reste tillsammans med proteinet och markerade dem som primära träffar. Ett uppföljande termiskt stabilitetstest, som mäter hur en förening stabiliserar proteinet vid uppvärmning, sållade bort falska positiva orsakade av egenskaper i gasfasmätningen. Tre ledande kandidater återstod, och detaljerade värmebaserade bindningsmätningar visade att en, kallad GalAldBZ20, band galectin-3 särskilt starkt, i submikromolärt område.
Upptäckt av en dold ficka och förstärkning av bindningen
Nästa överraskning kom när teamet studerade hur GalAldBZ20 låg på ytan av galectin-3. De flesta kända bindare använder en "alfa"-ficka nära sockerbindningsstället, men strukturella metoder och datorbaserade simuleringar indikerade att GalAldBZ20 istället föredrog en närliggande "beta"-ficka. Röntgendiffraktion antydde detta, kärnmagnetisk resonans i lösning visade flera lokala konformationer nära den fickan, och molekyldynamiksimuleringar stödde en modell där en nitrobärande ring på molekylen ligger inbäddad i beta-stället. Med tanke på att de kunde låsa denna ordning mer stabilt, redesignade kemisterna länkaren mellan socker och nitro-ring för att uppmuntra nya polära kontakter med proteinet och minska flexibiliteten.
Att förvandla en smart screening till en kraftfull kandidat
Med denna insikt syntetiserade teamet en liten serie mer styva uppföljningsmolekyler som behöll samma socker och nitro-ring men ändrade förbindelsen däremellan. En version, en N-galaktosid (förening 5), utmärkte sig: den band galectin-3 ungefär tio gånger starkare än den ursprungliga träffen och nådde en bindningsstyrka jämförbar med GB1107, men föredrog fortfarande beta-fickan. En extremt högupplöst kristallstruktur visade tydlig densitet för nitro-ringen i den fickan, stödd av flera vätebindningar och en kation-π-interaktion med nyckelaminosyror. När nitrogruppen togs bort eller ersattes med en enkel metylgrupp försvagades bindningen markant, vilket underströk dess betydelse. Eftersom galectin-1, ett närbesläktat protein, saknar denna beta-ficka kan den nya föreningen potentiellt erbjuda bättre selektivitet, en eftertraktad egenskap i läkemedelsdesign.
Vad detta betyder för framtida läkemedelsupptäckt
På ett tillgängligt sätt visar detta arbete att man kan blanda många besläktade molekyler, låta ett sjukdomsrelevant protein "välja" sina favoriter och sedan direkt väga dessa protein–molekylpar för att se vilka som binder bäst. Tillämpat på galectin-3 fann denna strategi oväntat och därefter förstärkte bindningen till en mindre utforskad ficka, vilket gav en förening som kan mäta sig med några av de bästa befintliga hämmarna och som kan fungera som en utgångspunkt för nya anticancerläkemedel. Mer generellt erbjuder kopplingen mellan in situ-kemi och nativer masspektrometri en generell genväg för att förfina läkemedelskandidater mot proteiner med flera möjliga bindningsställen, vilket kan spara tid, material och arbete i de tidiga skedena av läkemedelsupptäckt.
Citering: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
Nyckelord: galectin-3-hämmare, nativer masspektrometri, fragmentbaserad läkemedelsupptäckt, målinriktad syntes, cancerläkemedelskandidater