Clear Sky Science · sv
Integrativ analys av transkriptom och enskild-cellssekvensering kombinerat med experimentell validering identifierar biomarkörer kopplade till T‑celler och senescens vid sepsis
Varför denna forskning är viktig för patienter med allvarliga infektioner
Sepsis är en livshotande reaktion på infektion som kan förvandla en vanlig sjukdom eller skada till en akut situation, ofta inom några timmar. Läkarna saknar fortfarande ett enkelt, pålitligt sätt att tidigt upptäcka vilka patienter som är på väg mot organsvikt, och det finns inga läkemedel utvecklade specifikt för att korrigera det immunciella kaos som sepsis orsakar. Den här studien undersöker hur vissa immunceller, kallade T‑celler, och åldrande i dessa celler kan driva sepsis — och identifierar en liten uppsättning gener som kan hjälpa läkare att diagnostisera tillståndet tidigare och peka ut nya behandlingsmöjligheter.
Sepsis: när kroppens försvar spårar ur
Vid sepsis exploderar immunsystemet först i en intensiv inflammatorisk respons för att sedan ofta gå in i en farlig nedstängning. T‑celler, som normalt hjälper till att rensa bort infektioner och minnas tidigare infektioner, blir färre och mindre kapabla att bekämpa patogener. Samtidigt visar många immunceller tecken på "senescens" — en form av cellulärt åldrande där celler slutar dela sig men fortsätter att släppa ut inflammatoriska signaler. Författarna förutsatte att om de kunde identifiera gener som kopplar både till T‑celler och till senescens, så kunde de finna nya biomarkörer som avslöjar vem som utvecklar sepsis och varför vissa patienter försämras snabbare än andra.
Att gräva i blod på enskild‑cellsnivå
Forskargruppen kombinerade flera datalager från blodprover från personer med och utan sepsis. De använde först bulk‑transkriptomdata (en avläsning av vilka gener som är aktiva) för att hitta nästan 10 000 gener vars aktivitet förändrades vid sepsis. Därefter undersökte de med hjälp av enskild‑cells RNA‑sekvensering tiotusentals individuella blodceller för att identifiera mer än 1 300 gener som särskilt var förändrade i T‑celler. Genom att överlappa dessa uppsättningar med en kurerad lista på 866 gener kända för att vara involverade i cellulärt åldrande, smalnade de fältet ner till 45 kandidater som låg i korsningen mellan sepsis, T‑celler och senescens. 
Hitta fyra nyckelgenetiska vägvisare
För att filtrera listan ytterligare använde forskarna två maskininlärningstekniker som letar efter de mest informativa funktionerna i komplexa data. Dessa metoder konvergerade mot sex lovande gener, och när teamet kontrollerade två oberoende patientdataset stack fyra av dem konsekvent ut: PATZ1, SIN3B, BLK och MTHFD2. I offentliga data var PATZ1, SIN3B och BLK nedreglerade vid sepsis, medan MTHFD2 var uppreglerad. I en liten grupp kliniska prov som testades med en känslig metod kallad RT‑qPCR var de tre första generna återigen tydligt lägre i sepsispatienters blod, medan MTHFD2 inte visade någon klar skillnad — vilket antyder att dess roll kanske mer rör proteinets funktion än mängden som produceras.
Hur dessa gener kopplas till immunbalans och potentiella läkemedel
Ytterligare analyser kopplade varje gen till bredare biologiska vägar. PATZ1 var kopplad till DNA‑replikation och T‑cellreceptor‑signalering, processer som är viktiga för att T‑celler ska kunna föröka sig och reagera på infektion. SIN3B var associerad med ett lipidbaserat signalsystem som påverkar cellsurvival och inflammation. BLK, mer känt från autoimmuna sjukdomar, var förknippat med blodcellsutveckling och tarmens immunförsvar, inklusive produktion av IgA‑antikroppar som skyddar tarmbarriären. MTHFD2 var kopplat till maskineriet för proteinsyntes och nedbrytning, centralt för hur immunceller anpassar sin metabolism under stress. När teamet undersökte mönster av immuncells"infiltration" i blod korrelerade högre PATZ1‑nivåer med fler CD8‑T‑celler och färre neutrofiler, en balans som kan gynna bättre kontroll av infektion. Med hjälp av dessa fyra gener byggde forskarna ett artificiellt neuralt nätverk — en enkel AI‑modell — som särskilde sepsis från icke‑sepsisfall i två externa dataset med nästintill perfekt noggrannhet. De använde också en läkemedels‑gen‑databas och molekylär dockningsimuleringar för att föreslå flera befintliga föreningar, inklusive antibiotikumet latamoxef och molekylerna emetin och dihydroergotamin, som kandidater som binder starkt till dessa mål. 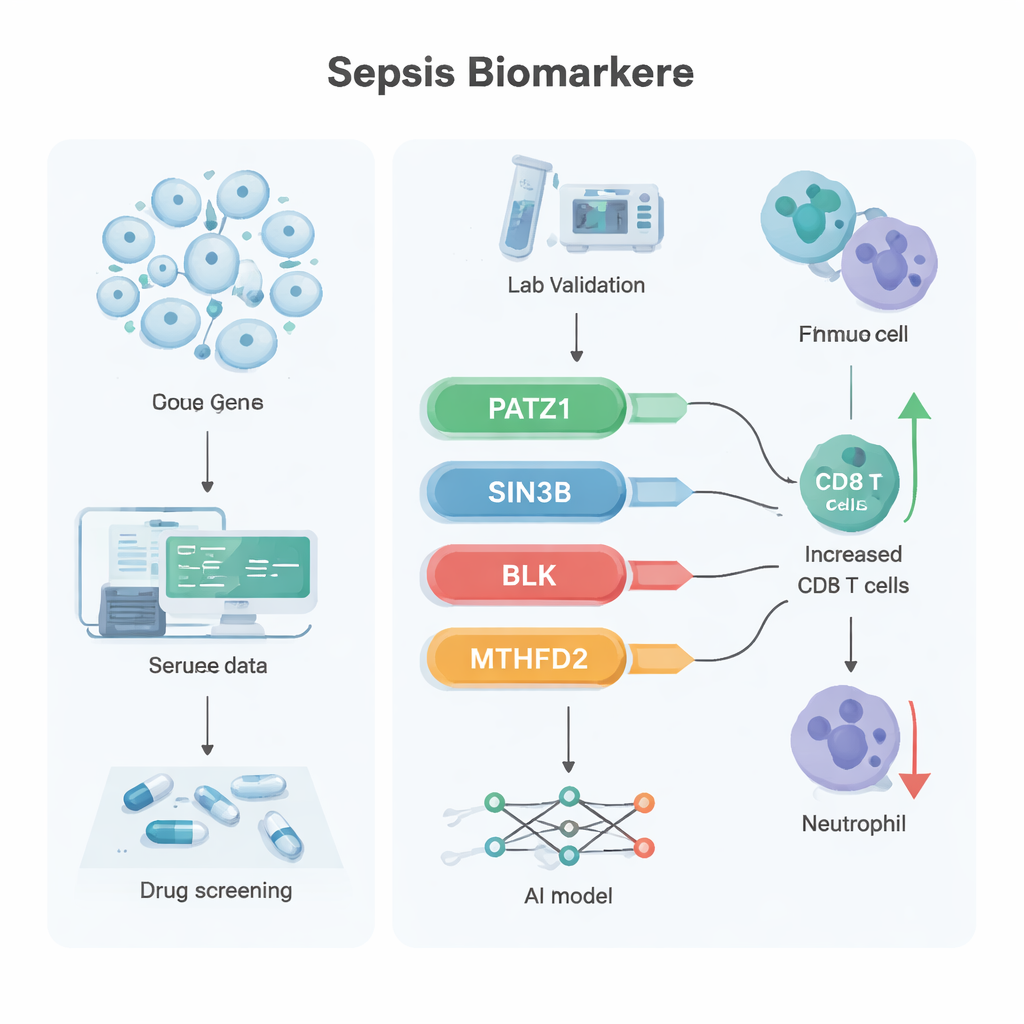
Vad detta kan innebära för framtida vård
För lekmannen är huvudpoängen att denna studie identifierar fyra gener som fungerar som varningssignaler på T‑celler som felaktigt aktiveras och åldras för tidigt under sepsis. Tillsammans utgör dessa gener ett potentiellt blodtestpanel som en dag kan hjälpa läkare att diagnostisera sepsis tidigare och mer träffsäkert än dagens verktyg. De ger också ledtrådar till hur immunsystemets energianvändning och reparationssystem fallerar, vilket föreslår nya angreppssätt för läkemedel utformade för att återställa T‑cellernas normala funktion snarare än enbart dämpa inflammation. Även om större studier och laboratorieexperiment krävs innan någon av dessa fynd når kliniken, kartlägger detta arbete en lovande väg mot mer precis, biologi‑baserad diagnostik och behandling av sepsis.
Citering: Yang, K., Hu, Y., Ma, C. et al. Integrative analysis of transcriptome and single-cell sequencing combined with experimental validation identifies biomarkers associated with T cell and senescence in sepsis. Sci Rep 16, 7109 (2026). https://doi.org/10.1038/s41598-026-38559-8
Nyckelord: sepsisbiomarkörer, T‑celler, immunologisk senescens, enskelcellssekvensering, immunometabolism