Clear Sky Science · sv
Jämförelse och kombination av xevinapant med ATR‑ och PARP‑hämning för radiosensibilisering av HPV‑negativa HNSCC‑celler
Varför det är viktigt att förstärka strålbehandling
Strålbehandling är en grundpelare vid cancer i mun och svalg, men många tumörer är motståndskraftiga vilket tvingar läkare att använda höga doser som kan skada frisk vävnad. Denna studie ställer en praktisk fråga med stora konsekvenser för patienter: bland flera moderna cancerläkemedel som är utformade för att göra tumörceller mer sårbara, vilka fungerar egentligen bäst tillsammans med strålning mot svårbehandlade, HPV‑negativa huvud‑ och halscancerceller odlade i laboratoriet?
Dagens behandling och dess begränsningar
Personer med lokalt avancerad skivepitelcancer i huvud och hals behandlas ofta med en kombination av strålning och cytostatikan cisplatin, eller med operation följt av strålning. Även om detta kan kontrollera cancer lämnar det ofta patienter med allvarliga långvariga biverkningar såsom sväljsvårigheter, muntorrhet, hörselproblem och njurskador. Många äldre eller medicinskt sårbara patienter tål inte cisplatin alls. Det har drivit ett stort intresse för så kallade ”radiosensibilisatorer” – läkemedel som gör tumörceller lättare att döda med strålning så att behandlingen kan bli mer effektiv eller, möjligtvis, mer skonsam.
Ett lovande läkemedel som snubblade
Ett sådant läkemedel, xevinapant, hyllades inledningsvis som ett genombrott. Det efterliknar ett naturligt protein kallat SMAC och blockerar molekyler som hjälper cancerceller att undvika programmerad celldöd. I tidigare arbete förbättrade tillägg av xevinapant till standard kemoradioterapi resultaten i en fas 2‑studie för huvud‑ och halscancer, vilket väckte förhoppningar om att det kunde bli en ny vårdstandard. Men en mycket större fas 3‑studie, kallad TrilynX, avbröts i förtid när preliminära data visade inte bara utebliven nytta utan även sämre överlevnad och fler biverkningar i xevinapant‑gruppen. Det oväntade fiaskot skapade ett akut behov av att ompröva hur väl xevinapant verkligen förbättrar strålning och att jämföra det med andra, nyare strategier.
Tre strategier ställda mot varandra
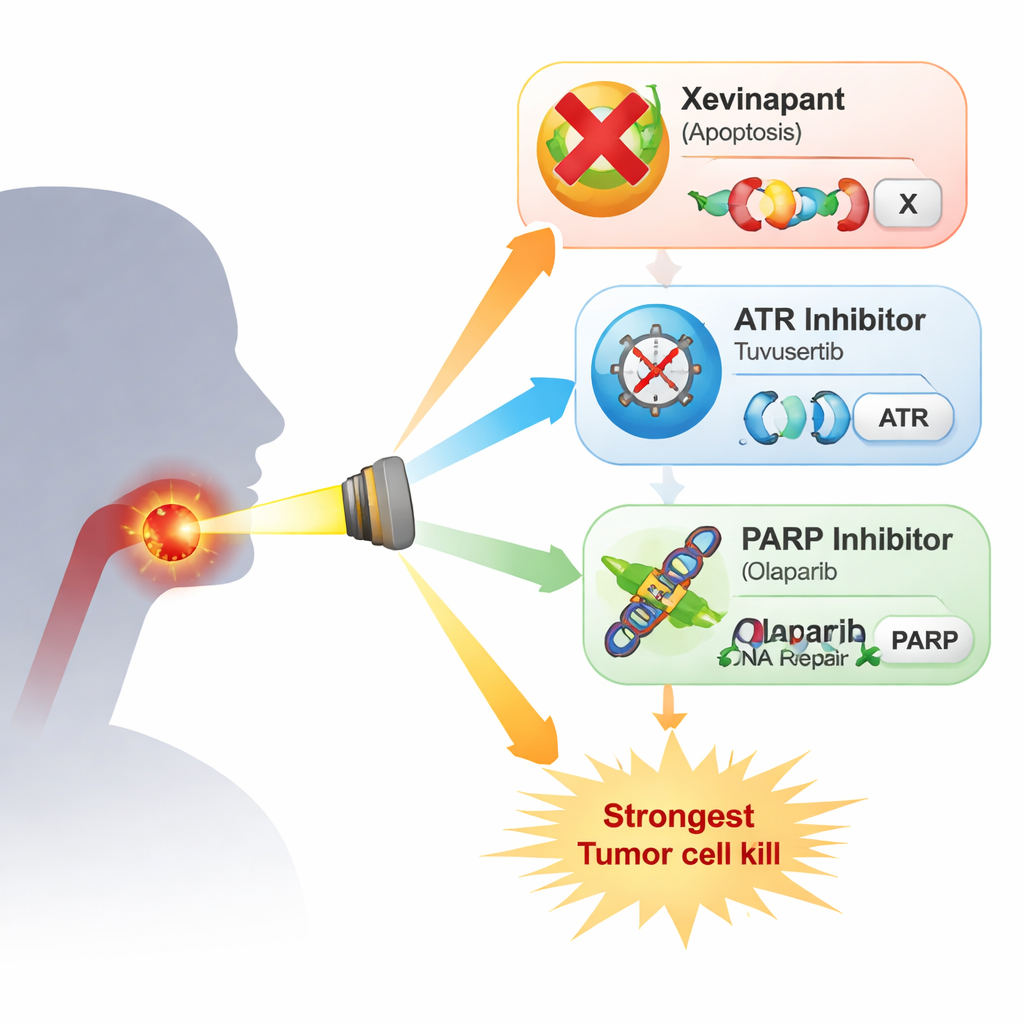
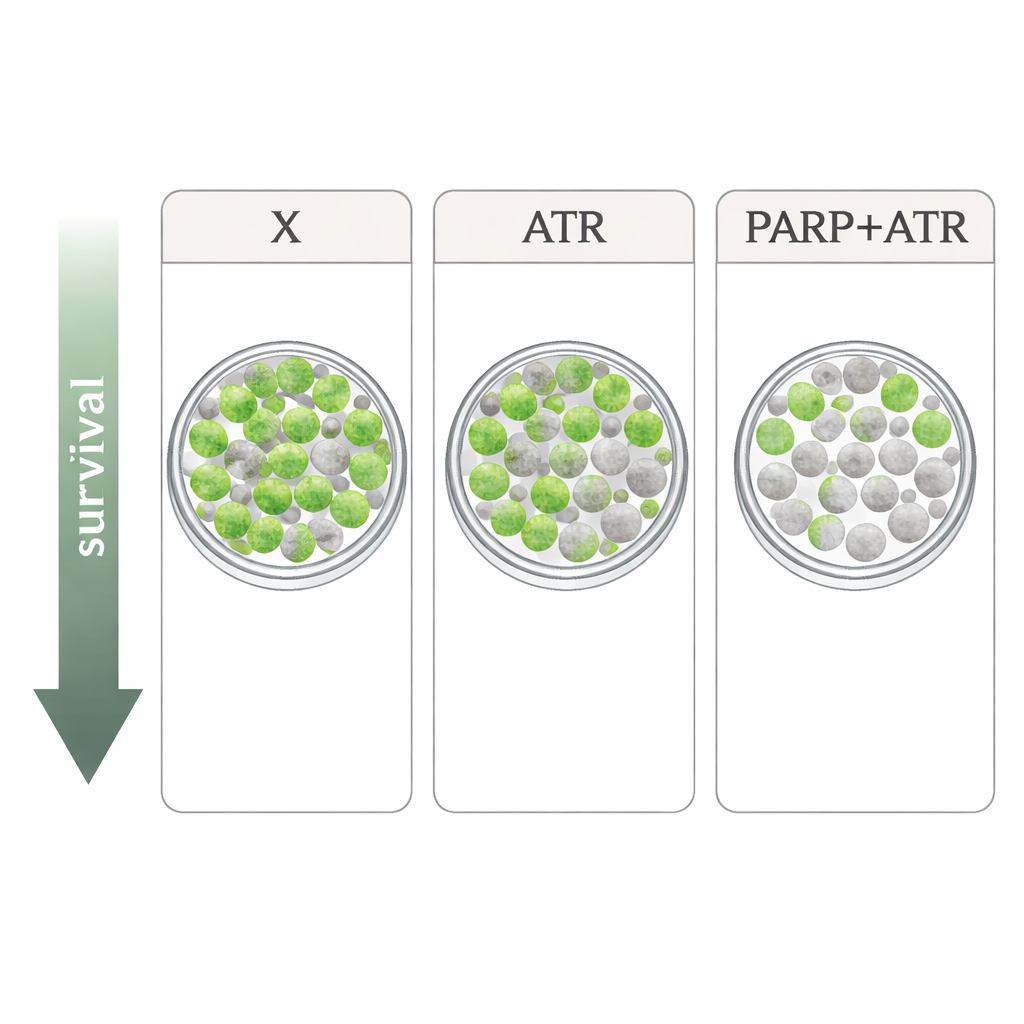
Forskarna studerade fyra strålningsresistenta HPV‑negativa huvud‑ och halscancercellinjer. De jämförde xevinapant med två läkemedel som riktar sig mot cellens respons på DNA‑skador: ATR‑hämmaren tuvusertib och PARP‑hämmaren olaparib, båda använda i doser som liknar de som kan uppnås hos patienter. ATR och PARP är nyckelspelare som hjälper celler att pausa cellcykeln och reparera DNA efter skador som orsakas av röntgenstrålar. I enkla tillväxttester saktade varje läkemedel ner cellproliferationen endast måttligt, och mönstren varierade mellan cellinjer. När de kombinerades med strålning i det mest krävande testet — där man räknar hur många enskilda celler som fortfarande kan växa till kolonier — blev bilden tydligare: xevinapant gav endast mild eller ingen extra strålningspåverkan i flera linjer, medan både tuvusertib och olaparib konsekvent gjorde strålningen mer dödlig. Starkast effekt sågs vid kombination av ATR‑ och PARP‑hämning, vilket gav särskilt stora minskningar i kolonisöverlevnad i tre av de fyra cellinjerna.
Signalsubstanser för celldöd förklarar inte allt
Eftersom xevinapant är utformat för att utlösa celldöd mätte teamet också hur många celler som blev apoptotiska eller lyserade efter behandling, med och utan strålning. Dessa dödmarkörer ökade märkbart i vissa sammanhang — särskilt i en cellinje kallad HSC4 och när läkemedlen kombinerades — men korrelerade inte tillförlitligt med hur väl strålningen faktiskt undertryckte långsiktig överlevnad. Med andra ord var de kortsiktiga dödsutfallen dåliga prediktorer för verklig radiosensibilisering. Denna mismatch betonarför en viktig lärdom för läkemedelsutveckling: endast analyser som följer cellerna tillräckligt länge för att se om de kan återväxa — såsom koloni‑bildningstester — kan korrekt bedöma om en radiosensibilisator är effektiv.
Vad detta betyder för framtida behandlingar
Utifrån dessa laboratorieförsök har xevinapant en viss förmåga att förstärka strålning i HPV‑negativa huvud‑ och halscancerceller, men dess effekt var svagare och mindre konsekvent än strategier som direkt stör hanteringen av DNA‑skador via ATR och PARP. Att kombinera ATR‑ och PARP‑hämmare gav den mest kraftfulla effekten, vilket tyder på att noggrant doserade kombinationer av dessa läkemedel med strålterapi kan erbjuda en mer lovande väg än att fortsätta satsa på xevinapant, åtminstone för denna tumörtyp. Att översätta dessa fynd till kliniken blir inte enkelt, eftersom sådana läkemedel också kan belasta normala, snabbt delande vävnader och redan krävt dosreduktioner i tidiga studier. Ändå pekar arbetet kliniker och forskare mot DNA‑reparationsinriktade strategier som mer övertygande kandidater för att göra strålbehandling både mer effektiv och, potentiellt, säkrare för patienter som inte kan få standardkemoterapi.
Citering: Roehrle, J., Perugachi-Heinsohn, A., Gatzemeier, F. et al. Comparing and combining xevinapant with ATR and PARP inhibition for the radiosensitization of HPV-negative HNSCC cells. Sci Rep 16, 5882 (2026). https://doi.org/10.1038/s41598-026-38550-3
Nyckelord: huvud‑ och halscancer, strålbehandling, hämmare av DNA‑reparation, xevinapant, radiosensibilisering