Clear Sky Science · sv
Målinriktad HDAC8-hämning med icke-hydroxamathaltiga [1,2,4]triazolo[4,3-a]quinolin-föreningar
Ny hoppfullhet för en barndomscancer
Neuroblastom är en aggressiv barndomscancer som uppstår från nervceller och ofta är svår att behandla när den har spridit sig. Denna studie undersöker ett nytt sätt att bromsa eller döda neuroblastomceller genom att stänga av en viktig cellulär brytare kallad HDAC8. Genom att bygga en ny familj av läkemedelslika molekyler som verkar mycket selektivt mot denna brytare vill forskarna skapa behandlingar som både är mer effektiva mot tumörer och skonsammare mot resten av kroppen.
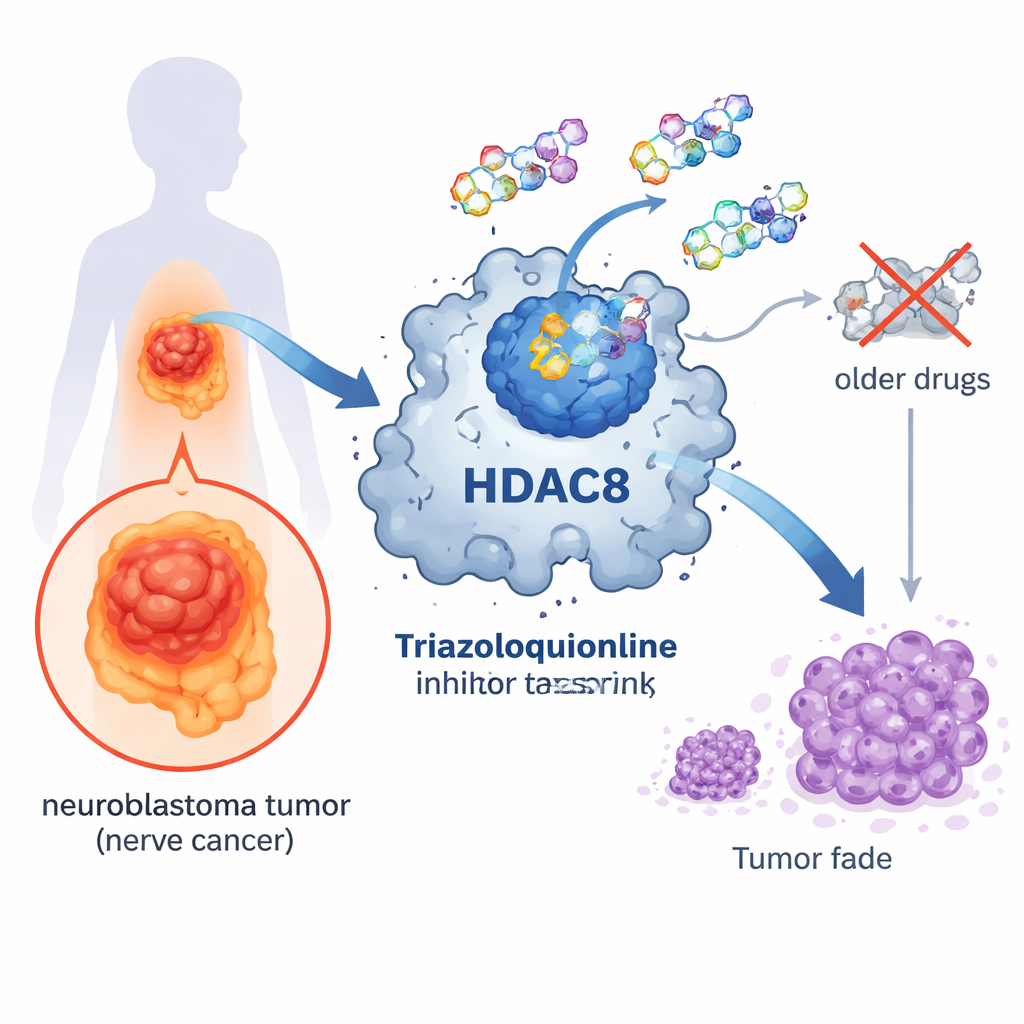
En molekylär brytare i cancerns mitt
Inuti våra celler slås gener ständigt på och av. Ett viktigt kontrollsystem förlitar sig på små kemiska taggar kallade acetylgrupper som fäster vid proteiner associerade med DNA. Enzymer kallade histondeacetylaser (HDAC:er) tar bort dessa taggar, vilket tätar DNA-paketeringen och vanligtvis sänker genaktiviteten. HDAC8 är en medlem av denna enzymfamilj och har kopplats till flera cancerformer, inklusive neuroblastom. När HDAC8 är överaktivt kan cancerceller växa, överleva och sprida sig lättare, vilket gör det till ett attraktivt mål för nya läkemedel.
Begränsningar hos äldre HDAC-läkemedel
Flera HDAC-blockerande läkemedel är redan godkända för vissa blodcancerformer, men de tenderar att påverka många HDAC-typer samtidigt. De flesta av dessa läkemedel använder en hydroxamatgrupp för att greppa en metalljon i enzymets aktiva yta. Även om detta är effektivt binder gruppen metaller så starkt att det kan leda till biverkningar och begränsar hur precist läkemedlet kan skilja mellan olika HDAC:er. Som ett resultat kan patienter drabbas av toxicitet och normala celler kan skadas tillsammans med cancerceller. Forskare har därför sökt efter alternativa kemiska utformningar som behåller de cancerbekämpande fördelarna samtidigt som oönskad skada minskas.
Design av en ny klass riktade hämmare
I detta arbete designade och syntetiserade teamet 21 nya föreningar byggda kring ett triazoloquinolin-skelett, kopplat via en flexibel länk till en "+alpha-amino amide"-region som kan binda zinkatomen i HDAC8:s aktiva yta. Med datorstyrd design valde de denna arkitektur för att passa in i en smal “acetat-releasekanal” unik för HDAC8, en strukturell egenskap som hjälper till att uppnå hög specificitet. Detaljerade dockningsstudier och molekyldynamiksimuleringar visade att flera av de nya molekylerna—särskilt de kallade 9m och 9r—bildar stabila, långvariga interaktioner inne i HDAC8-fickan och binder lika hårt som, eller hårdare än, en välkänd referenshämmare. Viktigt är att biokemiska tester bekräftade att de bästa föreningarna starkt blockerar HDAC8 samtidigt som andra HDAC-familjemedlemmar i stort sett lämnas orörda.
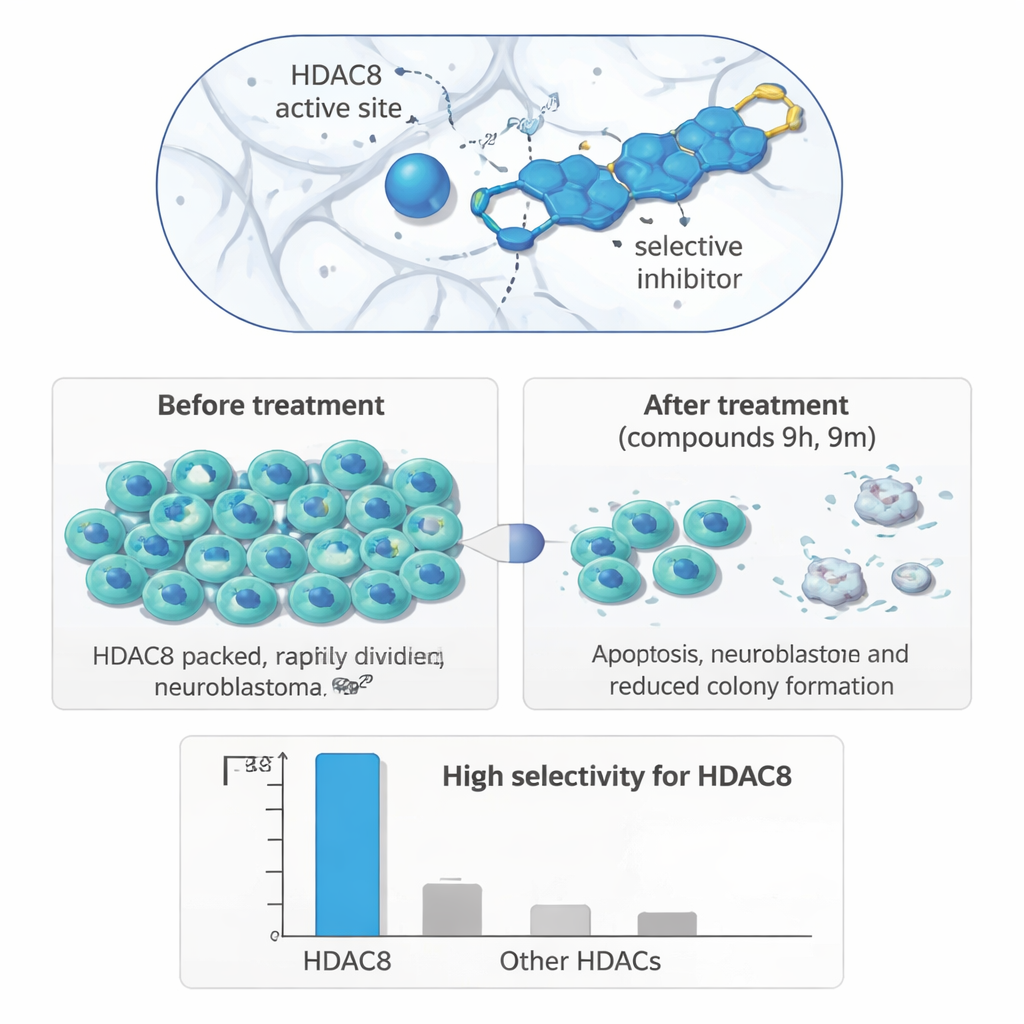
Från provrör till tumörceller
För att se om denna precisa enzymmålning översätts till användbara biologiska effekter testade forskarna sina föreningar på en panel av humana cellinjer. I neuroblastomceller (IMR‑32) utmärkte sig två molekyler, 9h och 9m: de minskade celltillväxten vid mikromolarkoncentrationer och gjorde det tydligare i neuroblastom än i bröst- eller tjocktarmsceller, eller i icke-cancerösa njurceller. Långsiktiga kolonioblastningsförsök visade att behandlade neuroblastomceller förlorade mycket av sin förmåga att återväxa efter läkemedelsexponering. I ett sår-läkningsassay, som följer hur snabbt celler förflyttar sig för att stänga en repa i ett cellager, saktade båda föreningarna ner neuroblastomcellernas rörelse, vilket antyder minskad metastatisk potential.
Undersökning av hur föreningarna dödar cancerceller
Flowcytometri-experiment visade att 9h och 9m utlöser programmerad celldöd (apoptos) i neuroblastomceller och orsakar en ansamling av celler i en fas av cellcykeln som förknippas med DNA-skada eller död (Sub‑G1). För att bekräfta att dessa effekter verkligen härrör från HDAC8-blockad mätte teamet acetylationsnivån av ett protein kallat SMC3, ett känt HDAC8-mål involverat i att hålla systerkromosomer samman under celldelning. När HDAC8 hämmas, byggs acetylerat SMC3 upp. Efter behandling med 9h eller 9m steg nivåerna av acetylerat SMC3 kraftigt, medan total mängd SMC3-protein förblev oförändrad—stark bevisning för att dessa föreningar direkt träffar HDAC8 i levande celler och stör dess normala funktion i kromosomkontroll.
Vad detta kan innebära för framtida behandlingar
Tillsammans målar kemin, datormodelleringen, enzymtesten och cellbaserade experiment en konsekvent bild: de nyligen utvecklade triazoloquinolin-föreningarna är potenta, mycket selektiva hämmare av HDAC8 som kan dämpa tillväxten och spridningen av neuroblastomceller samtidigt som andra HDAC-enzymer skonas. Eftersom de undviker den konventionella hydroxamatgruppen kan de erbjuda en säkrare väg att utnyttja HDAC8 som ett terapeutiskt mål. Även om mycket arbete återstår—särskilt studier i djur och så småningom kliniska prövningar—lägger denna forskning en stabil grund för att utveckla mer precisa läkemedel mot barndomsneuroblastom och möjligen andra HDAC8-drivna sjukdomar.
Citering: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Nyckelord: HDAC8-hämmare, neuroblastom, epigenetisk terapi, triazoloquinolin, riktade cancerläkemedel