Clear Sky Science · sv
GluN2A-medierade strömmar och kalciumsignal i mänskliga iPSC-deriverade neuroner
Varför små labbodlade hjärnceller spelar roll
Forskare vänder sig i allt högre grad till labbodlade mänskliga hjärnceller för att studera hur våra hjärnor utvecklas och för att undersöka vad som går fel vid tillstånd som autism, epilepsi och Alzheimers sjukdom. Denna studie ställer en enkel men avgörande fråga: växer dessa laboratorieframställda neuroner upp och kopplar sig på sätt som verkligen liknar den mänskliga hjärnan, särskilt när det gäller hur de hanterar en nyckelkemisk signal kallad glutamat? Svaret visar hur man bygger mer realistiska ”mini‑hjärnmodeller” och pekar på nya sätt att undersöka hjärnhälsa och sjukdom.
Bygga neuroner från omprogrammerade celler
Forskarna började med mänskliga inducerade pluripotenta stamceller — vanliga celler som ”omprogrammerats” tillbaka till ett stamcellstillstånd. Därifrån styrde de cellerna mot att bli neurala precursorsceller och slutligen nätverk av neuroner och stödjande astrocyter, för att efterlikna den utvecklande mänskliga cortex. De jämförde två vida använda protokoll, eller odlingsförhållanden. Det ena, kallat BrainPhys‑medium, är utformat för att främja aktiva, elektriskt responsiva neuroner och tenderar att ge fler astrocyter. Det andra, ett mer traditionellt neuralt underhållsmedium, gynnar neuroner med färre astrocyter. Under sextio dagar följde teamet hur dessa kulturer förändrades i utseende, genaktivitet och celltyper, och fann att BrainPhys‑odlade kulturer utvecklade mer detaljerade neuronformer och en neuron‑till‑astrocyt‑kvot närmare den i den verkliga mänskliga hjärnan.
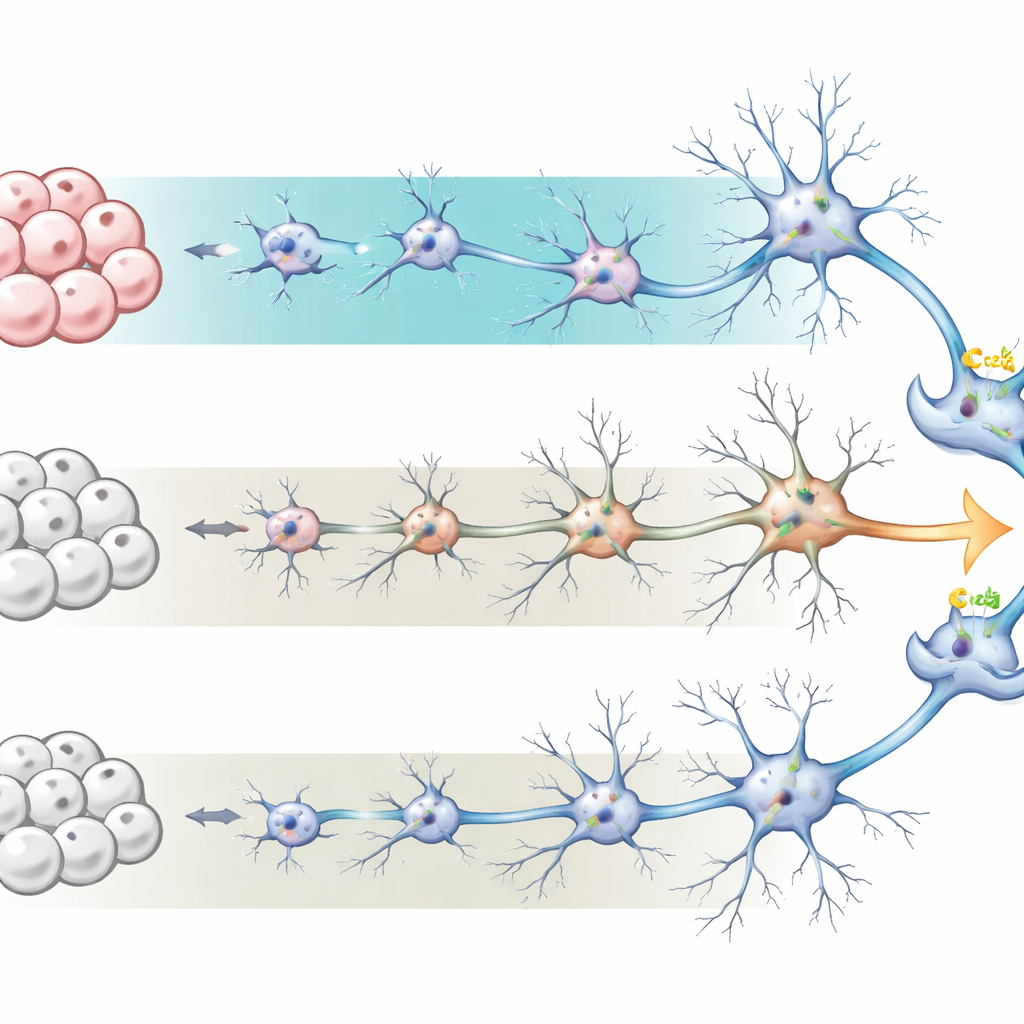
Tecken på att cellerna mognar
För att se hur ”mogna” neuronerna var mätte teamet global genaktivitet med RNA‑sekvensering vid dag 60. Celler odlade i BrainPhys visade nästan två tusen gener med differentierad uttrycksnivå jämfört med standardmediet, många kopplade till neuron‑differentiering, synapsbildning och elektrisk aktivitet. Gener som är förknippade med astrocyt‑funktion och inflammation var också högre, vilket speglar den större astrocytpopulationen. Tillsammans tyder dessa mönster på att BrainPhys‑kulturerna bättre återskapar senare steg i hjärnans utveckling, med mer förfinade kommunikationspunkter mellan neuroner och en stödjande miljö som närmar sig levande vävnad.
Nyckelomkopplare i kemisk kommunikation
Ett kännetecken för hjärnmognad är ett skifte i sammansättningen av NMDA‑receptorer — molekylära portar på neuroner som öppnas som svar på glutamat och hjälper till att etablera inlärningsrelaterade kopplingar. Tidigt i utvecklingen dominerar en subenhet kallad GluN2B; senare tar GluN2A över och ändrar hur länge och hur kraftigt receptorerna förblir öppna. Med mikroskopi visade teamet att över tid flyttade fler NMDA‑receptorer in i synapserna, kontaktpunkterna mellan neuroner, särskilt i BrainPhys‑kulturer. Målinriktade genmätningar avslöjade en nedgång i den ”tidiga” GluN2B‑subenheten och en ökning av den ”senare” GluN2A‑subenheten, vilket indikerar att neuronerna genomgick denna klassiska utvecklingsomkoppling.
Följa strömmar och kalcium inne i cellerna
Funktionella tester bekräftade att dessa molekylära förändringar hade betydelse. Med finspetsade elektroder registrerade forskarna elektriska strömmar utlösta av NMDA, ett ämne som selektivt aktiverar NMDA‑receptorer. Neuroner från båda odlingsmetoderna visade robusta strömmar, men blockering av GluN2A‑subenheten minskade dessa strömmar med ungefär hälften, vilket visar att GluN2A nu var en huvudaktör i signalflödet. Teamet följde sedan kalcium, en viktig intern budbärare, med en fluorescerande färg. När de utsattes för NMDA visade en mycket större andel av BrainPhys‑odlade neuroner starka kalciumtoppar, och signalens storlek var större. Genanalys föreslog varför: BrainPhys‑kulturer uppreglerade flera komponenter i kalciumkanaler och frisättningsvägar, vilket försåg cellerna att översätta NMDA‑receptoraktivering till breda, koordinerade kalciumsignaler.
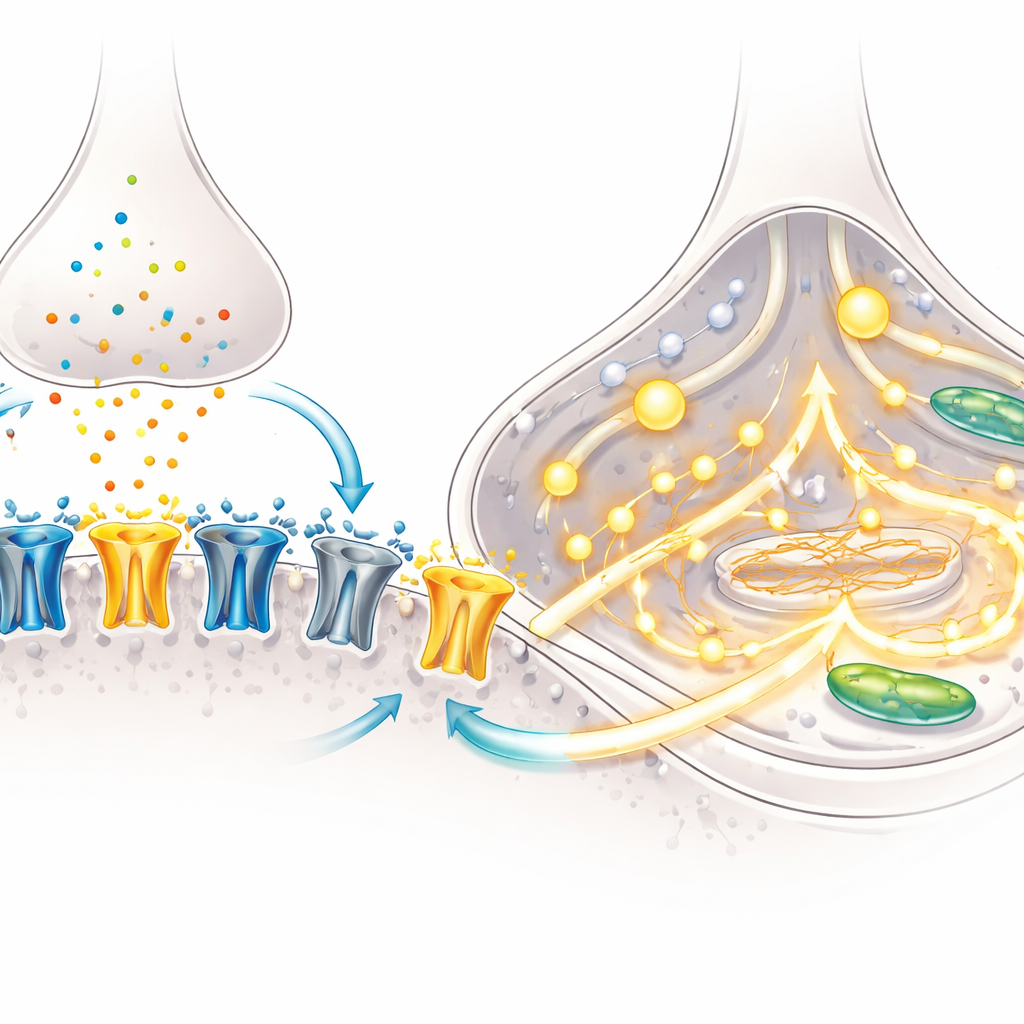
Vad detta betyder för studier av hjärnsjukdomar
Tillsammans visar dessa fynd att mänskliga stamcellsderiverade neuroner kan nå ett funktionellt moget tillstånd på bara två månader, särskilt när de odlas under förhållanden som gynnar aktiva nätverk och en realistisk blandning av neuroner och astrocyter. I detta tillstånd dominerar den ”vuxenliknande” GluN2A‑subenheten NMDA‑receptorströmmar och bidrar starkt till kalciumsignalering, ungefär som i den utvecklande mänskliga hjärnan. För icke‑specialister är slutsatsen att forskare nu har en mer trogen laboratoriemodell för hur humana excitatoriska neuroner mognar, kopplar ihop sig och svarar på glutamat. Det gör det möjligt att undersöka hur subtila genetiska förändringar eller sjukdomsprocesser stör dessa finstämda omkopplingar, vilket öppnar ett fönster mot tillstånd från epilepsi till Alzheimers sjukdom och vägleder design och testning av framtida terapier.
Citering: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
Nyckelord: NMDA-receptorer, stamcellsneuroner, hjärnans utveckling, kalciumsignalering, synaptisk mognad