Clear Sky Science · sv
Dubbla hämningen av G9a och antagonisten till histamin H3‑receptorn A-366 förbättrar repetitiva och sociala beteenden och dämpar neuroinflammation hos BTBR T + tf/J‑möss
Varför denna musstudie är viktig för autism
Familjer som lever med autismspektrumstörning (ASD) möter ofta en blandning av behandlingar som bara lindrar några få symtom åt gången. Denna studie undersöker en ny experimentell förening, kallad A‑366, framtagen för att verka på två mycket olika biologiska system samtidigt. I en ofta använd musmodell för autismliknande beteenden minskade A‑366 repetitiva handlingar, förbättrade social interaktion och dämpade hjärnans inflammation — vilket antyder en framtid där ett enda läkemedel skulle kunna angripa flera kärndrag hos ASD samtidigt.
En störning med många rörliga delar
ASD är inte en enda sjukdom med en enda orsak. Den innefattar svårigheter med social kommunikation, repetitiva beteenden och ofta andra utmaningar som ångest eller uppmärksamhetsproblem. Bakom dessa yttre tecken finns en trasslig väv av förändringar i hjärnans kemi och genreglering. Nuvarande läkemedel, som antipsykotikan aripiprazol, riktar sig främst mot hjärnans signalsystem som dopamin och serotonin och är endast godkända för associerade symtom som irritabilitet. Samtidigt har forskning visat att sättet DNA packas och kemiskt märks inne i hjärnceller — epigenetik — också förändras vid ASD, liksom aktiviteten i hjärnans egna immunsvar och inflammatoriska processer. Dessa flera nivåer tyder på att en "ett-mål-i-taget"‑strategi kan vara för snäv.
Att slå mot både genswitchar och hjärnans budbärare
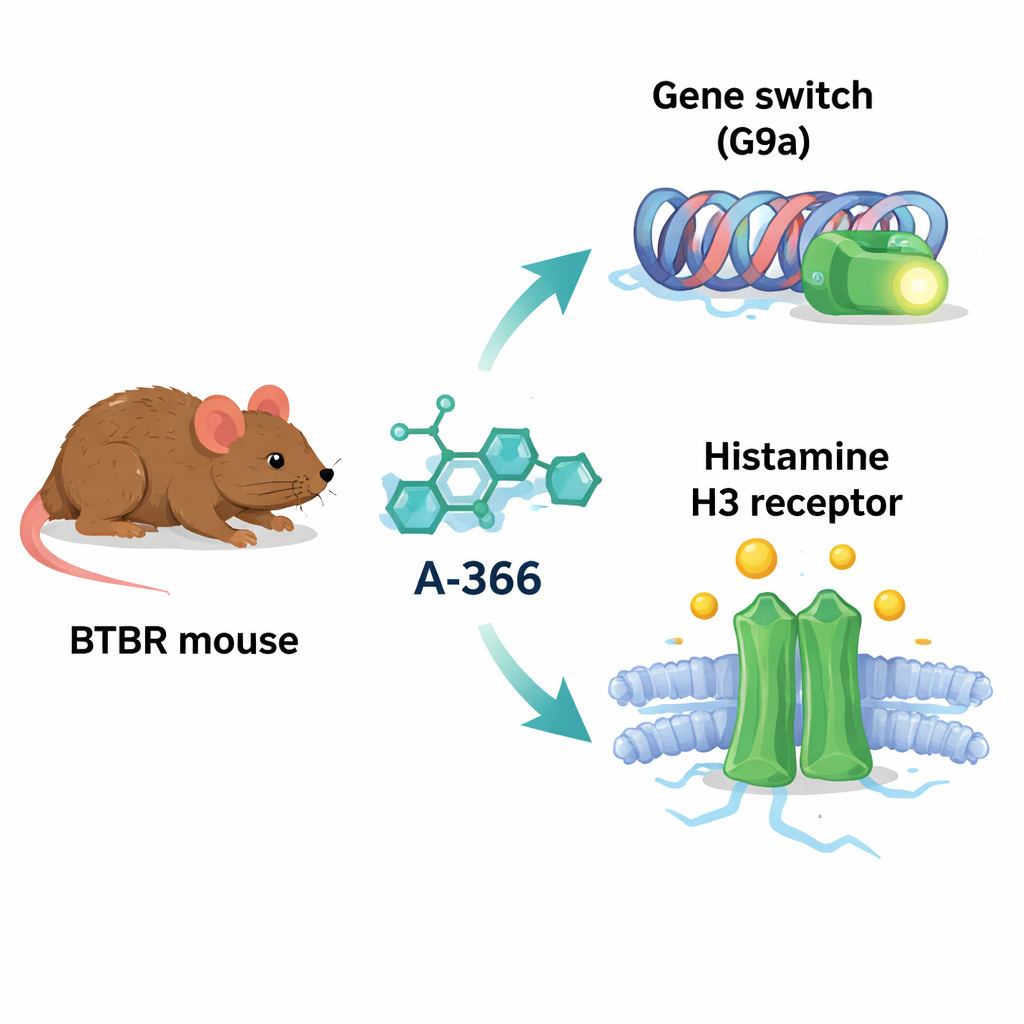
A‑366 utvecklades ursprungligen för att blockera ett protein kallat G9a, ett enzym som sätter kemiska markörer på histonproteiner och tenderar att dämpa genuttryck. I flera hjärnrelaterade störningar är G9a‑aktivitet och dess markeringar förhöjda, vilket potentiellt tystar gener viktiga för inlärning, minne och hälsosam nervkoppling. Intressant nog liknar A‑366:s kemiska form även den hos läkemedel som blockerar histamin H3‑receptorn, en brytare som kontrollerar frisättningen av histamin och andra transmittorer och som kopplats till uppmärksamhet, vakenhet och socialt beteende. På grund av denna överlappning misstänkte författarna att A‑366 kan fungera som en "dubbel agent": lätta upp skadlig genavstängning genom G9a‑inhibering samtidigt som histaminsignalering stärks genom H3‑blockad.
Att testa A‑366 i autistiskt liknande möss
Forskarna arbetade med BTBR T+tf/J‑möss, en stam som naturligt visar låg social förmåga, kraftigt repetitivt putsande och grävande samt förhöjd hjärninflammation — drag som speglar viktiga aspekter av ASD. Hanliga BTBR‑möss fick dagliga injektioner av A‑366 i tre veckor vid tre olika doser, och deras beteende jämfördes med typiska C57‑möss och med BTBR‑möss behandlade med antingen pitolisant (en standard H3‑receptorblockerare) eller aripiprazol. I flera tester minskade A‑366 repetitivt grävande, rivande och självputsning i en dosberoende mönster och förbättrade prestationen i en Y‑labyrint som mäter rumsligt arbetsminne. I ett trekammartest för socialt beteende återställde A‑366 inte bara mössens preferens för att tillbringa tid med en annan mus framför ett tomt burk, utan vid högsta dos lyfte det de sociala poängen till nivåer jämförbara med typiska möss och överträffade effekterna av både pitolisant och aripiprazol.
Dämpning av inflammation och bekräftelse av målen
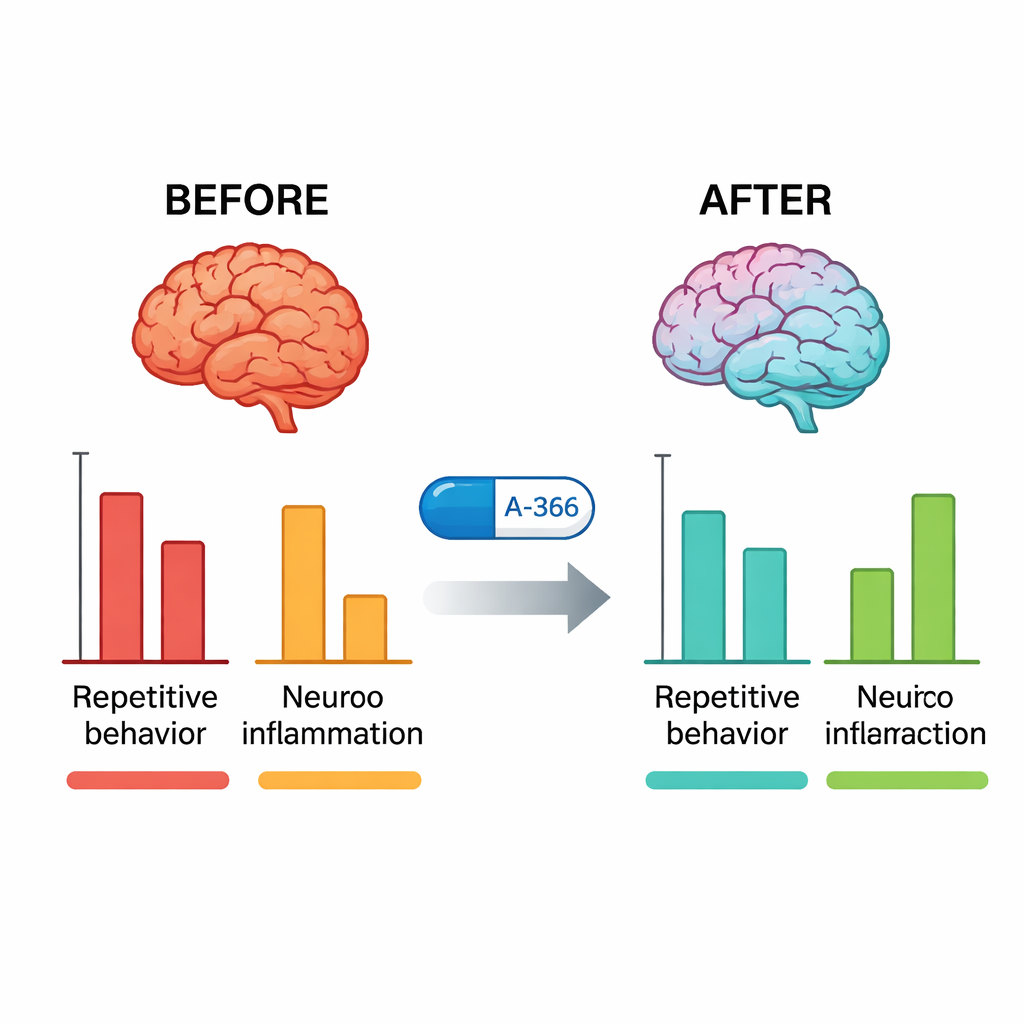
Efter beteendetesterna granskade forskarna mössens hjärnor. I obehandlade BTBR‑möss var G9a‑aktiviteten i hippocampus och cerebellum markant högre än hos typiska möss. Behandling med A‑366 minskade denna aktivitet kraftigt tillbaka mot normala nivåer, medan pitolisant ensam inte gjorde det, vilket bekräftar att A‑366 verkligen träffar sitt epigenetiska mål. Samtidigt var nyckelinflammatoriska molekyler — TNF‑α, IL‑6 och IL‑1β — kraftigt förhöjda i BTBR‑möss och sänktes signifikant av A‑366, mer än av aripiprazol. När forskarna gav ett läkemedel som aktiverar H3‑receptorer (RAMH) ovanpå A‑366, återställdes de beteendemässiga och antiinflammatoriska fördelarna bara delvis, och fallet i G9a‑aktivitet bestod. Detta mönster stödjer en kombinerad mekanism: stabil epigenetisk lindring genom G9a‑inhibering plus ett histaminmedierat bidrag via H3‑receptorblockad.
Vad detta kan innebära för framtida behandlingar
För en icke‑specialist tyder dessa fynd på att det kan vara möjligt att utforma läkemedel som verkar på både hjärnans "mjukvara" och dess "budbärarsystem" samtidigt. I denna musmodell för autismliknande beteende lindrade A‑366 repetitiva handlingar, förbättrade socialt engagemang och minskade tecken på kronisk hjärninflammation genom att samtidigt luckra upp skadliga gen‑nedstängningar och justera histaminsignalering. A‑366 i sig byggdes för andra sjukdomar och skulle behöva optimeras och genomgå omfattande säkerhetstester innan någon användning hos människor. Ändå erbjuder det en ritning för en ny klass av multimålsläkemedel riktade mot ASDs komplexa biologi, där att adresssera endast en väg i taget hittills gett begränsad lindring.
Citering: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Nyckelord: autismspektrumstörning, epigenetisk terapi, histamin H3‑receptor, neuroinflammation, musmodell