Clear Sky Science · sv
aFGF räddar fibroblaster som blivit senescent av högt glukos och förbättrar diabetisk sårheling genom att reglera SIRT1/STAT3‑vägen
Varför långsamt läkande sår är viktiga
För många personer med diabetes kan ett litet skrapsår på foten eller benet utvecklas till ett seglivat sår som blir kvar i månader, ibland leder till infektion eller till och med amputation. Dessa kroniska sår är inte bara ett ytligt problem: hudcellerna som ska bygga upp den skadade vävnaden blir ofta åldrade i förtid och slutar fungera korrekt. Denna studie undersöker ett lovande tillvägagångssätt för att ”föryngra” vissa av dessa celler med hjälp av en naturligt förekommande reparationssignal, med målet att få diabetiska sår att sluta sig snabbare och mer fullständigt.
Celler som åldras för tidigt
Frisk hud är beroende av fibroblaster—stödjeceller som finns i hudens djupare lager—som ska dela sig, röra sig in i ett sår och lägga ner ny stomme för vävnadsbildning. Vid diabetes driver långvarigt förhöjt blodsocker och sockerskadade molekyler dessa fibroblaster in i ett tillstånd kallat cellulär senescens. Senescenta fibroblaster delar sig inte längre bra, producerar mindre av de strukturella proteiner som behövs för reparation och frisätter istället en cocktail av irritationfrämjande faktorer som underhåller inflammation. Författarna visar att hud runt ett sår hos diabetiska råttor innehåller fler av dessa åldrade fibroblaster och mindre av de hjälpsamma matrixproteinerna, vilket korrelerar med betydligt långsammare läkning.
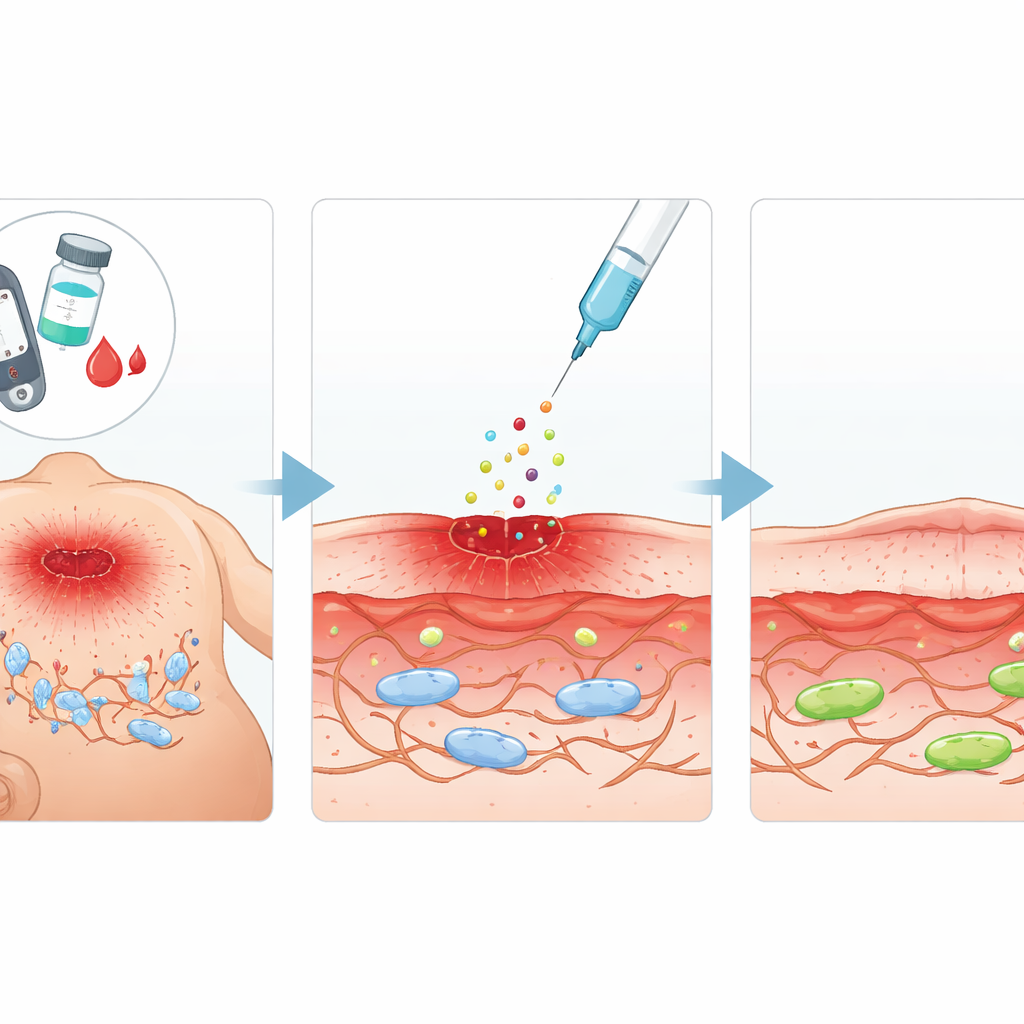
En reparationssignal med potential
Forskargruppen fokuserade på sur fibroblasttillväxtfaktor (aFGF), ett naturligt förekommande protein känt för att stimulera celltillväxt och vävnadsreparation. De undrade om aFGF inte bara kunde öka fibroblastaktivitet utan också vända åldringsliknande förändringar orsakade av högt socker. Hos diabetiska råttor skapade de standardiserade hudsår och injicerade aFGF runt det skadade området varannan till var tredje dag. Jämfört med obehandlade diabetiska djur visade aFGF‑behandlade råttor snabbare minskning av sårytan, bättre återuppbyggnad av underliggande vävnad och lägre nivåer av markörer som signalerar cellulär senescens. I parallella laboratorieexperiment med en musfibroblastcellinje exponerad för mycket högt glukos återställde aFGF cellernas förmåga att dela sig och migrera—två beteenden som är avgörande för att sluta ett sår.
Lugnar oxidativ stress inne i cellerna
Högt blodsocker gör mer än att bara lägga extra bränsle på cellerna: det driver också överproduktion av reaktiva syrearter, instabila molekyler som skadar proteiner, fetter och DNA. Denna oxidativa stress är en huvudorsak till att fibroblaster blir senescenta. Forskarna mätte flera standardindikatorer för denna stress i sin cellmodell, inklusive skadliga nedbrytningsprodukter och aktiviteten hos cellens egna antioxidantenzym. Vid högt glukos visade fibroblaster mer skada och svagare antioxidantförsvar. När aFGF tillsattes skiftade balansen: skadliga markörer minskade och skyddande enzymer blev mer aktiva. Detta tyder på att aFGF hjälper till att återställa en friskare intern miljö, vilket minskar sannolikheten att fibroblaster går över i ett permanent åldrat tillstånd.
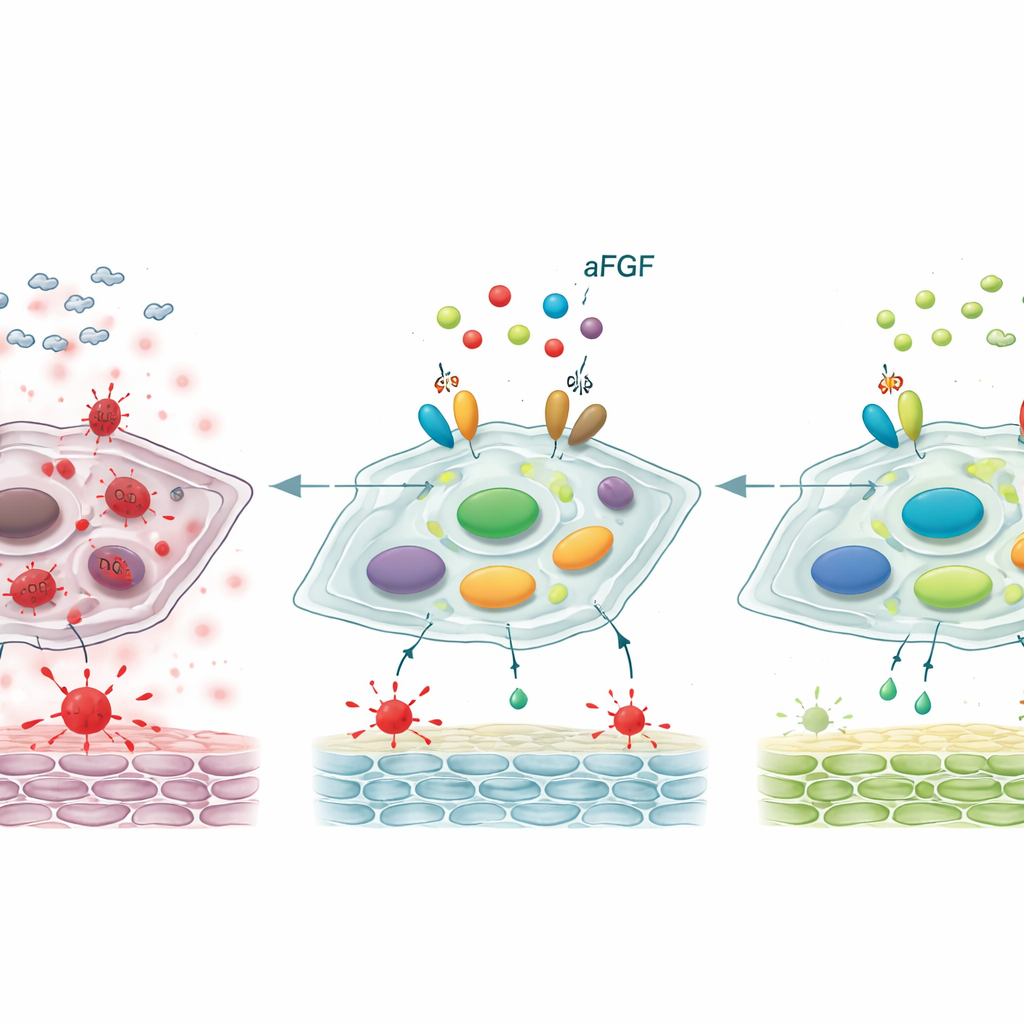
Återställer en viktig kontrollbrytare
Genom att gå djupare undersökte forskarna en molekylär kontrollaxel som involverar två proteiner, SIRT1 och STAT3, som tillsammans påverkar om fibroblaster förblir ungdomliga eller blir senescenta. I diabetiska sår och i celler behandlade med högt glukos var nivåerna av SIRT1, en beskyddare kopplad till stressmotstånd, reducerade, medan den aktiverade formen av STAT3—en drivare av åldrande och inflammatoriskt beteende—var ökad. Behandling med aFGF vände detta mönster: SIRT1 ökade och aktiverad STAT3 minskade. När teamet blockerade SIRT1 med en specifik hämmare förlorade aFGF till stor del sin förmåga att minska oxidativ stress, dämpa åldersmarkörer och påskynda sårslutning hos råttor. Det här indikerar att aFGF:s gynnsamma effekter i hög grad beror på att återaktivera SIRT1, som i sin tur håller STAT3 och det skadliga åldringsprogram det styr under kontroll.
Vad detta kan innebära för patienter
Sammantaget tyder fynden på att aFGF gör mer än att bara driva celltillväxt. Det verkar rädda överarbetade fibroblaster i diabetiska sår från en destruktiv åldringscykel, lindra oxidativ stress och återställa en viktig molekylär brytare så att dessa celler återigen kan hjälpa till att bygga upp vävnad. Även om arbetet utförts i råttor och odlade celler, och verkliga diabetiska sår är ännu mer komplexa än de modeller som användes här, pekar resultaten mot aFGF som en lovande kandidat för framtida behandlingar. Om liknande fördelar bekräftas hos människor kan noggrant riktad aFGF‑terapi en dag hjälpa kroniska diabetiska bensår att läka snabbare, minska smärta, infektionsrisk och risken för allvarliga komplikationer.
Citering: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Nyckelord: diabetisk sårheling, fibroblaståldrande, oxidativ stress, tillväxtfaktorbehandling, SIRT1 STAT3‑vägen