Clear Sky Science · sv
CNOT2 /c-Myc/STAT3-signalering är kritiskt involverad i glykosmedierad apoptos av bensylisotiocyanat i hepatocellulärt karcinom
En cancerbekämpande ingrediens på din tallrik
Bensylisotiocyanat, eller BITC i korthet, är en naturlig förening som finns i vanliga grönsaker som broccoli, kål och grönkål. Långt tillbaka har läkare noterat att personer som äter mer av dessa grönsaker ofta har lägre cancerförekomst, men hur specifika växtämnen bromsar eller dödar cancerceller håller man fortfarande på att reda ut. Denna studie undersöker hur BITC påverkar levercancerceller i laboratoriet och avslöjar en överraskande koppling mellan hur cancerceller förbränner socker och hur de skjuts in i självdestruktion.
Varför levercancer behöver bättre behandlingsalternativ
Levercancer är en av de dödligaste cancerformerna globalt, och hepatocellulärt karcinom är dess vanligaste form. Även med kirurgi, kemoterapi och riktade läkemedel återkommer många tumörer eller slutar svara på behandlingen. En orsak är att cancerceller omkopplar hur de använder energi: istället för att i första hand förlita sig på syre i sina mitokondrier förbränner de stora mängder socker mycket snabbt i en process som ofta kallas ”Warburg-effekten”. Denna förvridna sockeranvändning hjälper cancerceller att växa snabbare och motstå celldöd. Att hitta säkra sätt att störa denna energiförsörjning, särskilt med molekyler härledda från mat, är en lockande strategi.
Test av ett grönsaksämne på levercancerceller
Forskarna behandlade två humana levercancercellinjer, SK-Hep1 och Huh7, med ökande doser av BITC. När dosen ökade överlevde färre celler, vilket visar att BITC är toxiskt för levercancerceller under dessa villkor. När de granskade vad som skedde inne i cellerna såg de klassiska kännetecken för programmerad celldöd, eller apoptos. Nyckelproteiner som normalt förekommer i en ”inaktiv” form innan de klyvs under apoptos, såsom PARP och caspas-3, minskade i sina intakta, eller ”pro-”, former. Flödescytometritester visade också fler celler i sub-G1-fraktionen av cellcykeln och fler celler som var positiva för Annexin V — båda tecken på att cancercellerna aktivt genomgick apoptos snarare än bara blev skadade.
Stänga ner tumörers sockerbegär
Teamet undersökte därefter om BITC påverkade Warburg-effekten. De mätte proteiner som hjälper cancerceller att snabbt ta upp socker och omvandla det till energi och laktat — specifikt HK2, PKM2 och LDH. BITC-behandling sänkte nivåerna av alla tre i båda levercancercellinjerna och minskade hur mycket laktat cellerna släppte ut och hur mycket glukos de förbrukade från odlingsmediet. Med andra ord gjorde BITC levercancerceller mindre kapabla att driva sin högfrekventa sockerverksamhet. När forskarna tillsatte pyruvat, en nedströmsprodukt av sockernedbrytning som fortfarande kan mata cellmetabolismen, vändes många av BITC:s effekter: cellerna återfick högre nivåer av PARP, caspas-3 och glykolysenzymen. Denna räddning antydde att störning av sockerprocessningen är en nyckeldel i hur BITC utlöser celldöd.
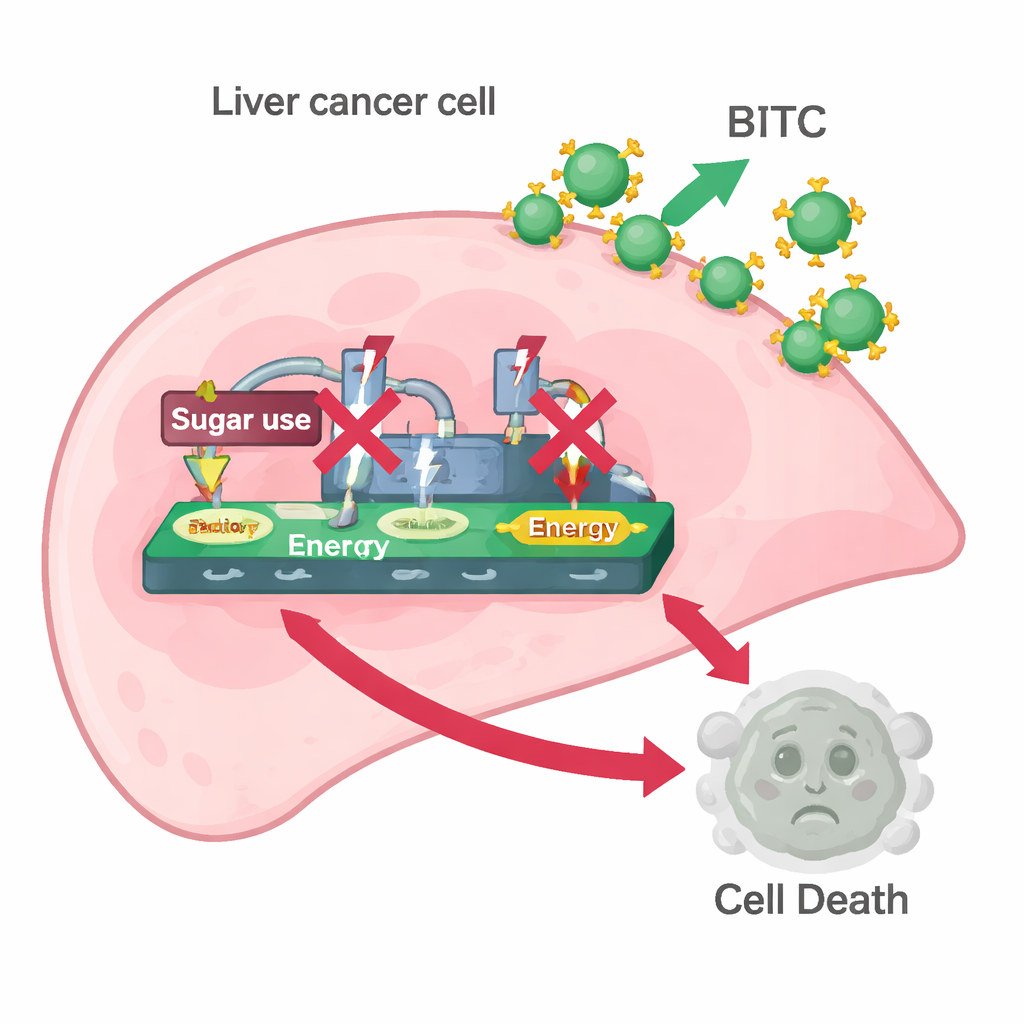
Att reda ut kontrollbrytare inne i cellen
För att förstå djupare kontrollskikt fokuserade forskarna på en signaltrio: CNOT2, c-Myc och STAT3. Dessa proteiner bidrar till tillväxt, överlevnad och metabol omstälning i många tumörer. Data från levercancerpatienter visade att CNOT2 tenderar att vara högre hos personer med sämre prognos. I laboratoriet sänkte BITC behandling den aktiva, fosforylerade formen av STAT3, dess uppströmsaktivator JAK1, det tillväxtfrämjande proteinet c-Myc och CNOT2 självt. Genetiska verktyg för att minska CNOT2- eller STAT3-nivåer gjorde BITC:s dödande effekt ännu starkare och sänkte ytterligare PARP och caspas-3. Proteinbindningsexperiment visade att BITC också störde de fysiska partnerskapen mellan CNOT2 och STAT3 och mellan CNOT2 och c-Myc. När CNOT2 eller c-Myc konstgjort höjdes förlorade BITC mycket av sin förmåga att stänga ner glykolysenzym och utlösa apoptos, vilket understryker att denna signalaxel fungerar som en huvudbrytare som kopplar samman sockermetabolism och överlevnad.
Vad detta kan innebära för framtida terapier
Tillsammans målar fynden upp en sammanhängande bild: BITC attackerar levercancerceller genom att kapa deras föredragna sockerbaserade bränslelina och slå om celldödsswitchar som beror på CNOT2/c-Myc/STAT3-axeln. Genom att blockera både tillväxtsignaler och sockeranvändning pressar BITC cancerceller förbi en metabolisk brytpunkt in i apoptos. Dessa resultat kommer från cellodlingsexperiment, inte patienter, och endast två typer av levercancerceller studerades, så mycket mer arbete i djur och människor krävs. Ändå stärker forskningen idén att vissa föreningar från vardagliga grönsaker skulle kunna förfinas eller kombineras med andra behandlingar för att mer precist svälta ut levertumörer samtidigt som de uppmuntrar dem att självdö.
Citering: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
Nyckelord: levercancer, bensylisotiocyanat, cancermetabolism, apoptos, kruciferväxter