Clear Sky Science · sv
Prognostisk modell baserad på maskininlärning för stamhets- och angiogenesrelaterade gener för att förutsäga prognos och immuninfiltration hos patienter med HCC
Varför denna forskning är viktig för levercancerpatienter
Hepatocellulärt carcinom, den vanligaste formen av levercancer, återkommer ofta eller sprider sig även efter behandling. Denna studie undersöker varför det sker och hur kliniker bättre kan förutsäga vilka patienter som löper störst risk. Genom att kombinera stora genetiska databaser med modern maskininlärning byggde forskarna ett verktyg som kopplar två centrala canceregenskaper — "stamhetsfaktor" (celler som beter sig som envisa frön) och ny blodkärlsbildning — till patienters överlevnadschanser och sannolikhet att svara på immunbaserade behandlingar.
Cancerens “fröceller” och nya blodkärl
Många tumörer innehåller en liten grupp celler som fungerar som frön. Dessa cancerstamceller kan förnya sig själva, motstå behandling och återstarta tumören efter operation eller cytostatika. Samtidigt behöver tumörer bygga nya blodkärl för att få syre och näring så att de kan växa och sprida sig. Nyare forskning visar att dessa två processer hänger ihop: stamliknande cancerceller avger signaler som främjar blodkärlsbildning, medan en kärlrik miljö hjälper dessa fröceller att överleva. Att förstå och gemensamt rikta in sig på detta samspel är särskilt viktigt vid levercancer, som både är mycket vaskulär och benägen att återkomma.
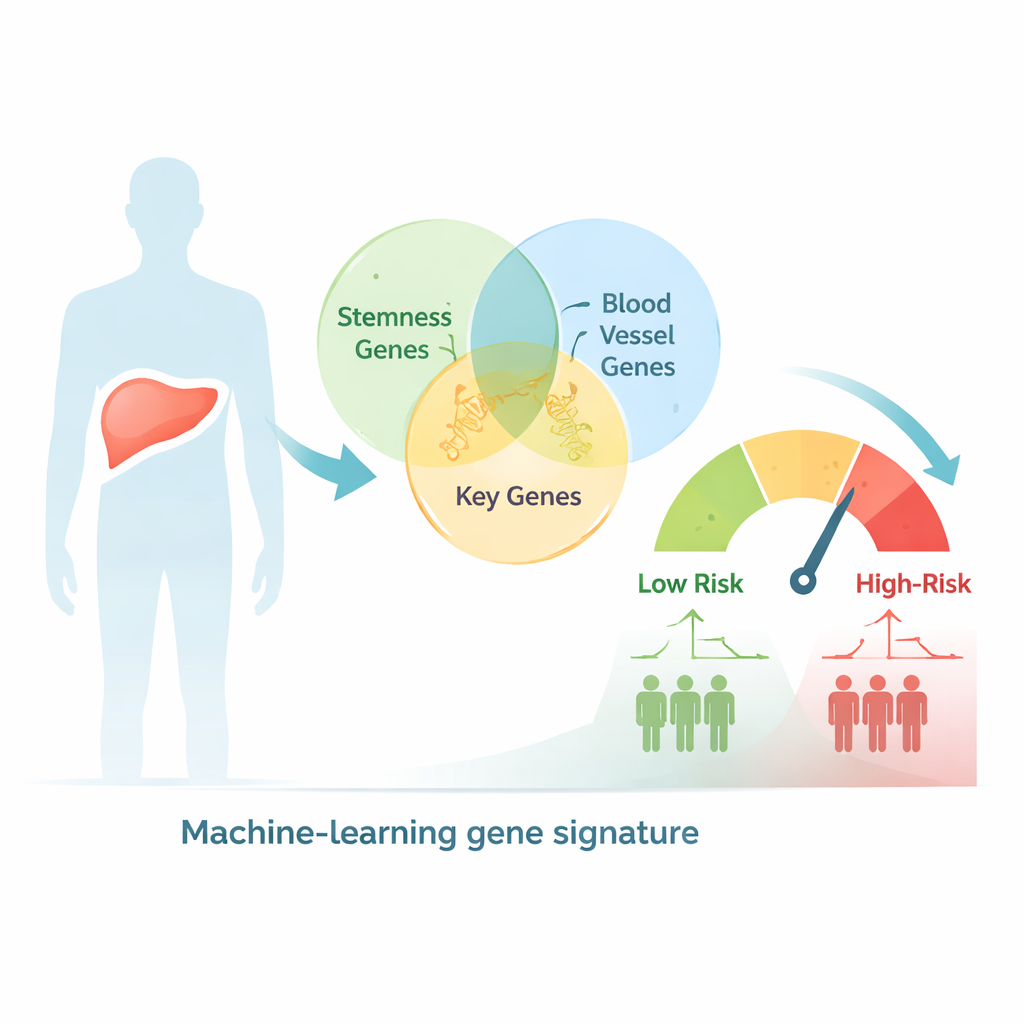
Användning av stordata för att sortera patienter efter risk
Forskarna började med att söka i en stor mänsklig gendatabas efter gener kopplade både till stamliknande beteende och till blodkärlsbildning, och landade i mer än 2 600 överlappande kandidater. De granskade sedan levercancerprover från hundratals patienter vars tumörers genaktivitet och kliniska utfall fanns registrerade i offentliga cancerarkiv. Med statistiska tester och klustringsmetoder grupperade de patienterna i två genetiska undergrupper som visade tydliga skillnader i stadium, tumörstorlek och överlevnad, vilket tyder på att kombinerade stamhets- och kärlrelaterade signaler fångar meningsfull biologi i denna sjukdom.
Uppbyggnad av en riskpoäng baserad på nio gener
Ur denna stora genpool använde teamet en maskininlärningsmetod för att reducera antalet till endast nio nyckelgener vars kombinerade aktivitet bäst förutsade hur länge patienterna levde. Dessa nio gener användes för att beräkna en riskpoäng för varje person. Patienter med tumörer som hade hög poäng hade signifikant kortare totalöverlevnad, både i den ursprungliga datamängden och i en oberoende uppsättning levercancerpatienter som användes för validering. Modellens noggrannhet var konkurrenskraftig med — eller bättre än — många befintliga verktyg, och när poängen kombinerades med enkel klinisk information såsom tumörstadi i en nomogram ökade förutsägelsen av 1-, 3- och 5-årsöverlevnad ytterligare.
Kopplingar till immunsystemet och behandlingssvar
Teamet undersökte också vad niogenspoängen avslöjade om tumörens immiljö. Låg-risktumörer tenderade att vara mer "inflammerade", med högre nivåer av olika immunceller och starkare signaler från angreppsvägar. Hög-risktumörer visade däremot mönster som stämde överens med immunundvikande och högre mutationsfrekvenser i viktiga gener som TP53. Med etablerade datorverktyg som uppskattar hur tumörer kan svara på moderna immunterapier antydde studien att låg-riskpatienter kan svara bättre på immune checkpoint‑hämmare än hög-riskpatienter. Dessa prognoser behöver fortfarande prövas i verkliga behandlingsmiljöer, men pekar mot ett praktiskt sätt att identifiera patienter som kan ha störst nytta av sådana läkemedel.
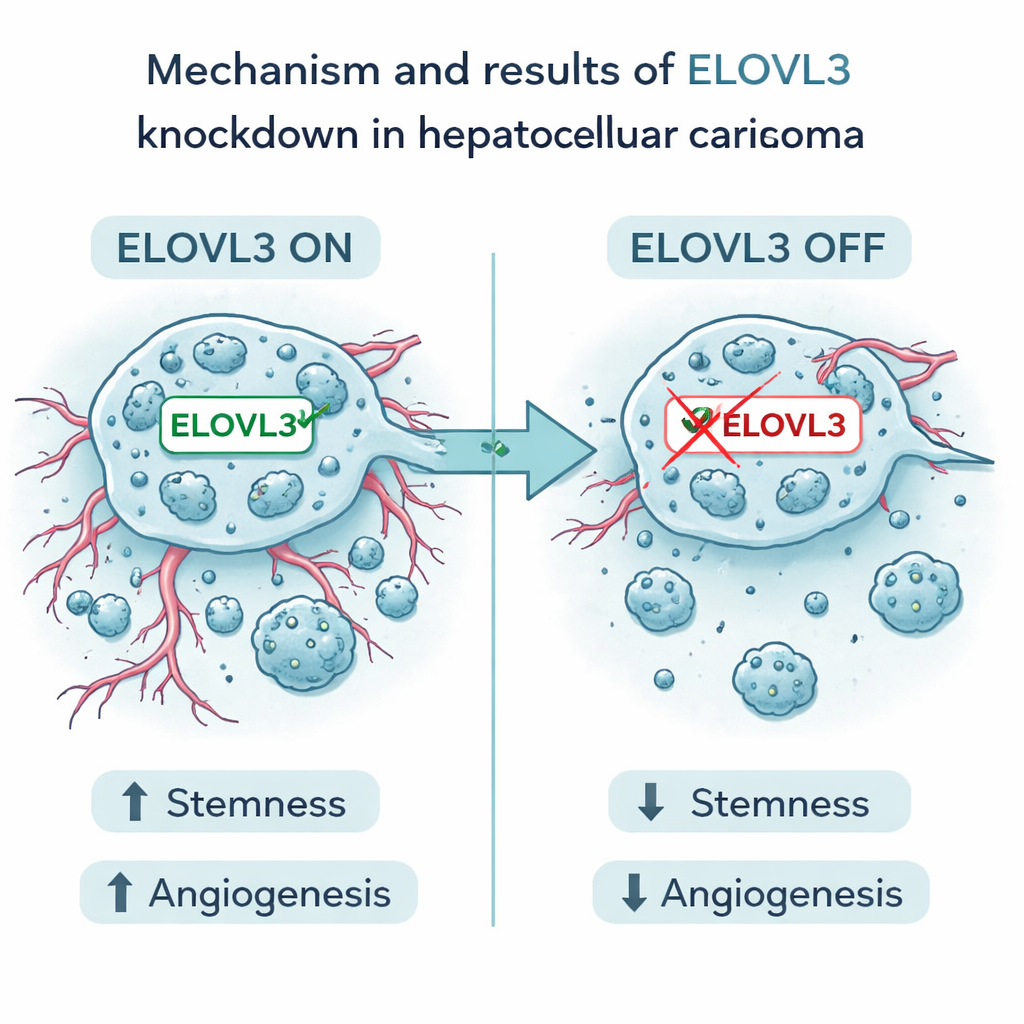
Fokus på ett lovande mål
Bland de nio generna framstod en kallad ELOVL3. Höga nivåer av denna gen var kopplade till sämre överlevnad. I laboratorieexperiment minskade författarna ELOVL3 i mänskliga levercancerceller. Det gjorde cellerna mindre kapabla att bilda stamliknande kluster och minskade nivåerna av välkända stamhetsmarkörer. Det minskade också produktionen och frisättningen av två huvudfaktorer som främjar kärlbildning, VEGFA och FGF2. Cancercellerna växte, migrerade och invaderade mindre, och i musexperiment var tumörer med reducerat ELOVL3 mindre och visade färre tecken på aggressiv sjukdom. Dessa fynd stödjer idén att ELOVL3 bidrar till både levercancercellernas fröliknande beteende och deras förmåga att bygga stödjande blodkärl.
Vad detta kan betyda för framtida vård
I klartext levererar arbetet två huvudsakliga budskap. För det första kan en enkel niogenspoäng härledd från tumörprover sortera levercancerpatienter i högre respektive lägre riskgrupper och ge en indikation på hur de kan svara på immunbaserade behandlingar. För det andra verkar en av generna i poängen, ELOVL3, ligga i ett korsfält mellan tumörens förmåga att regenerera och dess förmåga att skapa nya blodkärl, vilket gör den till ett attraktivt läkemedelsmål framöver. Även om modellen och målet behöver bekräftas i prospektiva kliniska prövningar öppnar de dörren för mer individualiserad levercancervård och för kombinationsstrategier som blockerar både cancerens "fröceller" och deras blodtillförsel.
Citering: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Nyckelord: levercellscancer, cancerstamceller, angiogenes, prognostiskt gensekret, ELOVL3