Clear Sky Science · sv
DGCR8 reglerar flera processer i transkriptionskopplad nukleotid-excisionsreparation
Hur solljus talar med våra gener
Varje gång vi går ut i solen träffas huden av osynliga ultravioletta (UV) strålar som skadar DNA i våra celler. Oftast reparerar cellerna tyst dessa skador innan de orsakar problem. Denna studie avslöjar en oväntad aktör i det skyddssystemet: ett protein kallat DGCR8, tidigare känt för att hjälpa celler att producera microRNA. Forskarna visar att DGCR8 kan byta uppgift efter UV-exponering och samordna flera steg i en viktig DNA-reparationsväg som hjälper till att förebygga cancer och andra sjukdomar.
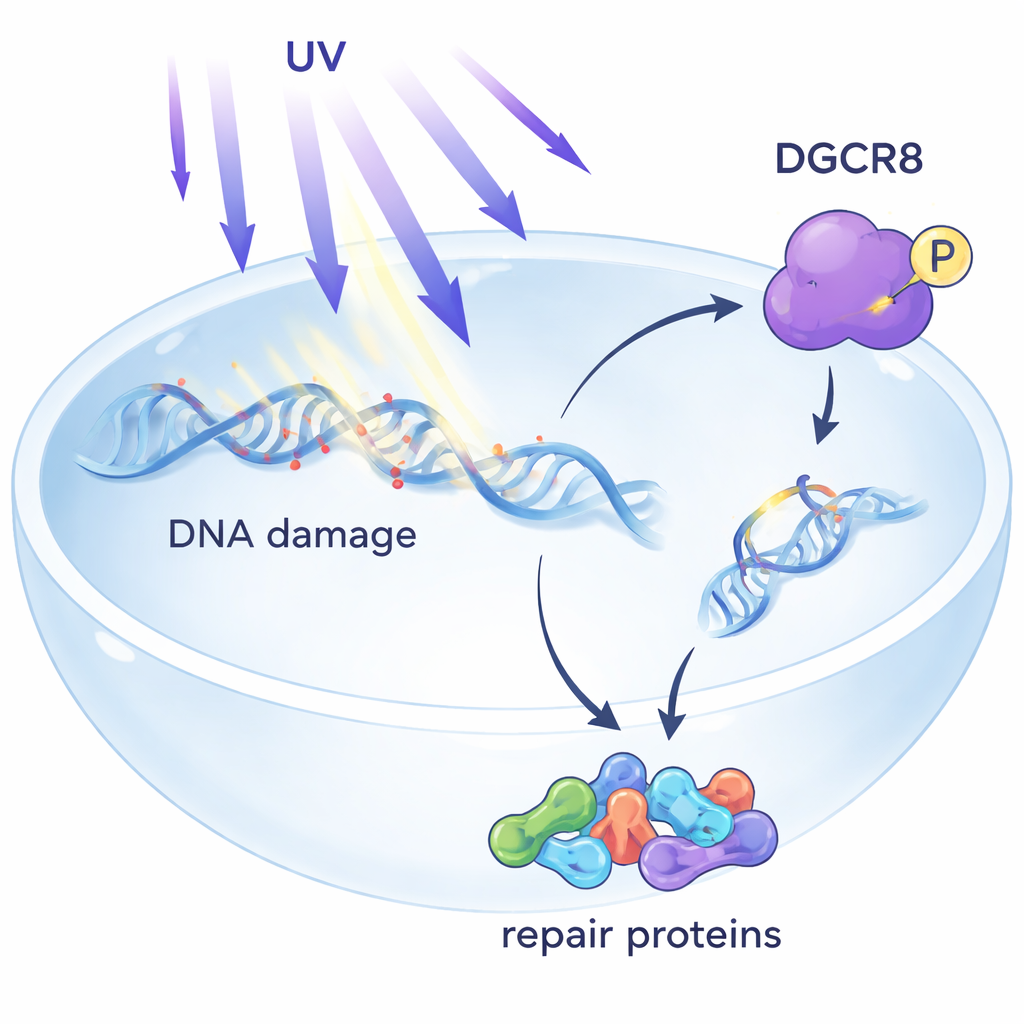
En dold väktare i DNA-reparation
UV-ljus skapar små lesioner i DNA som kan blockera de molekylära maskiner som läser gener. Ett av kroppens huvudförsvar är transkriptionskopplad nukleotid-excisionsreparation, eller TC-NER, som riktar in sig på skador som stannar upp genläsande enzymer. Hittills var DGCR8 mest känt för att bearbeta microRNA, korta RNA-molekyler som finjusterar genaktivitet. Tidigare arbete antydde att DGCR8 också skyddar celler mot UV, men hur det gick till var oklart. Denna artikel visar att DGCR8, efter UV-exponering, fysiskt associerar med centrala TC-NER-faktorer och fungerar som en organisatör som för samman reparationskomponenter precis där genläsning har blockerats.
En molekylär på-/av-knapp för DGCR8
Nyckeln till DGCR8:s nya roll är en enskild kemisk märkning på en av dess byggstenar, aminosyran serin på position 153. När denna plats fosforyleras—det vill säga när en fosfatgrupp läggs till—får DGCR8 förmågan att binda till centrala TC-NER-aktörer, inklusive RNA-polymeras II (genenläsningsenzymet) och reparationsfaktorerna CSB, CSA och UVSSA. Celler som konstruerats med en version av DGCR8 som inte kan fosforyleras på denna plats (S153A-mutanten) visade svaga eller förlorade interaktioner mellan dessa reparationsproteiner, och den normala UV-utlösta sammankomsten av reparationskomplexet misslyckades. En ”fosfomimetisk” variant som beter sig som om den alltid är fosforylerad hade motsatt effekt och stärkte viktiga interaktioner även utan UV. Dessa resultat indikerar att fosforylering vid Ser153 fungerar som en på-/av-knapp som växlar DGCR8 från dess vanliga RNA-bearbetningsroll till en koordinator för DNA-reparation.
Trassla upp farliga DNA–RNA-knutar
Förutom att samla reparationsproteiner hjälper DGCR8 också till att hantera strukturer som kallas R-loopar—korta sträckor där nyligen syntetiserat RNA återfäster till det DNA det härstammar från och bildar ett DNA–RNA-hybrid. I små mängder kan R-loopar vara användbara, men när de ackumuleras efter UV-exponering kan de stoppa DNA-kopiering och göra kromosomer instabila. Med specialiserade antikroppar och fluorescerande prober fann författarna att celler utan DGCR8, eller som bär den icke-fosforylerbara S153A-formen, bygger upp betydligt fler R-loopar efter UV. Fosforylerat DGCR8 sågs vid dessa hybridstrukturer, särskilt där de överlappade med UV-inducerade lesioner, vilket tyder på att det hjälper till att förebygga eller rensa skadliga R-loopar precis vid aktiva gener under stress.
Kontroll av DNA-kopiering
När DNA-skador eller R-loopar stör kopieringen av genomet bromsar celler normalt sin replikation via ett skyddssystem känt som ATR–CHK1-checkpointen. Fiber-spårningsexperiment visade att celler med normalt DGCR8 saktade ner sina replikationsbanor efter UV-exponering, vilket speglar en aktiverad checkpoint. I en slående kontrast fortsatte celler som saknade DGCR8 eller bar S153A-mutationen att replikera i nästan normal takt, trots att de hade ackumulerat DNA-skador och R-loopar. Ytterligare tester visade att medan ATR självt aktiverades, så var dess viktiga partner CHK1 dåligt aktiverad i dessa mutanta celler. Detta tyder på att fosforylerat DGCR8 hjälper till att vidarebefordra stressignalen från skadat DNA och R-loopar till CHK1, vilket gör det möjligt för cellen att pausa och stabilisera replikationen.
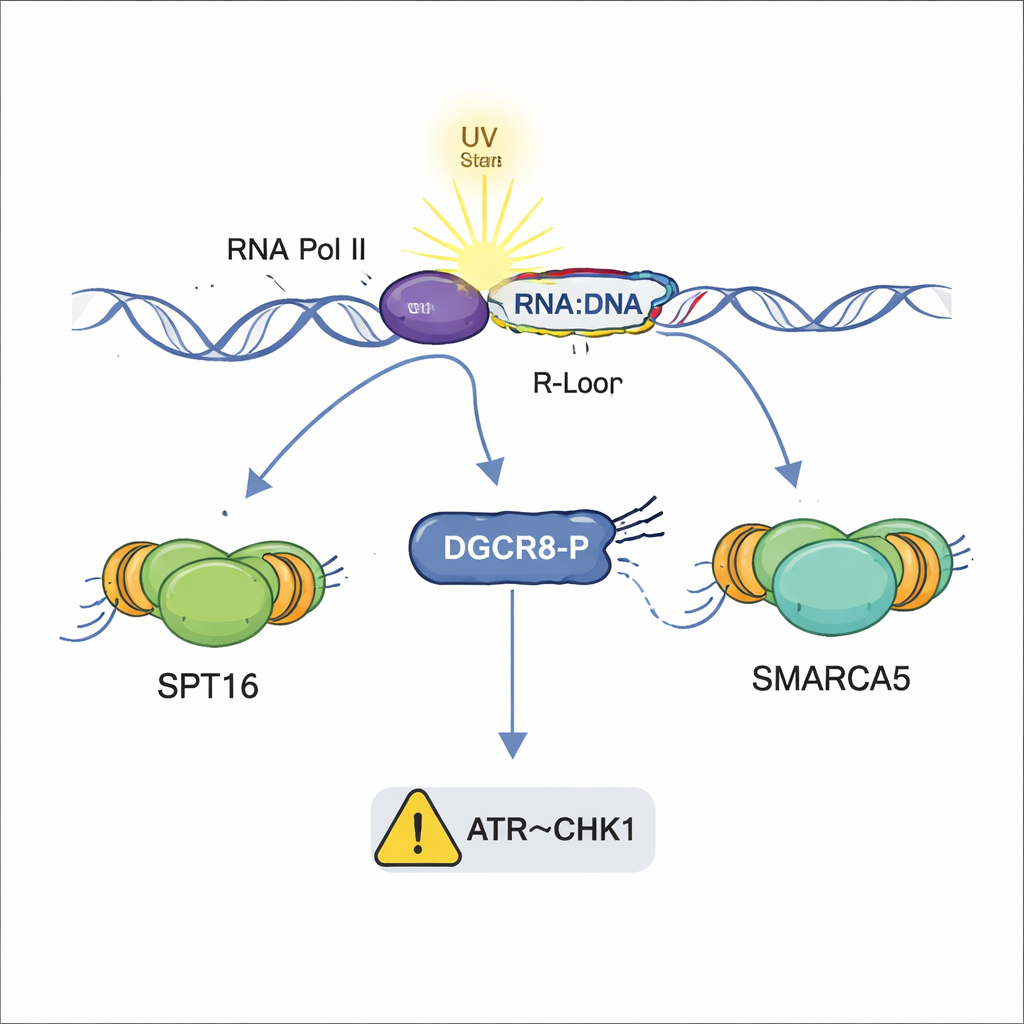
Varför detta är viktigt för hälsa och sjukdom
Tillsammans visar fynden att DGCR8 är en mångsidig väktare som samordnar flera lager av UV-skaderesponsen: ihopställning av TC-NER-reparationslaget, rekrytering av kromatinombyggare som öppnar upp DNA, begränsning av skadliga DNA–RNA-hybrid och hjälp med att utlösa en replikationsinbromsning via ATR–CHK1-vägen. Avgörande är att dessa funktioner är separata från DGCR8:s traditionella uppgift i microRNA-biogenes och beror på fosforylering av en enda plats. Eftersom fel i DNA-reparation och R-loop-kontroll är kopplade till cancer och neurologiska sjukdomar, och DGCR8-mutationer har identifierats i vissa tumörer, kan förståelsen av denna molekylära strömbrytare öppna nya vägar för diagnostik eller behandling av tillstånd som drivs av UV-skador och genominstabilitet.
Citering: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
Nyckelord: UV-DNA-skada, DGCR8, DNA-reparation, R-loopar, genomstabilitet