Clear Sky Science · sv
PARP-1 kopplar ihop β-catenin/TCF4‑signalering med epitelskiv–mesenkymal omvandling vid endometrios
Varför denna forskning är viktig för kvinnors hälsa
Endometrios är ett smärtsamt tillstånd där vävnad som liknar livmoderslemhinnan växer på fel ställen, till exempel på äggstockarna. Dessa felplacerade fläckar kan invadera närliggande strukturer, orsaka ärrbildning och bidra till infertilitet, men nuvarande behandlingar är ofta otillräckliga och symtomen återkommer ofta. Denna studie undersöker en molekylär "strömbrytare" kallad PARP‑1 och ställer frågan om den hjälper endometrioslesioner att bli mer invasiva — och om befintliga läkemedel som blockerar PARP‑1 kan dämpa den strömbrytaren.
Närmare om invasivt lesionbeteende
Även om endometrios klassificeras som en benign sjukdom, beter sig den ektopiska (felplacerade) vävnaden ofta förvånansvärt aggressivt: den migrerar, implanterar och persisterar påminnande om en långsamt växande cancer. En nyckelprocess bakom detta beteende är epitelskiv–mesenkymal omvandling, eller EMT, där ordnade, skivbildande celler luckrar upp sina förbindelser och antar en mer rörlig, fibrös identitet. Forskarna undersökte vävnad från kvinnor med och utan endometrios och fann att ovariala endometrioslesioner visade ett tydligt EMT‑liknande mönster: "limproteinet" E‑cadherin var minskat, medan markörer för mer rörliga celler, såsom N‑cadherin och vimentin, ökade. Samtidigt var nivåerna av PARP‑1 och komponenter i en tillväxtreglerande väg känd som Wnt/β‑catenin som högst i dessa lesioner, vilket tyder på att alla dessa förändringar rör sig tillsammans.
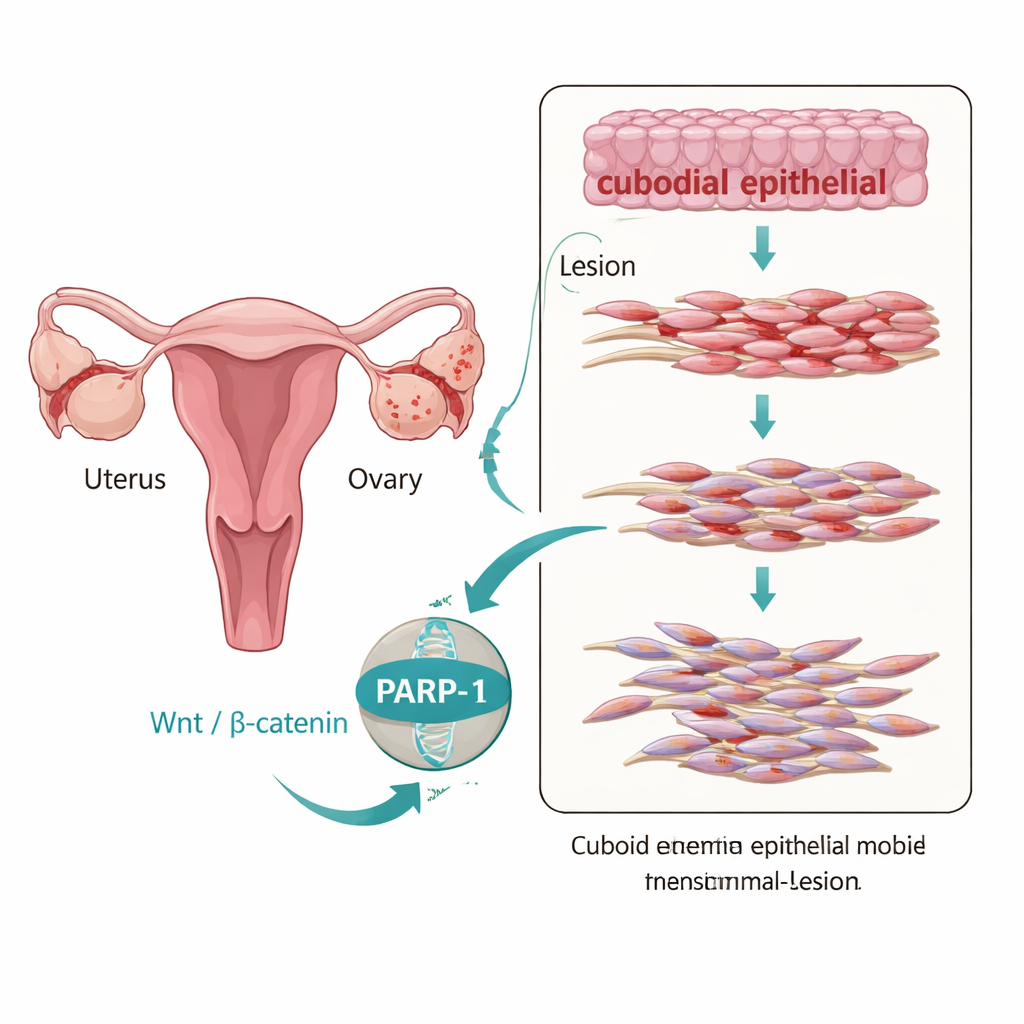
Den molekylära bron mellan signaler och cellförändring
För att ta reda på om PARP‑1 bara är närvarande eller aktivt driver dessa förändringar använde forskarna en odödliggjord endometriotisk epitelcellinje kallad 12Z. När de artificiellt ökade PARP‑1‑nivåerna i dessa celler skiftade EMT‑markörerna mot en mer invasiv profil och cellerna blev mer rörliga och livskraftiga i laboratorietester som efterliknar sårläkning och vävnadsinvasion. När de minskade PARP‑1 med riktade RNA‑molekyler vände mönstret: E‑cadherin ökade, mesenkymala markörer sjönk och cellerna rörde sig och växte mindre. Viktigt är att PARP‑1 fysiskt associerade med β‑catenin och TCF4, två nyckelfaktorer som översätter Wnt‑signaler till genaktivitet, vilket pekar på PARP‑1 som en bro som hjälper till att länka yttre signaler till EMT‑genprogrammet inne i kärnan.
Att dämpa strömbrytaren med ett cancerläkemedel
Då läkemedel som blockerar PARP‑aktivitet redan används i cancerbehandling frågade teamet om ett sådant läkemedel, olaparib, kunde mildra EMT‑lika drag och minska lesionstillväxt i en musemodell för endometrios. Möss som fick små fragment av livmodervävnad implanterade utvecklade ektopiska lesioner i buken, vilket efterliknade delar av den mänskliga sjukdomen. När de behandlades med olaparib i två veckor hade dessa djur markant mindre total lesionsvolym och lättare livmödrar med färre vidhäftande lesioner jämfört med obehandlade kontroller. Vävnad från behandlade möss visade också ett mer "epitelialt" markörmönster — högre E‑cadherin och lägre N‑cadherin, vimentin, β‑catenin och TCF4 — vilket indikerar att PARP‑hämmning hade skjutit cellerna bort från det invasiva EMT‑lika tillståndet.
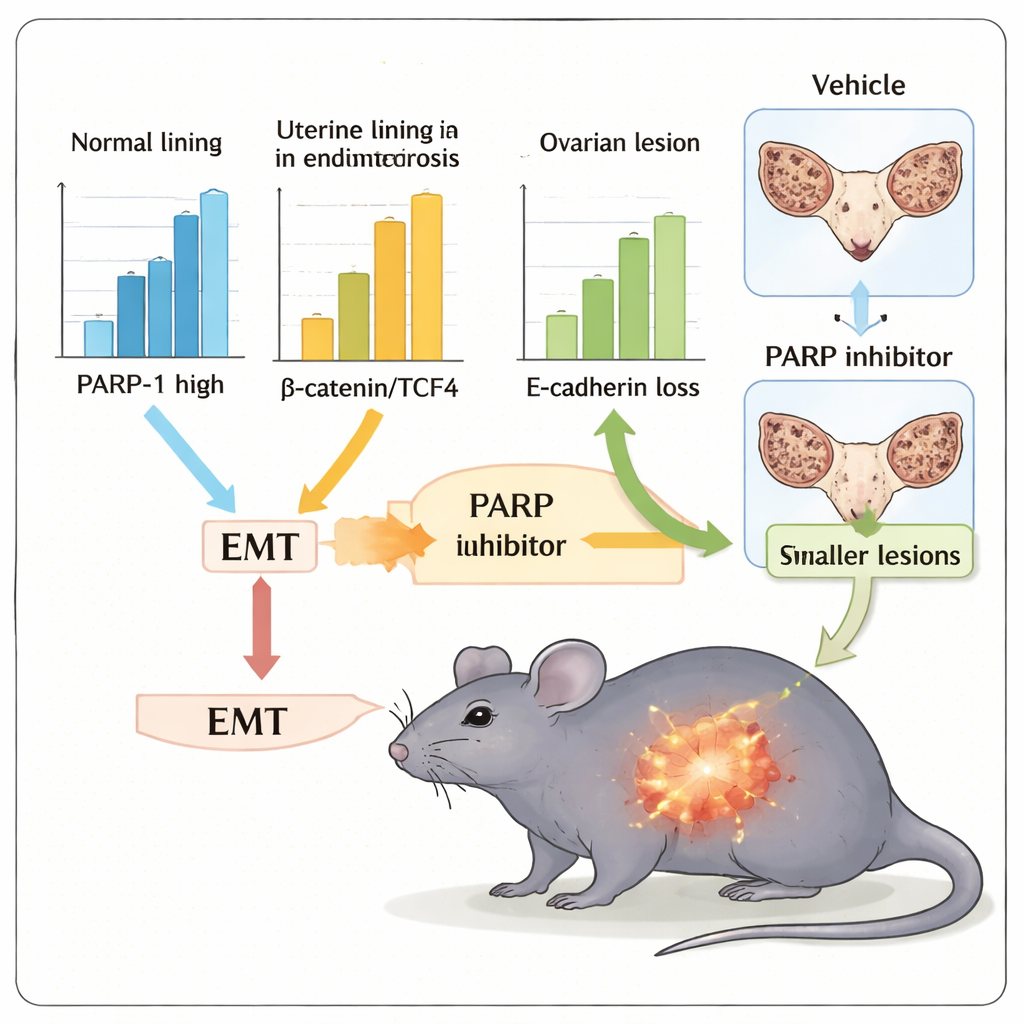
Vad detta kan innebära för framtida vård
Tillsammans stöder fynden från patientprover, cellkulturexperiment och musemodellen en enhetlig idé: PARP‑1 fungerar som en läkemedelsmålbar knutpunkt som kopplar Wnt/β‑catenin‑signalering till EMT‑liknande beteende vid endometrios. Istället för att vara den enda huvudströmbrytaren framstår PARP‑1 som en viktig förbindelse i ett större nätverk av inflammation, oxidativ stress och hormonstyrda signaler som formar hur lesioner växer och invaderar. Eftersom PARP‑hämmare redan finns ökar detta arbetet möjligheten att återanvända eller anpassa dem — kanske i kombination med andra väg- eller immunriktade läkemedel — för att minska lesionbörda, ärrbildning och eventuellt påverkan på fertilitet. Större och längre studier kommer att behövas, men denna forskning öppnar en konkret väg mot mer målinriktade, mekanismbaserade terapier för ett tillstånd som drabbar miljontals kvinnor världen över.
Citering: Zhang, L., Li, X., Kong, L. et al. PARP-1 couples β-catenin/TCF4 signaling to epithelial–mesenchymal transition in endometriosis. Sci Rep 16, 6940 (2026). https://doi.org/10.1038/s41598-026-38335-8
Nyckelord: endometrios, PARP-1, epitelskiv–mesenkymal omvandling, Wnt/β-catenin, PARP‑hämmarbehandling