Clear Sky Science · sv
En ny AI-kopplad flödeskammarmetod som kvantifierar erytrocyters osmotiska bräcklighet
Varför röda blodkroppars bräcklighet spelar roll
Varje sekund pressas miljontals av dina röda blodkroppar genom hårtunna kärl medan de transporterar syre. Hur lätt dessa celler spricker under påfrestning — deras ”bräcklighet” — kan avslöja anemi, problem med blodlagring och komplikationer vid allvarliga infektioner som sepsis. Denna studie presenterar en modern, AI‑stödd mikroskop‑enhet som mäter hur snabbt röda blodkroppar faller sönder i saltlösningar, med målet att göra detta viktiga test snabbare, mer precist och enklare att genomföra både i forskningslaboratorier och så småningom på sjukhus.
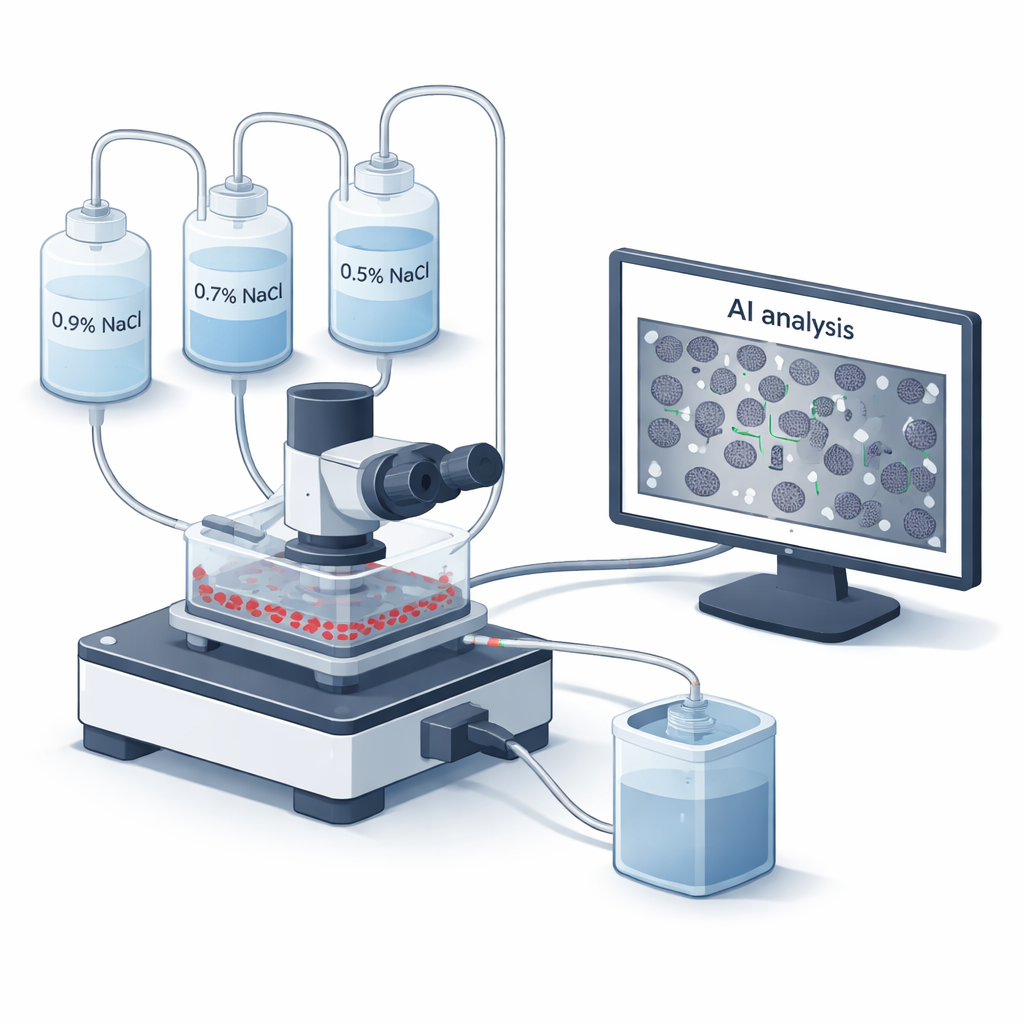
Ett nytt sätt att observera blodceller under stress
Läkare har använt tester för osmotisk bräcklighet sedan 1940‑talet för att bedöma hur motståndskraftiga röda blodkroppars membran är. Traditionellt blandas blod med en serie saltlösningar, och en maskin mäter hur mycket hemoglobin som läcker ut när celler lyserar. Även om den klassiska metoden är pålitlig är den långsam, manuell och ser inte hur enskilda celler ser ut när de fallerar. Forskargruppen bakom denna artikel byggde ett nytt mikrofluidiskt ”flödeskammarsystem”, kallat BioExP, som sprider röda blodkroppar som ett tunt monolager på en behandlad glasyta. Olika saltlösningar pumpas över detta lager medan ett mikroskop och en kamera spelar in vad som händer i realtid, och inbyggd programvara använder artificiell intelligens för att räkna hur många celler som förblir intakta vid varje saltkoncentration.
Att sätta AI och flödeskontroll på prov
För att bedöma om BioExP är pålitligt jämförde forskarna det direkt med den gamla spektrofotometerbaserade analysen med blod från fyra friska givare. De fokuserade på en nyckelstorhet kallad MCF₅₀: den saltkoncentration där hälften av de röda cellerna har lyserat. Först behövde de ställa in sitt nya system genom att hitta bästa ”mättnadstiden” — hur länge cellerna ska exponeras för en given lågsaltlösning så att de mest sårbara cellerna lyserar utan att överexponera. Genom att följa hur många celler som försvann vid 0,4 % salt under 15 minuter fann de att nästan 80 % av all hemolys skedde under de första tre minuterna. Detta treminutfönster blev deras standardexponeringstid, vilket balanserade hastighet med tillförlitliga mätningar.
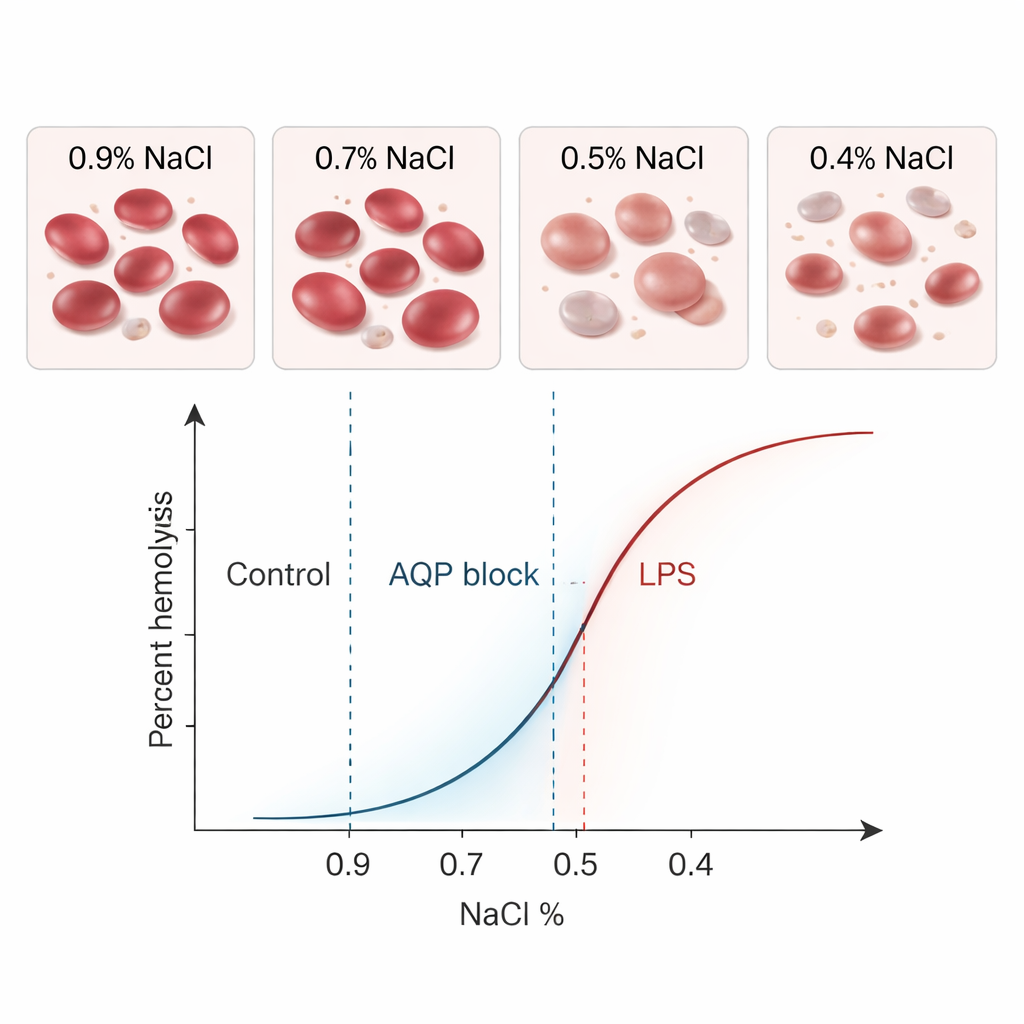
Överensstämmelse med det klassiska testet och undersökning av verklig biologi
När de körde samma friska prov genom båda metoderna gav BioExP och det klassiska testet nästan identiska genomsnittliga MCF₅₀‑värden — 0,41 % salt — med liknande spridning. Statistiska analyser visade ingen meningsfull skillnad mellan metoderna, och de flesta parade resultat hamnade inom snäva överensstämmelsegränser. Med andra ord talade den nya enheten i praktiken samma ”språk” som den etablerade analysen. Den verkliga styrkan hos BioExP ligger dock i dess förmåga att testa hur olika tillstånd ändrar cellernas bräcklighet. Forskarna valde två biologiskt viktiga modifierare: kvicksilverklorid, som blockerar vattenkanalproteiner kallade akvaporiner i cellmembranet, och bakteriellt lipopolysackarid (LPS), ett toxin kopplat till sepsis.
Hur toxiner och vattenkanaler förändrar cellernas tålighet
Blockering av akvaporiner gjorde röda blodkroppar svårare att få att lysera: MCF₅₀ försköts till lägre saltvärden, vilket betyder att cellerna tålde större utspädning innan de brast. Både BioExP och den klassiska metoden upptäckte denna förskjutning åt vänster tydligt. LPS gav motsatt effekt. När röda celler inkuberades med en hög dos LPS i frånvaro av plasma blev de mer bräckliga och lyserade vid högre saltkoncentrationer. Under mikroskopet förändrade många celler form, blev mer sfäriska eller taggiga — visuella tecken på att deras membran hade påverkats. Återigen registrerade båda metoderna en stark, statistiskt signifikant förskjutning åt höger i bräcklighetskurvorna. I alla dessa tester följde det nya flödeskammarsystemet konsekvent samma biologiska trender som den äldre analysen, om än med något lägre absoluta värden som var små och systematiska.
Vad detta betyder för patienter och labb
BioExP‑plattformen kortar analystiden från flera timmar till under en timme, kräver bara mycket små blodvolymer (möjligen bara ett stick i fingret) och automatiserar räkning och kurvpassning med AI istället för att förlita sig på många manuella steg. Eftersom den avbildar exakt samma celler över tid kan den koppla hur cellerna ser ut till hur lätt de lyserar, och den kan testa många saltnivåer eller läkemedelsförhållanden i en enda körning. Studien visar att detta moderna angreppssätt kan matcha noggrannheten hos det klassiska testet för osmotisk bräcklighet samtidigt som det tillför hastighet, flexibilitet och rik visuell information. Om det valideras vidare i större och mer mångsidiga givarpopulationer kan sådana system bli värdefulla verktyg för att diagnostisera hemolytiska anemier, övervaka lagrat blod i blodbanker och utforska hur infektioner eller nya läkemedel försvagar eller skyddar våra röda blodkroppar.
Citering: Fırat, I.S., Alaçayır, Ö., Creutz, T. et al. A novel AI-coupled flow chamber method quantifying erythrocyte osmotic fragility. Sci Rep 16, 7175 (2026). https://doi.org/10.1038/s41598-026-38322-z
Nyckelord: röda blodkroppar, osmotisk bräcklighet, mikrofluidik, sepsis, artificiell intelligens