Clear Sky Science · sv
Selektiv inaktivering av Lis1 stör migration och positionering av kortikala somatostatin‑interneuroner
Varför små hjärnceller och ett enda gen är viktiga
Inuti våra hjärnor måste miljarder nervceller hamna på precis rätt plats för att tankar, känslor och minnen ska fungera korrekt. Denna studie undersöker en liten men inflytelserik grupp hjärnceller kallade somatostatin‑interneuroner och ett gen som heter Lis1, redan känt för att orsaka en svår "slät hjärna"‑störning när det är muterat. Genom att ställa frågan vad som händer när Lis1 stängs av endast i denna lilla cellpopulation avslöjar forskarna hur subtila fel i cellrörelse under utvecklingen kan omforma viktiga hjärnregioner som är inblandade i stämning, minne och psykisk sjukdom.
Nyckelspelare i hjärnans bromssystem
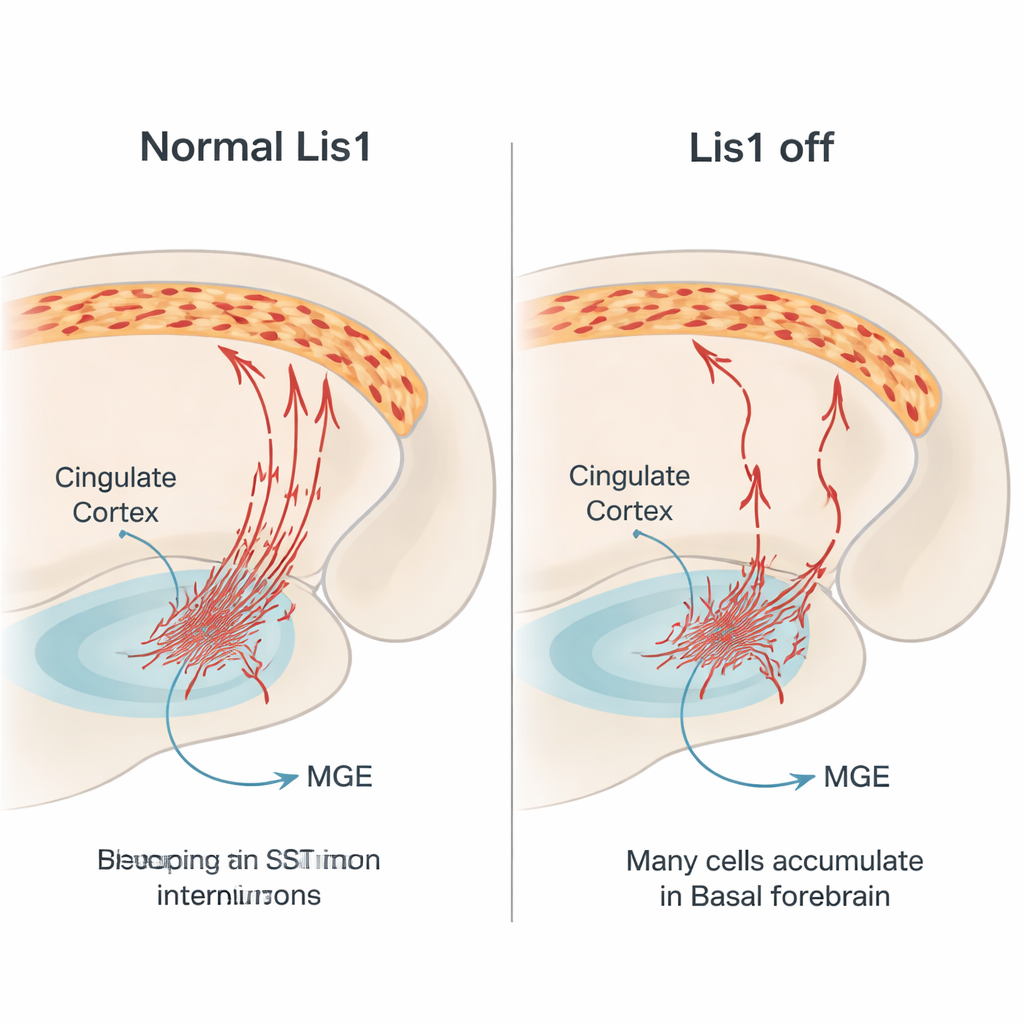
Somatostatin‑interneuroner fungerar som en del av hjärnans bromssystem. De frisätter den hämmande signalsubstansen GABA och peptiden somatostatin, och riktar sig främst mot utskotten hos excitatoriska pyramidceller. Det hjälper till att hålla hjärnans aktivitet i balans, vilket är avgörande för normal perception, beslutsfattande och emotionell kontroll. Många av dessa interneuroner föds i en djup region av den embryonala hjärnan kallad medial gangliär eminens. Därifrån färdas de sidledes långa sträckor in i hjärnbarken, inklusive cingulära kortex, en nod för känslor, smärta och minne. Eftersom denna resa är komplex och noggrant tidsbestämd är gener som styr cellrörelse kritiska. Lis1 är ett sådant gen, känt för att reglera cellens interna skelett och motoriska maskineri som förflyttar kärnan och formar cellen under migration.
Ett riktat genetiskt "stäng av"‑experiment
För att ta reda på vad Lis1 gör specifikt i somatostatin‑interneuroner konstruerade författarna möss där Lis1 raderas endast i celler som aktiverar somatostatin‑genen. De använde också ett fluorescerande rött protein för att permanent märka dessa celler och följa dem under utvecklingen. Denna design gjorde det möjligt för teamet att särskilja effekter inne i somatostatin‑cellerna själva från förändringar i resten av hjärnan. De undersökte därefter två cingulära regioner — anteriora cingulate cortex och retrospleniala cortex — omkring en månad efter födseln, en tid då kortikala kretsar är relativt mogna men fortfarande plastiska. Noggranna räkne‑metoder användes för att uppskatta både det absoluta antalet och tätheten av somatostatin‑interneuroner i varje kortikal lager.
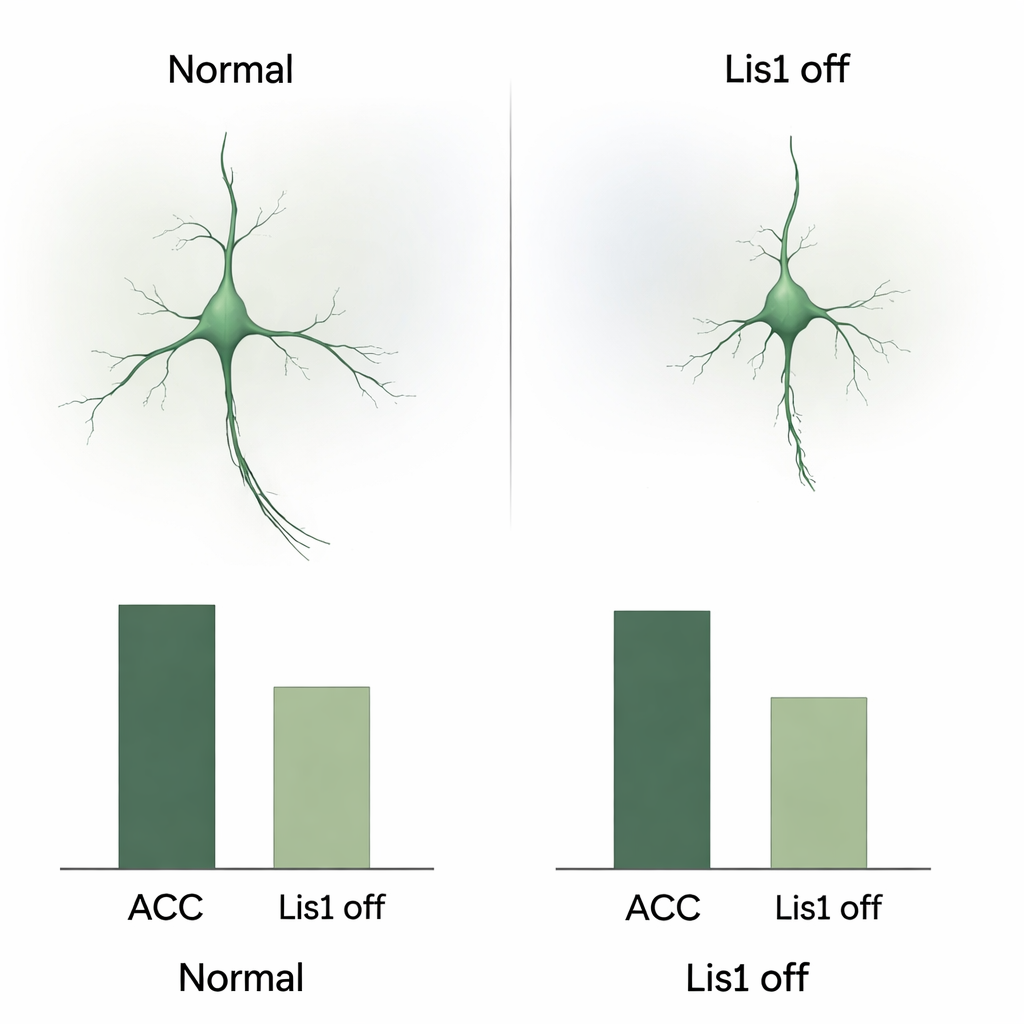
I unga vuxna möss som saknade Lis1 i somatostatin‑interneuroner innehöll både anteriora cingulate och retrospleniala kortex betydligt färre av dessa celler än hos kontroll‑djur. Minskningen var stor och konsekvent över alla undersökta lager, vilket indikerar en verklig förlust snarare än en enkel omfördelning. När forskarna granskade hur de kvarvarande cellerna var ordnade fann de en förändring i det vanliga lagermönstret. I friska möss tenderar somatostatin‑interneuroner att vara mer koncentrerade i de djupare lagren av kortex. I mutantdjuren var denna gradient omvänd, med relativt fler celler i de övre lagren och färre i det djupaste lagret. Viktigt är att den övergripande storleken på de cingulära regionerna inte krympte, så den lägre tätheten speglar verkligen saknade interneuroner och inte en komprimerad vävnadsvolym.
Utvecklingsresan som går snett
För att förstå hur denna förlust uppstår följde teamet de rödmarkerade somatostatincellerna i embryon. De bekräftade att Lis1‑raderingen börjar efter att dessa celler slutat dela sig, vilket utesluter en direkt effekt på deras födelse. Problemen uppstod istället under deras långa migration. I mitten av graviditeten hittades betydligt färre märkta celler som färdades genom de normala vägarna mot kortex, och många verkade stanna upp i basala framhjärnan, en ventral region de måste korsa. De migrerande celler som faktiskt rörde sig visade förändrade former: kortare ledande utskott, färre förgreningar och mindre, rundare cellkroppar — alla tecken på att deras interna transportmaskineri var komprometterat. I senare stadier innehöll den ventrala regionen hos mutanter fler celler som visade markörer för programmerad celldöd, vilket tyder på att många fastnade interneuroner dör innan de når kortex.
Vad detta betyder för hjärnhälsa
Enkelt uttryckt: när Lis1 stängs av endast i somatostatin‑interneuroner börjar många av dessa celler sin resa normalt men når inte sina slutdestinationer i cingulära kortex. Några ansamlas och dör på vägen, och de som anländer är färre till antalet och ojämnt positionerade över kortikala lager. Eftersom somatostatin‑system har kopplats upprepade gånger till depression, schizofreni, epilepsi och neurodegenerativa sjukdomar framhäver detta arbete en direkt, cellspecifik väg genom vilken Lis1‑funktionsbortfall kan bidra till störda hjärnrytmer och psykiatriska symptom. Studien visar att även en relativt liten neuronpopulation, styrd av ett enda gen, kan vara avgörande för att bygga de balanserade kretsar som ligger till grund för hälsosamt tänkande och beteende.
Citering: Pombero, A., García-López, R., Geijo-Barrientos, E. et al. Selective Lis1 inactivation disrupts migration and positioning of cortical somatostatin interneurons. Sci Rep 16, 7330 (2026). https://doi.org/10.1038/s41598-026-38316-x
Nyckelord: somatostatin‑interneuroner, Lis1‑genet, neuronal migration, cingulära kortex, neurodevelopmentala störningar