Clear Sky Science · sv
Heterogena grafneurala nätverk avslöjar molekylära mekanismer för folatbrist vid placentainsufficiens genom multiomisk integrering
Varför detta är viktigt för mödrar och barn
Folat är mest känt som vitaminen i graviditetstabletter som hjälper till att förebygga missbildningar, men dess roll i en frisk graviditet är mycket mer omfattande. I denna studie undersöks hur brist på folat tyst kan skada placenta — organet som försörjer och skyddar det växande fostret. Genom att kombinera banbrytande biologi med avancerad artificiell intelligens visar forskarna hur subtila förändringar i gener, proteiner och små molekyler samverkar för att beröva placentan det den behöver, och de utforskar hur denna kunskap en dag kan hjälpa läkare att tidigare upptäcka högriskgraviditeter.
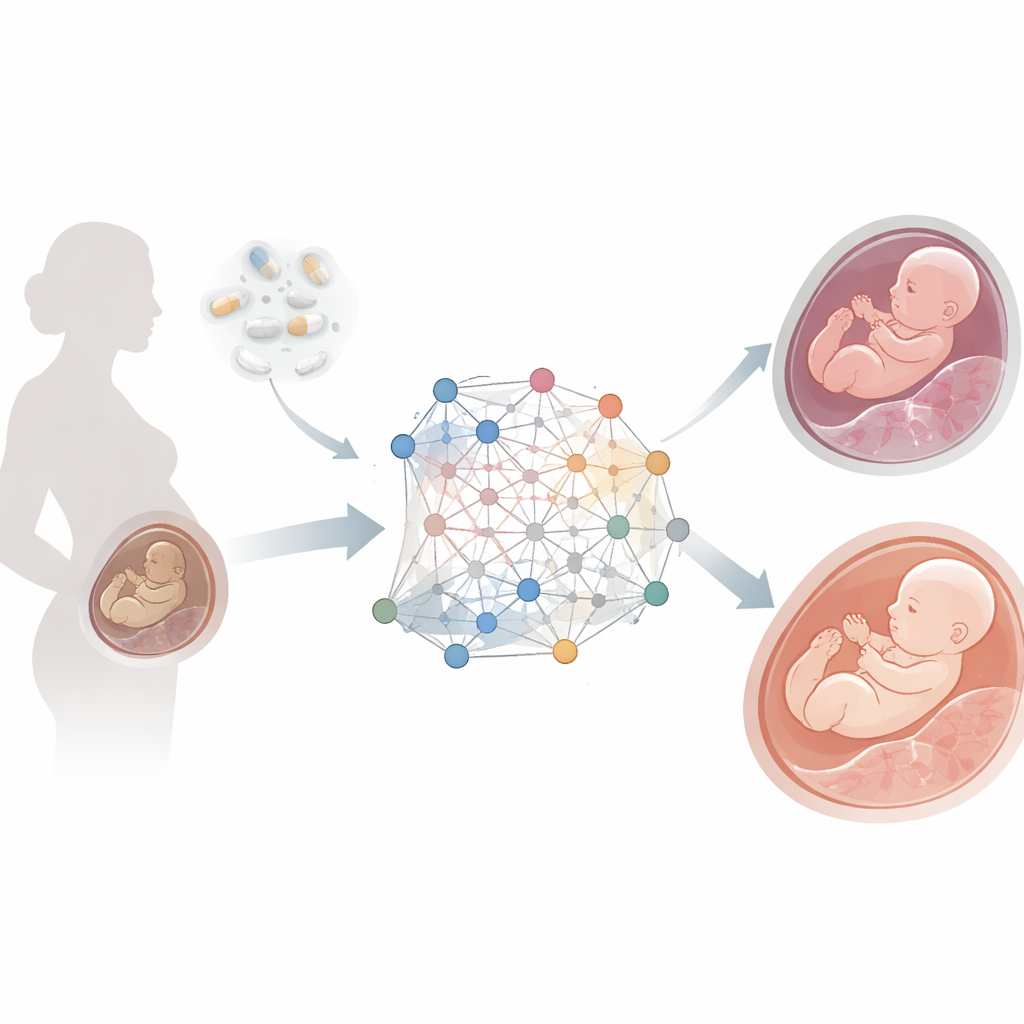
När placentan inte räcker till
Placentainsufficiens uppstår när placentan inte kan leverera tillräckligt med syre och näring till fostret, vilket leder till komplikationer som tillväxthämning, preeklampsi och för tidig födsel. Tillståndet drabbar ungefär fem till tio procent av graviditeter globalt. Folat står i centrum för många cellprocesser — uppbyggnad av DNA, styrning av vilka gener som är aktiva och stöd för friska blodkärl. När folatnivåerna är för låga kan dessa system misslyckas, men den precisa kedjan av händelser i placentavävnad har varit svår att kartlägga. Traditionella studier undersöker ofta bara en typ av biologiska data i taget, till exempel gener eller metaboliter, och missar då helheten i hur dessa nivåer samspelar.
Att läsa placentan med många perspektiv
För att hantera denna komplexitet samlade teamet placentaprover vid förlossning från 156 graviditeter med folatrelaterad placentainsufficiens och 142 friska kontroller. Från varje prov mätte de fyra olika typer av molekylär information: DNA‑förändringar, genaktivitet, proteinnivåer och små metaboliter. Istället för att behandla dessa mätningar som långa, separata listor kopplade de ihop dem i en stor biologisk karta innehållande 6 704 molekyler och över 16 000 kända interaktioner. Gener, proteiner och metaboliter representerades som olika typer av noder kopplade med kanter som speglade hur de binder, reglerar eller omvandlar varandra i verkliga celler.
Att lära ett smart nätverk att upptäcka problem
Forskarna tränade sedan en specialiserad AI‑modell kallad ett heterogent grafneuralt nätverk på denna molekylära karta. Till skillnad från standardalgoritmer som ser varje mätning isolerat, ”lyssnar” denna modell på hur signaler sprids över hela nätverket. Den tilldelar uppmärksamhetsvikter för att framhäva de mest informativa molekylerna och kopplingarna för att skilja sjuka placentor från friska. På ett hållet testset klassificerade modellen korrekt 94,7 % av placentorna och uppnådde ett nästan perfekt area under ROC‑kurvan (AUC) på 0,978, och överträffade tydligt traditionella maskininlärningsmetoder och analyser som använde endast en datatyp. Detta visar att sjukdomssignalen inte bara finns i enskilda markörer, utan i mönster som delas över flera biologiska lager.
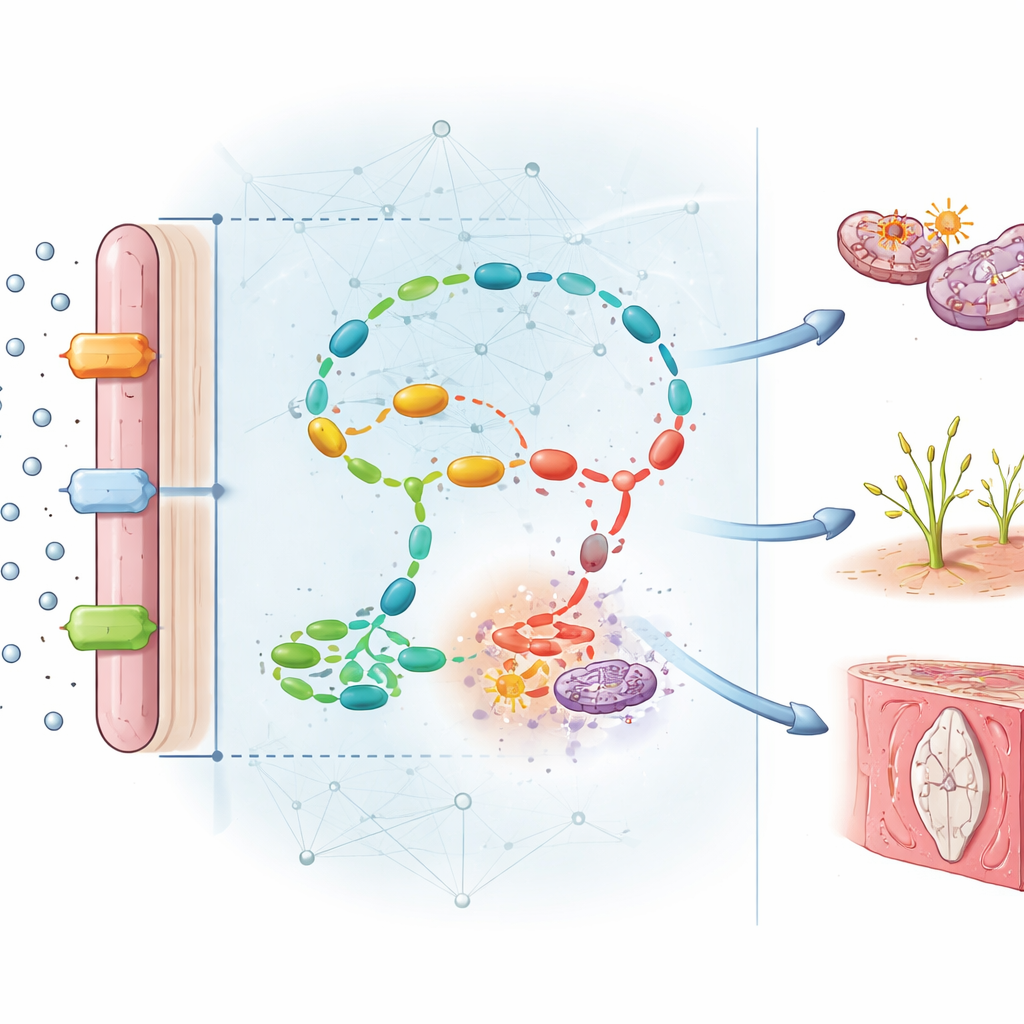
Att avslöja de dolda kedjorna av skada
Utöver prediktion gjorde modellens utformning det möjligt för författarna att se vilka molekyler som bar mest vikt i dess beslut. Flera framträdde. Centrala komponenter för folathantering — såsom enzymet MTHFR och folattransportören FOLR1 — var starkt reducerade i sjuka placentor, medan homocystein, en toxisk biprodukt, ackumulerades mer än sexfaldigt. Från nätverket framträdde sju större funktionella moduler som kopplade störd folatkemi till minskad DNA‑metylering, ökad oxidativ stress, felaktig blodkärlsbildning, inflammation och överdriven celldöd. Med andra ord skadar inte folatbrist placentan på ett enda sätt; den sätter igång ett nätverk av sammankopplade fel som tillsammans begränsar blodflödet och näringstillförseln till fostret.
Vad detta kan innebära för framtida vård
För nu är detta arbete främst ett kraftfullt mikroskop snarare än ett sängkantsprov. Eftersom alla prover togs vid förlossningen kan modellen ännu inte användas för att förutsäga risk under graviditeten, när intervention skulle vara mest betydelsefull. Trots det erbjuder de molekylära signaturer den avslöjar — särskilt de kombinerade förändringarna i folattransport, homocysteinansamling och skadade kärltillväxtvägar — en färdplan för att söka blodbaserade markörer som kan spegla vad som händer i placentan. Med framtida studier som följer mödrar över tid och jämför deras blod med placentavävnad kan detta tillvägagångssätt bidra till att bygga tidiga, icke‑invasiva screenverktyg och mer skräddarsydda närings‑ eller medicinska strategier för att skydda sårbara graviditeter.
Citering: Xie, X., Li, Z., Xiao, Q. et al. Heterogeneous graph neural networks reveal molecular mechanisms of folate deficiency in placental insufficiency through multiomics integration. Sci Rep 16, 8417 (2026). https://doi.org/10.1038/s41598-026-38288-y
Nyckelord: placentainsufficiens, folatbrist, grafneurala nätverk, multiomik, graviditetskomplikationer