Clear Sky Science · sv
Hämning av PERK dämpar multipla program för celldöd genom aktivering av Nrf2/HO-1 vid diabetisk retinopati med integrerad proteomik och funktionell validering i HRECs
Varför det är viktigt att skydda synen vid diabetes
För miljontals människor med diabetes är en av de mest fruktade komplikationerna den gradvisa synförlusten som kallas diabetisk retinopati. Denna skada på det ljuskänsliga vävnadsskiktet längst bak i ögat börjar ofta tyst, långt innan symtom uppträder. Studien bakom den här artikeln undersöker vad som faktiskt dödar de små blodkärlscellerna som håller näthinnan frisk — och prövar ett nytt sätt att skydda dem. Genom att förstå och dämpa cellernas ”stressreaktioner” som triggas av högt blodsocker hoppas forskarna kunna bromsa eller till och med förebygga blindhet hos personer med diabetes.
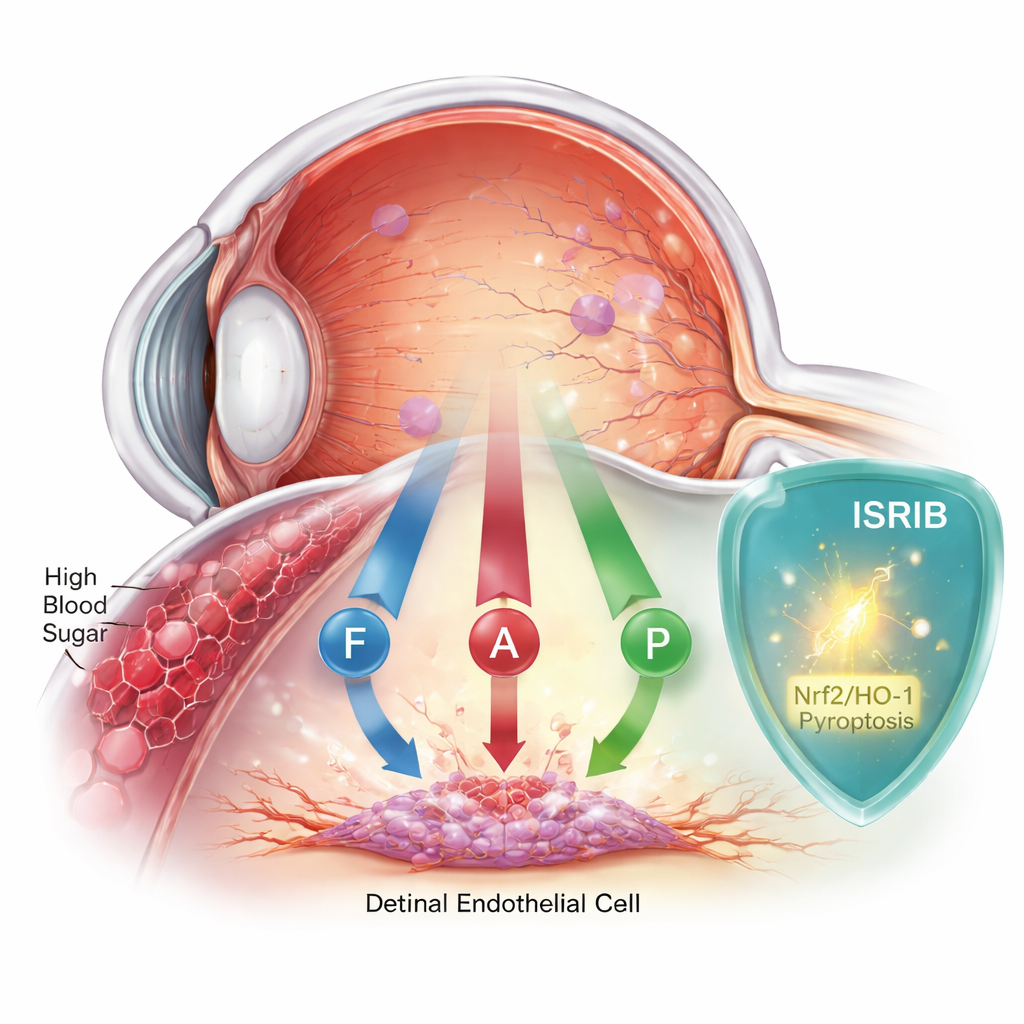
När blodsocker tyst skadar ögat
Diabetisk retinopati börjar när högt blodsocker skadar det känsliga innerlagret av de retinala blodkärlens endotelceller. Dessa celler bildar en barriär som håller näthinnan försörjd och skyddad. Under lång tid trodde forskare att en enda form av celldöd, kallad apoptos, främst låg bakom skadan. Men växande bevis pekar på att bilden är mer komplex. Forskarna fokuserade på humana retinala endotelceller odlade i laboratoriet och exponerade dem för sockernivåer liknande de som ses vid dåligt kontrollerad diabetes, och följde cellernas respons över två dagar.
Tre sätt som celler kan dö samtidigt
Med hjälp av en kraftfull proteomikmetod för att mäta proteiner upptäckte forskarna att högt socker störde hundratals proteiner, särskilt de som är involverade i stressreaktioner, ämnesomsättning och järnhantering. Uppföljande tester visade att cellerna inte bara dog på ett sätt, utan tre: klassisk programmerad celldöd (apoptos), en inflammationskopplad, ”brinnande” form (pyroptos) och en nyare järnberoende form kallad ferroptos. Markörer för oxidativ skada, järnöverskott och uttömda antioxidanter ökade, medan skyddande enzymer minskade. Tillsammans målade dessa förändringar upp en bild av celler överväldigade av stress, inflammation och giftig ansamling av reaktiva molekyler.
En stressbrytare i kärnan av problemet
Forskarna riktade sedan in sig på en nyckelsensor för stress inne i cellerna kallad PERK, som sitter på membranet till det endoplasmatiska retiklet, en struktur som hjälper till att veckla och bearbeta proteiner. Under höga sockernivåer blev PERK överaktivt, och fungerade som en fastnat nödlarm som fortsätter att tjuta. Detta verkade driva på alla tre dödsprogrammen. Samtidigt var ett naturligt försvarssystem som normalt hjälper celler hantera oxidativ skada — Nrf2/HO-1-antioxidantvägen — försvagat. Enkelt uttryckt: farosignalerna var uppvridna medan cellernas interna brandsläckare var nedvridna.
Sänka stressen, höja skyddet
För att se om de kunde bryta denna destruktiva cykel behandlade forskarna högsocker-exponerade celler med ISRIB, en liten molekyl som effektivt dämpar PERK:s stressignalering. Resultaten var påtagliga. ISRIB förbättrade cellöverlevnaden, minskade markörer för järn- och oxidativt relaterad skada och sänkte kemiska tecken på både apoptos och pyroptos. Samtidigt förstärkte det Nrf2/HO-1-försvarsvägen och hjälpte cellerna återställa sin antioxidantkapacitet. Ett separat läkemedel som specifikt blockerar ferroptos hade också effekt, men ISRIB utmärkte sig genom att lugna alla tre dödsfärdvägarna samtidigt istället för bara en.
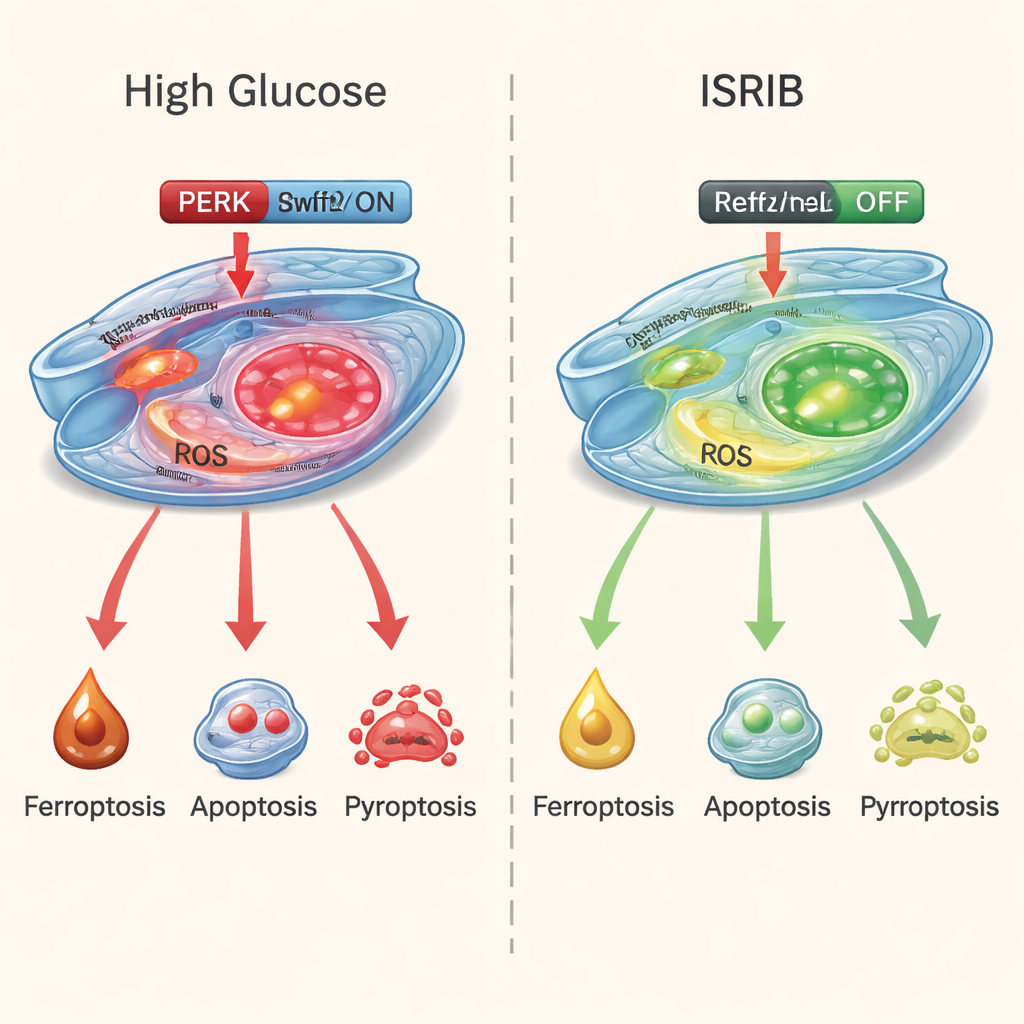
Vad detta kan innebära för personer med diabetes
Dessa resultat tyder på att tidig skada vid diabetisk retinopati inte orsakas av en ensam ”boven”, utan av en konvergens av flera självförstärkande dödsprogram driva av kronisk cellstress. Genom att vrida ner PERK-stressväljaren och återaktivera cellens egna skyddssystem kan läkemedel som ISRIB erbjuda ett mer enhetligt sätt att hålla retinala blodkärl vid liv. Även om dessa experiment gjordes i celler och ännu inte i patienter, pekar de mot framtida behandlingar som riktar sig mot stressreaktioner inne i ögat — vilket potentiellt kan lägga ett nytt skyddsskikt utöver blodsockerkontroll och dagens ögondroppar/injektioner för att bevara synen vid diabetes.
Citering: Xie, L., Zhang, X., Tian, M. et al. PERK inhibition attenuates multi-program cell death through Nrf2/HO-1 activation in diabetic retinopathy with integrated proteomics and functional validation in HRECs. Sci Rep 16, 7225 (2026). https://doi.org/10.1038/s41598-026-38213-3
Nyckelord: diabetisk retinopati, retinal celldöd, oxidativ stress, PERK-vägen, Nrf2 HO-1