Clear Sky Science · sv
Hämning av SHH‑vägen och samexperiment med astrocyter ger skilda responser i glioblastom och cancerstamceller
Varför hjärntumörer är så svåra att behandla
Glioblastom är en av de dödligaste hjärntumörerna, och även med kirurgi, strålning och cytostatika lever bara en liten andel patienter längre än fem år. En anledning är att dessa tumörer inte består av bara en celltyp. De innehåller en liten grupp särskilt motståndskraftiga ”cancerstamceller” som kan överleva behandling och bidra till att tumören växer tillbaka. Den här studien ställer en central fråga: hur svarar de olika tumörcellerna när en tillväxtdrivande signal blockeras, och hur påverkar närvaron av normala hjärnceller kallade astrocyter detta svar?
Tittar närmare på tumörens tuffaste celler
Forskarna arbetade med två huvudsakliga celltyper från en vanlig glioblastommodell: bulk‑tumörceller och en liten subpopulation märkta med ett protein kallat CD133, som beter sig som cancerstamceller. Dessa stamliknande celler delade sig långsammare, var mindre och rundare till formen och bildade tätare kluster än bulkcellerna. Teamet odlade också tumörceller tillsammans med astrocyter, de stjärnformade celler som hjälper till att upprätthålla frisk hjärnvävnad. Denna blandkultur efterliknar bättre den verkliga tumörmiljön, där cancerceller ständigt ”pratar” med sina grannar. 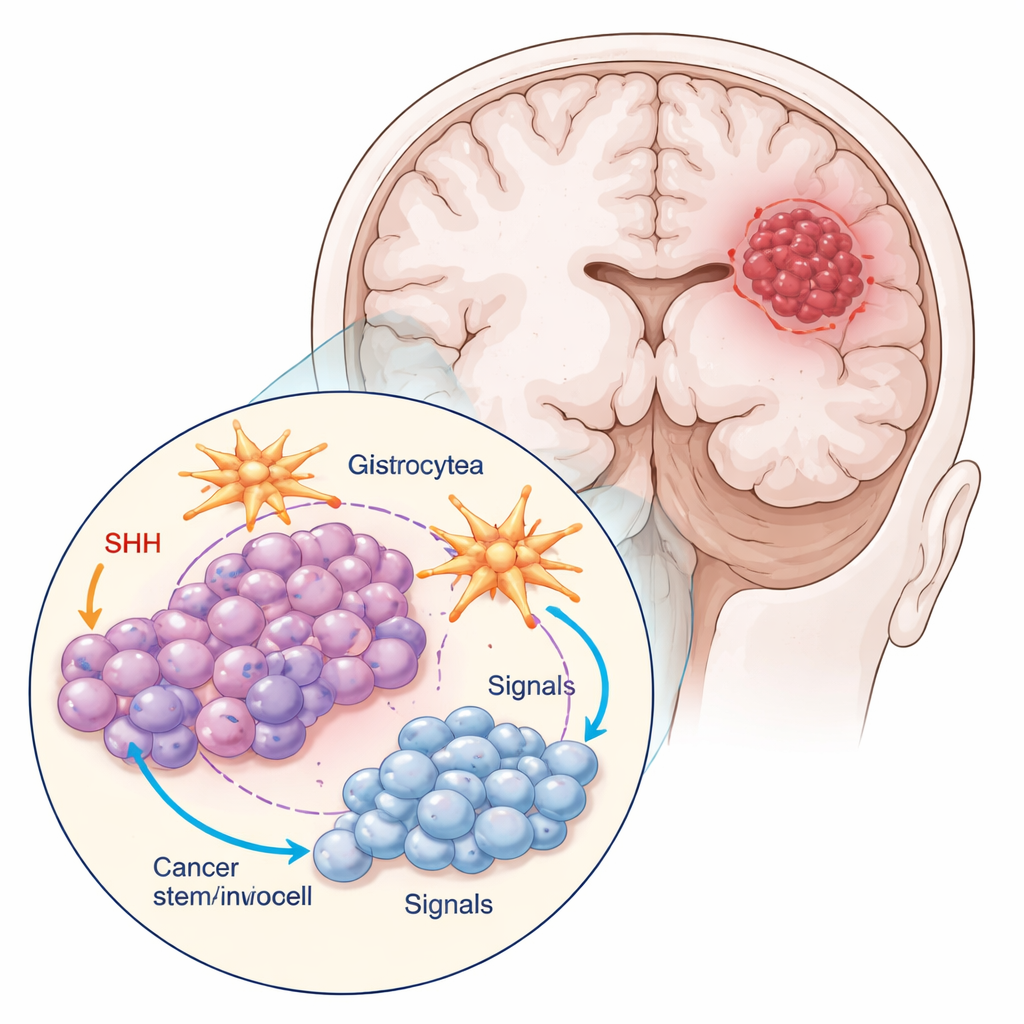
Blockera en utvecklingssignal som tumörer återanvänder
Många glioblastom, särskilt deras stamliknande celler, kapar en molekylär kommunikationsväg kallad Sonic Hedgehog (SHH), som normalt är aktiv under hjärnans utveckling. Gruppen använde cyklopamin, en förening som blockerar en nyckelkomponent i SHH‑vägen, för att se hur både bulk‑tumörceller och cancerstamceller reagerar. De mätte aktivitet i SHH‑relaterade gener och proteiner, hur snabbt cellerna gick igenom cellcykeln och hur ofta de genomgick programmerad celldöd (apoptos). Cyklopamin förändrade SHH‑signaleringen på ett sätt som starkt berodde på celltyp och om astrocyter fanns närvarande. Cancerstamcellerna producerade mest SHH‑signal när de odlades ensamma, men denna sekretion minskade när de odlades med astrocyter och exponerades för läkemedlet, vilket tyder på att omgivande hjärnceller kan dämpa tumörens kemiska ”självstöd”.
Hur grannskapet skiftar tillväxt och död
Bortom SHH i sig följde teamet andra gen‑nätverk som styr om celler fortsätter dela sig, stannar av eller börjar specialisera sig. I enkla kulturmodeller med bara tumörceller drev SHH‑blockad bulkceller mot ett stopp i ett sent delningsstadium (G2/M‑fasen), medan stamliknande celler tenderade att samlas tidigare, i vilofasen eller införing i cellcykeln (G0/G1). När astrocyter tillsattes förändrades dessa mönster: cancerstamcellerna, som tidigare varit mer quiescenta, försköts mot G2/M‑arrest, vilket antyder att en annan uppsättning ”bromsar” aktiveras i den blandade miljön. Forskarna såg också att signaler kopplade till cellöde och vävnadsbildning — såsom WNT-, BMP‑ och TGF‑β‑vägarna — var annorlunda inställda i bulkceller och stamliknande celler när astrocyter var närvarande, vilket betyder att mikromiljön kan luta cellerna mot antingen fortsatt stamliknande beteende eller en mer differentierad, mindre aggressiv status.
Utlösa celldöd i de mest resistenta cellerna
Studien undersökte vidare hur benäget cellerna var att genomgå apoptos. Genetiska avläsningar och ett DNA‑skade‑kännande test (TUNEL‑analys) visade att cyklopamin gynnade en ”extern” väg till celldöd, driven av ett protein kallat CASP8, särskilt i populationen av cancerstamceller. Intressant nog minskade den totala celldoden ibland i tumörceller odlade ensamma efter SHH‑blockad, vilket antyder att dessa celler kunde aktivera reservstrategier för överlevnad. Däremot, när stamliknande celler samexperimenterades med astrocyter, ökade cyklopamin markörer för apoptos, vilket indikerar att de omgivande hjärncellerna kan göra dessa annars tåliga celler mer sårbara när SHH‑signaleringen blockeras. 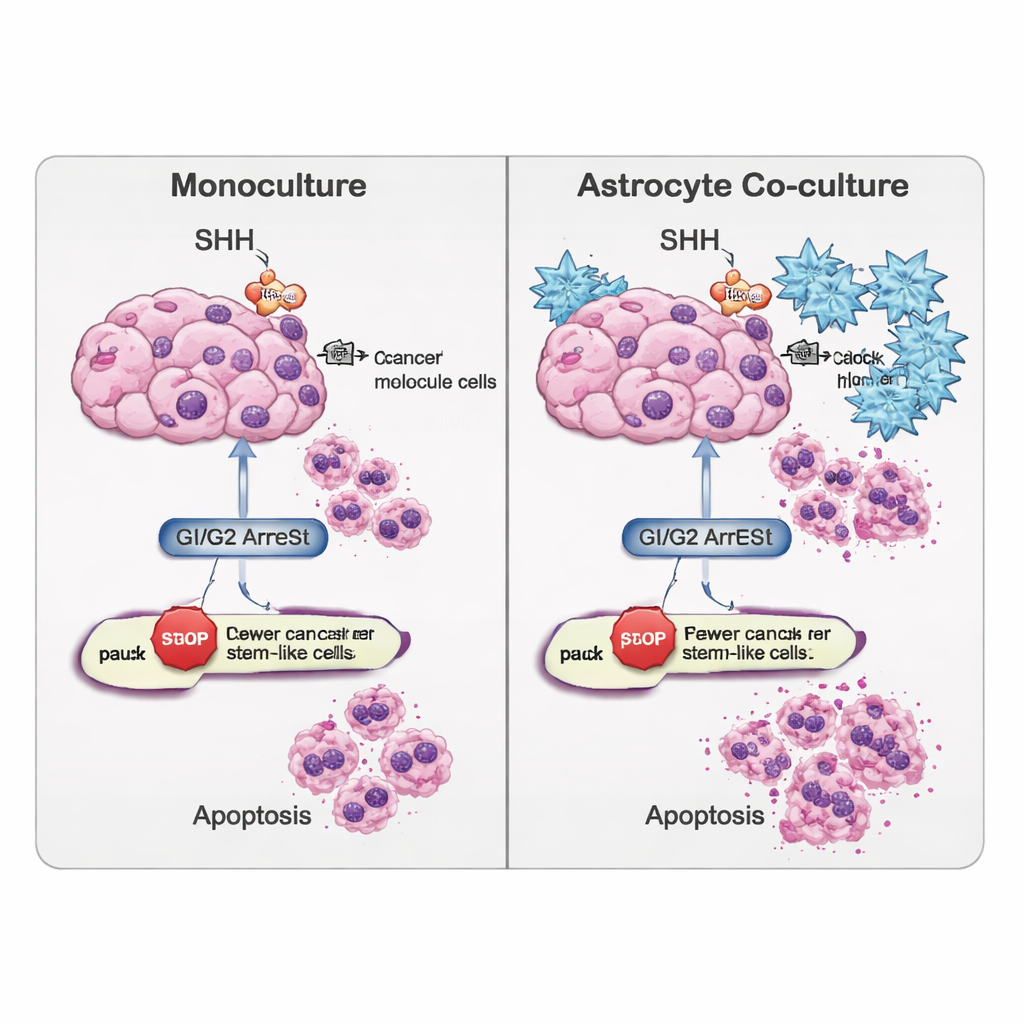
Vad detta innebär för framtida behandlingar av hjärncancer
För icke‑specialisten är huvudbudskapet att målinriktning av en enda tillväxtsignal i glioblastom inte räcker om vi ignorerar tumörens grannskap. Detta arbete visar att astrocyter — de normala celler som delar utrymme med tumören — kan kraftigt förändra hur både bulkcancer‑celler och cancerstamceller svarar på SHH‑hämning. Särskilt blev cancerstamcellerna mer benägna till cellcykelarrest och till en form av celldöd när astrocyter fanns närvarande. Författarna drar slutsatsen att läkemedel riktade mot SHH och närliggande vägar troligen fungerar bättre om de testas och så småningom används på sätt som speglar den verkliga hjärnmiljön, möjligen i kombination med andra behandlingar som angriper tumörens reservöverlevnadsstrategier. Kort sagt: att förstå och utnyttja ”samtalet” mellan tumörceller och deras grannar kan öppna mer precisa och hållbara strategier mot denna annars obevekliga cancer.
Citering: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Nyckelord: glioblastom, cancerstamceller, Sonic Hedgehog‑vägen, tumörmikromiljö, astrocyter