Clear Sky Science · sv
Integrerad metabolomik och 16S rRNA‑sekvensering avslöjar verkningsmekanismen för totala flavoner från Abelmoschus manihot (L.) Medic mot leverskleros
Blomkraft mot en ärrad lever
Leverskada i form av fibros är en tyst fara som långsamt kan leda till cirros och leversvikt. Modern medicin saknar fortfarande säkra, allmänt verksamma läkemedel för att stoppa eller vända denna process. Denna studie undersöker om naturliga föreningar från de ljusgula blommorna av Abelmoschus manihot — en traditionell kinesisk medicinalväxt redan använd vid njursjukdom — kan skydda levern mot långvarig toxisk skada, och hur de eventuellt gör det genom att påverka både kroppens kemi och mikroberna i tarmen.
En växande global leverutmaning
Hundratals miljoner människor världen över lever med kronisk leversjukdom orsakad av virus, alkohol, fettinlagring eller toxiner. När levern skadas upprepade gånger reagerar den genom att lägga ner ärrvävnad, ungefär som ett sår som aldrig läker helt. Med tiden kan denna fibros göra organet stelare, blockera blodflödet och utvecklas till cirros, en ledande dödsorsak relaterad till levern. Eftersom många olika utlösare kan driva denna skada samtidigt är forskare särskilt intresserade av växtbaserade blandningar som kan verka på flera mål på en gång, snarare än enskilda molekyler som bara påverkar en väg.
Test av ett traditionellt botemedel på möss
Gruppen fokuserade på de ”totala flavonerna” från Abelmoschus manihot (TFA) — en koncentrerad blandning av sju besläktade växtföreningar som tidigare visat antiinflammatoriska och antioxidativa egenskaper. De använde en väletablerad modell där upprepad exponering för industrikemikalien koltetraklorid (CCl4) orsakar kronisk leverskada och ärrbildning liknande mänsklig fibros. Hannmöss delades in i grupper: friska kontroller, CCl4‑skadade ”modell”möss, en standardläkemedelsgrupp och tre TFA‑dosgrupper. Efter veckors exponering för CCl4 behandlades djuren med TFA per os och undersöktes därefter vad gäller blod, levervävnad och tarminnehåll.
Bättre blodprover och friskare levervävnad
TFA gav tydliga skyddseffekter. Blodnivåerna av leverenzymen ALT och AST — kliniska indikatorer på leverskada — steg kraftigt hos möss som exponerats för CCl4, men föll med ungefär hälften hos djur som fick TFA. Mikroskopisk undersökning berättade samma historia: obehandlade fibrotiska leverer visade förvrängd arkitektur, döda celler, kraftiga kollageninlagringar och inflammation. TFA‑behandlade leverer hade färre ärrliknande ”pseudolobuler”, mindre kollagenfärgning och minskade tecken på celldöd. Markörer för oxidativ stress förbättrades också: antioxidativa försvar (SOD och GSH‑Px) ökade, medan skadliga biprodukter (MDA) sjönk. Centrala inflammatoriska budbärare, inklusive TNF‑α, IL‑6 och TGF‑β1, minskade också, liksom kemiska markörer för fibros såsom hydroxyprolin, kollagen IV och hyaluronsyra.
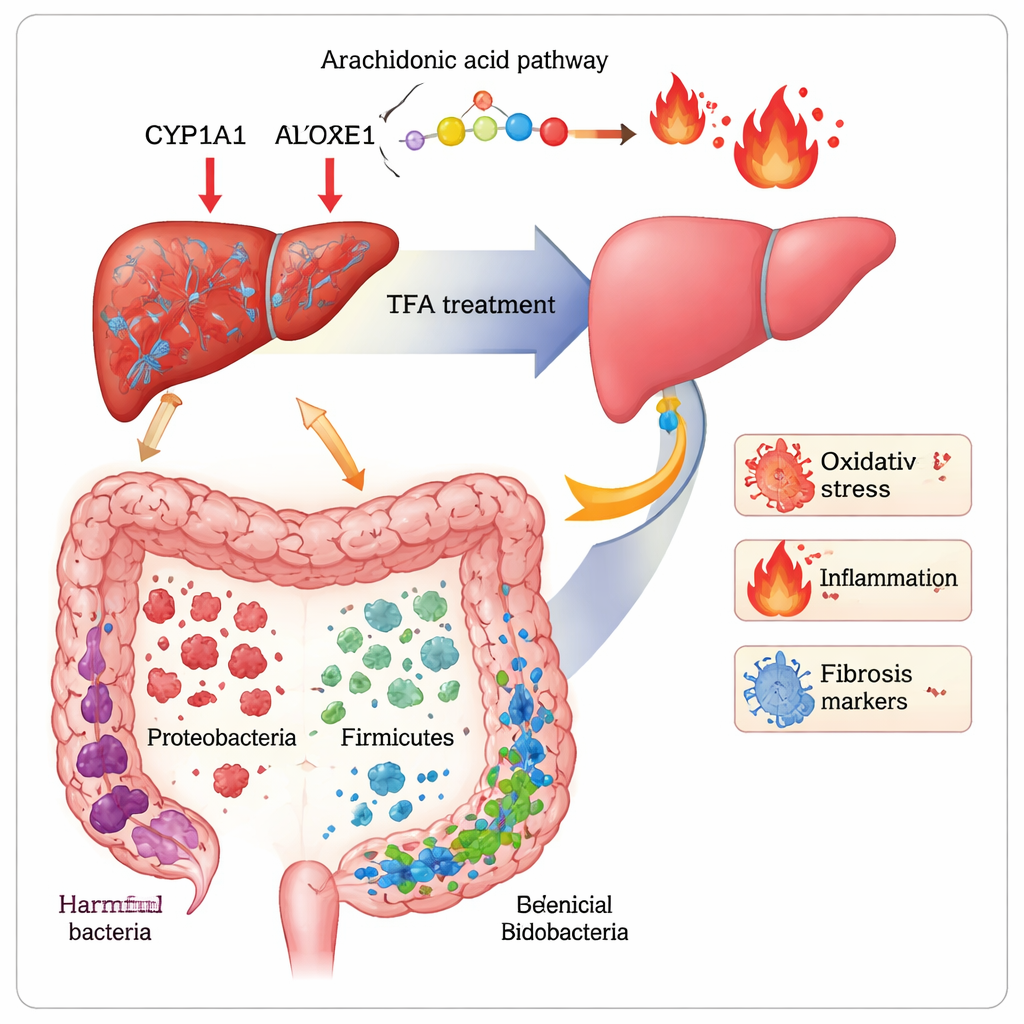
Återställning av kroppskemi och tarmbakterier
För att förstå hur TFA ger dessa fördelar kombinerade forskarna två kraftfulla verktyg: metabolomik, som profilerar hundratals småmolekyler i blodet, och 16S rRNA‑sekvensering, som kartlägger bakterietyper i tarmen. Hos de fibrotiska mössen var dussintals metaboliter som deltar i fettmetabolism och aminosyranedbrytning rubbade. TFA återställde delvis balansen i vägar kopplade till cellmembran (glycerofosfolipider), den humörrelaterade aminosyran tryptofan och en fettsyra kallad arakidonsyra som driver inflammatoriska signaler. Nivåerna av två arakidonsyraprodukter, 20‑HETE och 16(R)‑HETE — båda knutna till oxidativ stress och fibros — pressades tillbaka mot normalvärden. I levern minskade TFA rikligheten av tre enzymer (CYP1A1, CYP2E1, ALOX15) som bidrar till att skapa dessa skadliga molekyler. Samtidigt störde CCl4 tarmmikrobiotan, minskade fördelaktiga grupper som Firmicutes, Lactobacillus och Bifidobacterium och lät potentiellt skadliga Proteobacteria blomma ut. TFA vände mycket av denna förändring, ökade mångfalden och återställde "vänliga" bakterier kopplade till bättre barriärfunktion och lägre inflammation.
En multi‑målstrategi längs tarm–lever‑axeln
Genom att koppla bakterieändringar till blodkemikalier och sjukdomsmarkörer antyder studien att TFA verkar längs ”tarm–lever‑axeln” — den aktiva motorvägen av signaler, näringsämnen och toxiner som färdas från tarmen till levern. Skadliga bakterier och deras produkter verkar sammanfalla med högre inflammation och ärrbildning, medan fördelaktiga mikrober korrelerar med friskare metabola profiler och mindre fibros. TFA verkar skjuta detta hela system tillbaka mot balans: det stärker antioxidativa försvar, lugnar inflammatoriska vägar som drivs av arakidonsyra, omformar mikrobiell sammansättning i tarmen och mildrar i slutändan ärrbildningen i levern.
Vad detta kan betyda för framtida behandlingar
För icke‑specialister är huvudbudskapet att ett blomextrakt som länge använts i traditionell medicin visade verklig potential i ett modernt, rigoröst test av kronisk leverskleros. Hos möss gjorde TFA mer än att bara skydda leverceller — det dämpade giftig kemi och skadliga tarmmikrober samtidigt. Även om dessa resultat ännu inte bevisar nytta hos människor, och endast erhölls i handjur av ena könet med en typ av leverskada, framhäver de en potentiell multi‑målsterapi som samarbetar med kroppens egna nätverk snarare än att angripa en enda molekyl. Med vidare prövningar skulle sådana växt‑baserade flavoner kunna bli en del av ett bredare verktygsfält för att bromsa eller till och med vända leverskleros.
Citering: Li, D., Ge, H., Zhang, Y. et al. Integrated metabolomics and 16S rRNA sequencing reveal the mechanism of total flavones of Abelmoschus manihot (L.) Medic against liver fibrosis. Sci Rep 16, 7342 (2026). https://doi.org/10.1038/s41598-026-38192-5
Nyckelord: leverskleros, tarmmikrobiota, metabolomik, flavonoider, traditionell kinesisk medicin