Clear Sky Science · sv
INHBA: ett mitokondrierelaterat pan-celldöd-genkopplat till prognos och immunitet vid OSCC
Varför detta är viktigt för munhålecancer
Oral skivepitelcancer, en vanlig form av munhålecancer, kan beröva människor grundläggande förmågor som att tala, äta och till och med le bekvämt. Trots kirurgi, strålning och cytostatika drabbas många patienter fortfarande av återfall och dålig långtidsöverlevnad. Denna studie tar ett nytt grepp på munhålecancer genom att fokusera på hur en enskild gen, kallad INHBA, bidrar till att forma celldöd, tumörens omgivning av stödjeceller och framgången eller misslyckandet för moderna behandlingar som immunoterapi.
En närmare titt på en dödlig munhålecancer
De flesta huvud- och halscancerformer börjar i munhålans slemhinna, och mer än 90 % av dessa är oral skivepitelcancer (OSCC). Globalt ökar både insjuknande och dödlighet i OSCC, och förväntas stiga med ungefär 40 % fram till 2040. Standardvården bygger på kirurgi i kombination med strålning och kemoterapi, men många tumörer är behandlingsresistenta och återkommer. Nyare immunoterapier, som syftar till att väcka kroppens egna försvar, hjälper bara en bråkdel av patienterna. För att gå bortom försök-och-fel behövs bättre förståelse för vilka gener som driver OSCC och hur de samverkar med immunsystemet.
Celldöd, kraftverk och en ny genkategori
Våra celler är programmerade att dö på flera noggrant kontrollerade sätt, inklusive processer med namn som apoptos, autofagi, ferroptos med flera. I cancer är dessa dödsprogram ofta omkopplade så att tumörceller överlever när de borde dö. Forskarna bakom denna studie fokuserade på en bred grupp som de kallar “pan-celldöd”-gener — gener som sitter i korsningen mellan olika dödssignaler — och begränsade vidare till de som är kopplade till mitokondrierna, cellernas små kraftverk. Genom att kombinera stora publika cancer-dataset med en specialiserad katalog över mitokondriella gener definierade de en uppsättning “mitokondrie-associerade pan-celldöd-gener” och sökte efter dem som starkast kopplades till OSCC-beteende och patientutfall.
INHBA hittad bland många misstänkta
Med avancerad statistik och nio olika maskininlärningsalgoritmer siktade forskarna igenom tusentals gener och identifierade 19 mitokondriella pan-celldöd-gener med starka kopplingar till prognos vid OSCC. Bland dessa utmärkte sig INHBA. Dess aktivitet var konsekvent högre i tumörprover än i normalt munslemhinnevävnad och var kopplad till sämre överlevnad både i OSCC och i den bredare gruppen huvud- och halscancer. När tumörer delades upp i hög- och låg-INHBA-grupper visade de med högre nivåer mer aggressiva biologiska signaler, inklusive vägar relaterade till vävnadsinvasion, blodkärlsbildning och mitokondriell stress. Laboratorietester på patientprover bekräftade att INHBA:s budbärare (mRNA) verkligen var förhöjda i verkliga tumörer.
Den dolda rollen hos stödjeceller kring tumören
För att förstå var INHBA är mest aktiv använde teamet single-cell RNA-sekvensering och spatial transkriptomik, tekniker som kartlägger genaktivitet i individuella celler och över vävnadssnitt. De fann att INHBA inte huvudsakligen produceras av cancercellerna själva, utan av cancerassocierade fibroblaster — stödjeceller som omformar vävnad och formar den immuna miljön. En särskild undergrupp, kallad myofibroblastiska CAFs, visade särskilt höga INHBA-nivåer. Detaljerade kommunikationskartor antydde att INHBA-rika fibroblaster kommunicerar intensivt med immunceller och tumörceller och bidrar till att skapa en immunosuppressiv, ärrliknande nisch runt cancern. Denna mikromiljö verkar främja tumörtillväxt och kan dämpa vissa former av immunoterapi.
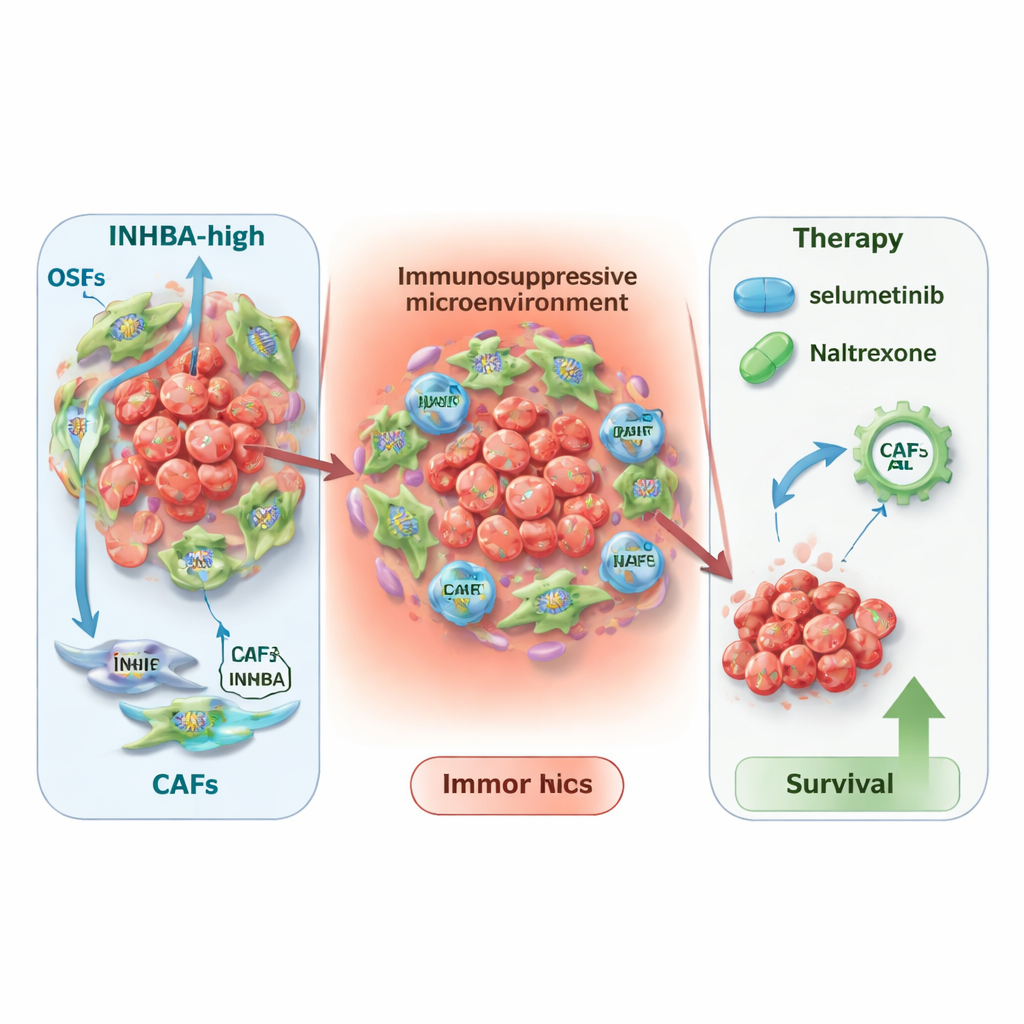
Nya behandlingsvinklar och bredare påverkan
Med vetskapen om att INHBA markerar en mer farlig tumöromgivning frågade forskarna hur detta kan vägleda terapi. Hos patienter som fick immunoterapi var låga INHBA-nivåer kopplade till bättre utfall med vanliga läkemedel som riktar sig mot PD-L1 eller CTLA4, medan höga INHBA-nivåer föreföll förutsäga bättre nytta av CAR-T-cellsterapier. Genom att undersöka två stora databaser för läkemedelssvar lyfte de också fram två befintliga läkemedel — selumetinib och naltrexon — som särskilt lovande i tumörer med hög INHBA. Datorbaserade modeller visade att båda läkemedlen kan binda tätt till INHBA-proteinet, vilket antyder en möjlig direkt effekt. Slutligen visade en pan-cancer-analys att INHBA är förhöjt och kopplat till dålig överlevnad i många andra tumörtyper, vilket tyder på att dess betydelse sträcker sig långt bortom munhålecancer.
Vad detta betyder för patienter
Enkelt uttryckt identifierar denna studie INHBA som en “master-switch”-gen som hjälper farliga munhåletumörer att växa, sprida sig och undkomma immunsystemet, i hög grad genom att verka via specialiserade stödjeceller snarare än enbart genom cancercellerna själva. Att mäta INHBA i tumörer kan hjälpa läkare att identifiera högriskpatienter, förutsäga vem som kommer att gynnas av olika typer av immunoterapi och välja riktade läkemedel som kan fungera bättre i detta sammanhang. Eftersom INHBA spelar en liknande skadlig roll i flera andra cancerformer kan terapier som riktar sig mot denna gen och dess fibroblast-partners potentiellt gynna ett brett spektrum av patienter och föra vården närmare precisionsanpassad behandling.
Citering: Zhang, X., Sun, M., Qiu, T. et al. INHBA: a mitochondrial-related pan-cell death gene associated with the prognosis and immunity of OSCC. Sci Rep 16, 7642 (2026). https://doi.org/10.1038/s41598-026-38131-4
Nyckelord: oral skivepitelcancer, INHBA, tumörmikromiljö, cancerassocierade fibroblaster, immunoterapi