Clear Sky Science · sv
Nanopartiklar av serumalbumin från nöt förbättrar bakteriofagstabilitet och antimikrobiell aktivitet mot Pseudomonas aeruginosa
Varför det är viktigt att skydda nyttiga virus
När antibiotikaresistensen ökar börjar läkarna få ont om effektiva metoder för att behandla farliga infektioner. En enveten bov är Pseudomonas aeruginosa, en bakterie som ofta infekterar lungorna hos människor med nedsatt försvar och som kan stå emot många läkemedel. Denna studie undersöker en kreativ strategi: använda vänliga virus som angriper bakterier, så kallade bakteriofager, och skydda dem inuti pyttesmå proteinsfärer gjorda av ett vanligt blodprotein, bovint serumalbumin (BSA). Målet är att hålla dessa virus stabila och aktiva tillräckligt länge för att bättre bekämpa svåra lunginfektioner.
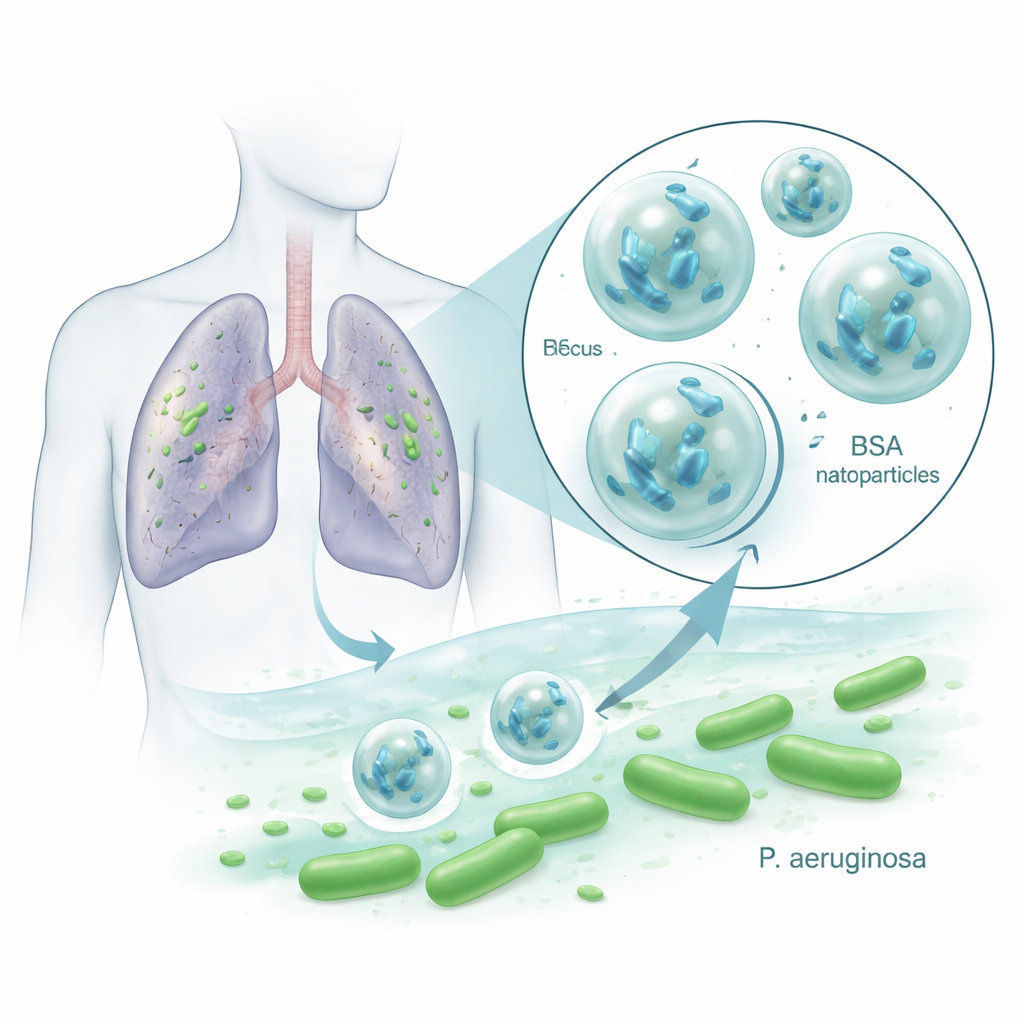
Små allierade mot besvärliga lungbakterier
Pseudomonas aeruginosa är ökänd på sjukhus eftersom den är motståndskraftig mot flera antibiotika och bildar slemmiga biofilmer som skyddar den från behandling. Bakteriofager, eller fager, är virus som infekterar och spränger specifika bakterier medan de i stort sett lämnar humana celler och nyttiga mikrober orörda. De kan föröka sig där deras bakteriella värd finns, vilket gör dem till ett lockande komplement eller alternativ till antibiotika. Men fager är ömtåliga: värme, sur miljö, enzymer och immunförsvaret kan snabbt göra dem inaktiva, vilket har begränsat deras framgång i verkliga patienter. Forskarna undersökte om inkapsling av en Pseudomonas‑dödande fag kallad VAC1 i BSA‑nanopartiklar kunde skydda den och göra behandlingarna mer effektiva.
Bygga ett skyddande proteinskal
Teamet var först tvungna att utforma en partikel som inte skulle skada fagen. De testade vanliga lösningsmedel som används för att forma BSA‑nanopartiklar och fann att etanol och metanol förstörde VAC1, medan aceton inte gjorde det, så de använde aceton i sin process. De blandade fagen med en BSA‑lösning och tillsatte sedan försiktigt aceton för att få proteinet att klumpa ihop sig till nanoskaliga sfärer, stabiliserade med ett tvärbindande kemiskt ämne. Dessa fagfyllda partiklar, kallade NPPha, hade i genomsnitt ungefär 220 nanometers diameter — mycket mindre än en mänsklig cell — och fångade över 95 % av fagen inuti. Elektronmikroskopbilder visade oregelbundet formade BSA‑partiklar med tätare områden som sannolikt motsvarade fag, och tester bekräftade att aktiva virus långsamt frigjordes under minst två dagar i kroppstemperatur utan att förlora sin infektivitet.
Starkare bakteriedödande effekt i laboratoriet
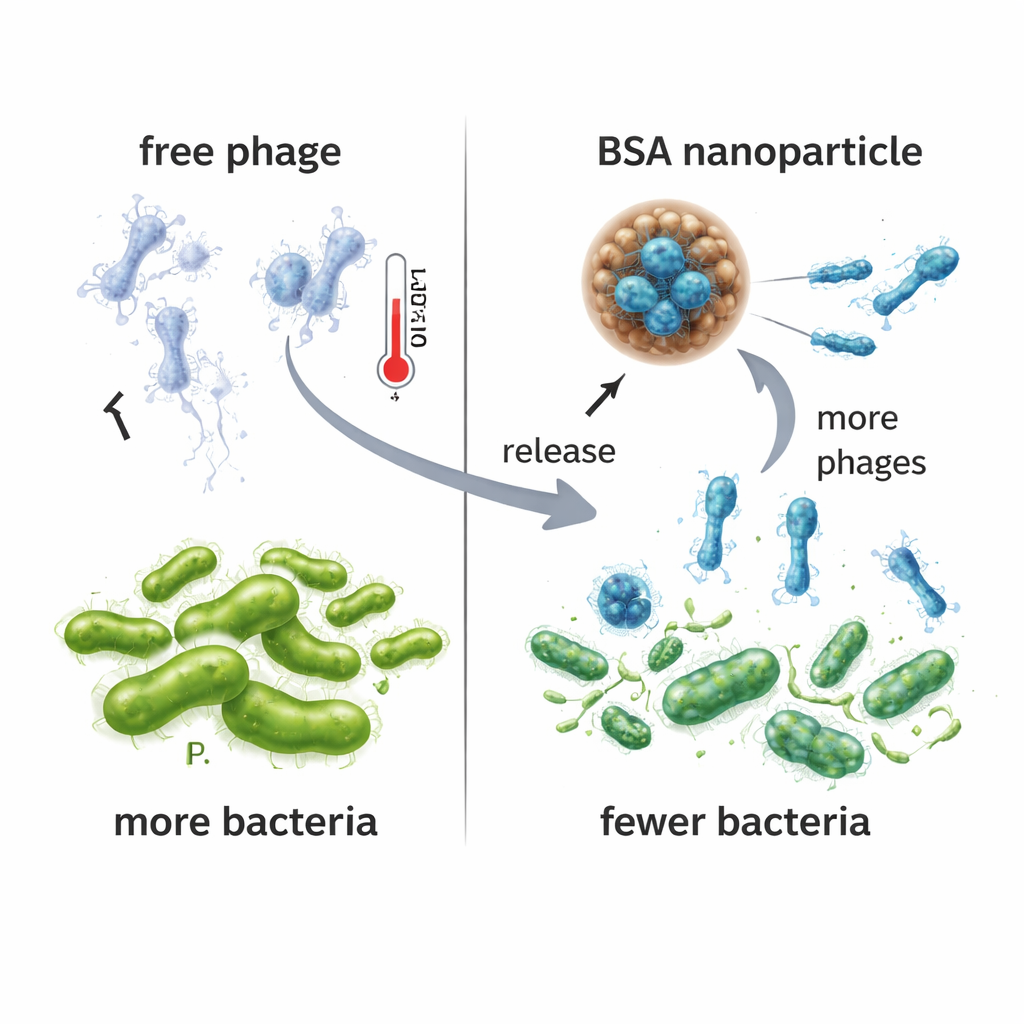
Forskarna jämförde sedan hur väl fri VAC1 och NPPha kontrollerade Pseudomonas i flytande odling. När bakterier exponerades för NPPha undertrycktes deras tillväxt mycket starkare än vid samma mängd fag given ensam eller tillsammans med tomma nanopartiklar. Under 24 timmar producerade kulturer behandlade med NPPha ungefär hundratusen gånger fler nya fagpartiklar än kulturer behandlade med fri VAC1, vilket tyder på att den jämna frisättningen från nanopartiklarna skapade en mer uthållig virus‑bakteriekamp. Viktigt är att BSA‑nanopartiklarna — vare sig fyllda med fag eller tomma — inte skadade människoceller av leverursprung i toxicitetstester, vilket talar för deras potentiella säkerhet som leveransfordon. Stabilitetsexperiment vid 37 °C visade att fri fag snabbt förlorade aktivitet inom två dagar, medan fag inneslutna i NPPha förblev infektiva i upp till fem dagar.
Test av metoden i infekterade möss
För att se om dessa fördelar gick igen i levande djur använde teamet en musmodell för akut Pseudomonas‑lunginfektion. Mössen infekterades via näsan och behandlades en timme senare med NPPha, fri VAC1, tomma nanopartiklar eller en saltlösning. I denna mycket svåra modell dog alla djur, oavsett behandling, inom 12 timmar, så överlevnaden förbättrades inte. När forskarna däremot undersökte lungorna fann de att möss som gavs NPPha hade färre bakterier och var mer benägna att fortfarande ha påvisbar fag än de som behandlats med fri VAC1. Vävnadssnitt från NPPha‑behandlade lungor visade mindre strukturell skada, tunnare väggar mellan luftblåsor och minskad ansamling av inflammatoriska celler jämfört med andra infekterade grupper, vilket indikerar att infektionen dämpades något även om det inte räckte för att rädda djuren under dessa hårda förhållanden.
Vad detta betyder för framtida infektionsbehandlingar
För icke‑specialister är huvudbudskapet att inkapsling av bakteriofager i pyttesmå proteinbaserade bubblor kan hålla dem vid liv och potenta längre, vilket hjälper dem att bättre angripa svårbehandlade bakterier som Pseudomonas aeruginosa. I odlingar och i mushlungor ökade BSA‑nanopartiklarna fagtalen, minskade bakterietillväxten och reducerade lungskador, även om de ännu inte förhindrade död i en mycket aggressiv infektionsmodell. Arbetet tyder på att albumin‑nanopartiklar erbjuder ett enkelt, kostnadseffektivt och till synes säkert sätt att stabilisera terapeutiska fager. Med förfinad dosering, timing och kanske användning i mindre extrema eller mer kroniska infektioner skulle sådana nanopackade fager kunna bli ett värdefullt verktyg vid sidan av antibiotika i kampen mot multiresistenta bakterier.
Citering: Cunha, G.A.d., Marangoni, G.S., Durante, M.F.R. et al. Bovine serum albumin nanoparticles improve bacteriophage stability and antimicrobial activity against Pseudomonas aeruginosa. Sci Rep 16, 7146 (2026). https://doi.org/10.1038/s41598-026-38106-5
Nyckelord: fagterapi, nanopartiklar, Pseudomonas aeruginosa, antibiotikaresistens, lunginfektion