Clear Sky Science · sv
Obinutuzumab orsakar lysosomal destabilisering via sfingomyelin‑beroende hämning av TRPML2
Varför den här antikroppsberättelsen är viktig
För många med B‑cellslymfom har moderna antikroppsbaserade läkemedel förvandlat en tidigare i stort sett alltid dödlig diagnos till en behandlingsbar sjukdom. Men inte alla antikroppar är likadana: vissa dödar cancerceller kraftfullare och mer tillförlitligt än andra. Denna artikel undersöker varför ett sådant läkemedel, obinutuzumab, är bättre på att direkt döda lymfomceller än sin föregångare rituximab, genom att zooma in på en oväntad förövare djupt inne i cellen — cellens egna återvinningscentraler, lysosomerna, och en känslig balans av fetter och jonkanaler i deras membran.
Från ytligt mål till intern självförstöring
Både rituximab och obinutuzumab känner igen samma mål på B‑celler, ett protein som kallas CD20. Men författarna visar att obinutuzumab tas upp i cellen mycket snabbare och mer effektivt. När antikropp–receptorkomplexen bundit CD20 på cancercellens yta dras de in genom endocytos och levereras till sura compartment, inklusive lysosomer. Där utlöser obinutuzumab permeabilisering av lysosomala membranet: det normalt tåliga lysosomala membranet blir läckande, vilket tillåter matsmältningsenzymer som kathepsiner att läcka ut i cytosolen och starta dödsprogram i cellen. Förändringar i salt‑ och vattenbalansen i dessa compartment, som får lysosomer att svälla, visade sig kraftigt förstärka denna dödliga effekt.
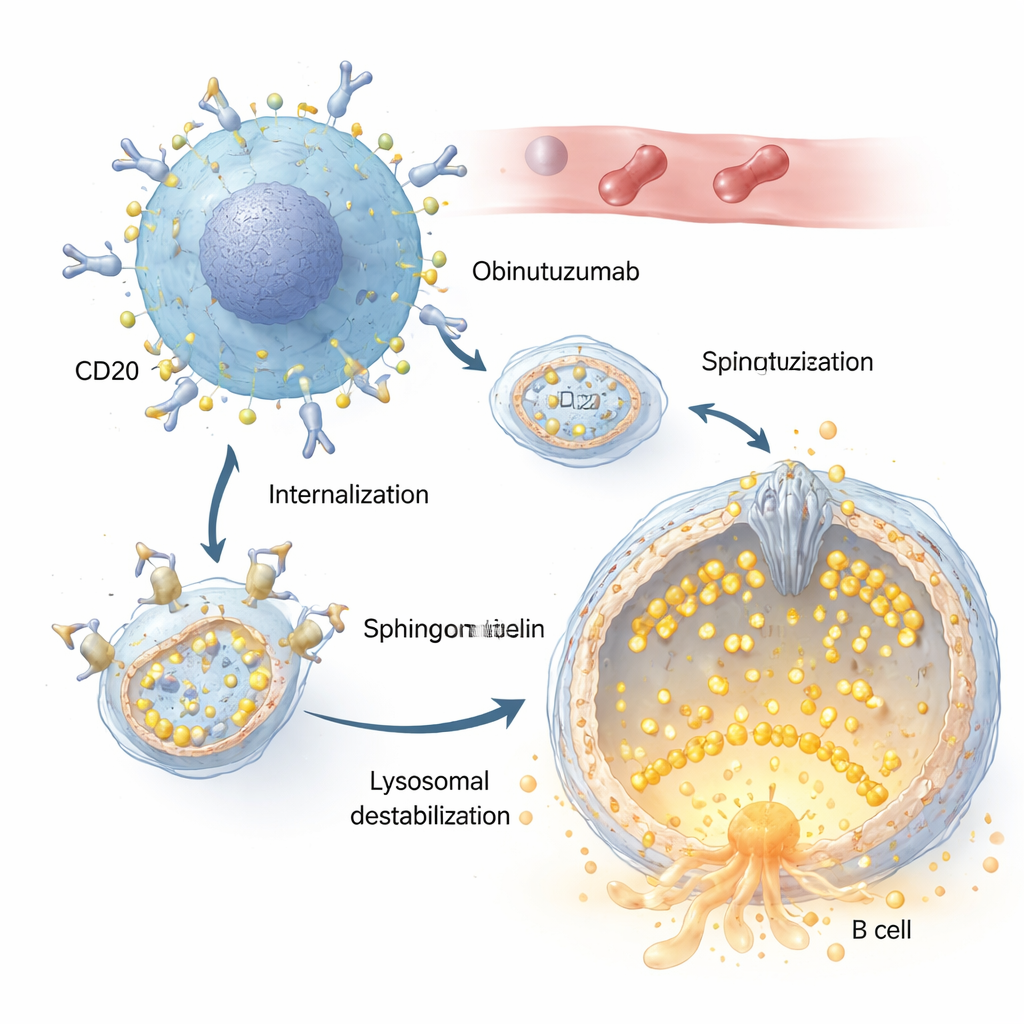
En liten grindvaktkanals roll
Centralt i berättelsen står TRPML2, en kalciumkanal inbäddad i lysosommembranet. Under normala förhållanden hjälper TRPML2 lysosomer att hantera mekanisk och osmotisk stress genom att släppa ut kalcium, vilket stödjer membranreparation, trafik och volymkontroll. Med hjälp av fluorescerande kalciumfärgämnen och konstruerade kalciumsensoriska varianter av TRPML2 visar forskarna att obinutuzumab snabbt slår av denna kanal: inom minuter efter behandling ger ett ämne som normalt öppnar TRPML‑kanaler inte längre någon kalciumpuls. Genetiska metoder som minskar TRPML2‑nivåer, eller småmolekylära hämmare som blockerar TRPML‑aktivitet, gör båda lymfomceller mer känsliga för obinutuzumab, vilket leder till mer lysosomal läckage och högre andel direkt celldöd.
Hur membranfetter påverkar balansen
Studien ställer sedan frågan vad som kopplar antikroppsupptaget till kanalavstängningen. Uppmärksamheten riktas mot sfingomyelin, ett lipid (fett) som är vanligt i cellmembran och som är känt för att störa TRPML‑kanaler. Med en fluorescerande probe som binder sfingomyelin finner författarna att vesiklar som innehåller obinutuzumab är rika på sfingomyelin när de når sura compartment, mycket mer än vesiklar med rituximab. När celler behandlas med sfingomyelinase, ett enzym som trimrar sfingomyelin, återställs TRPML2:s kalcium‑frisättande aktivitet även i närvaro av obinutuzumab. Under dessa förhållanden är lysosomer mindre benägna att läcka och färre celler dör, vilket starkt tyder på att ackumulerat sfingomyelin inaktiverar TRPML2 och förbereder lysosomer för ruptur.
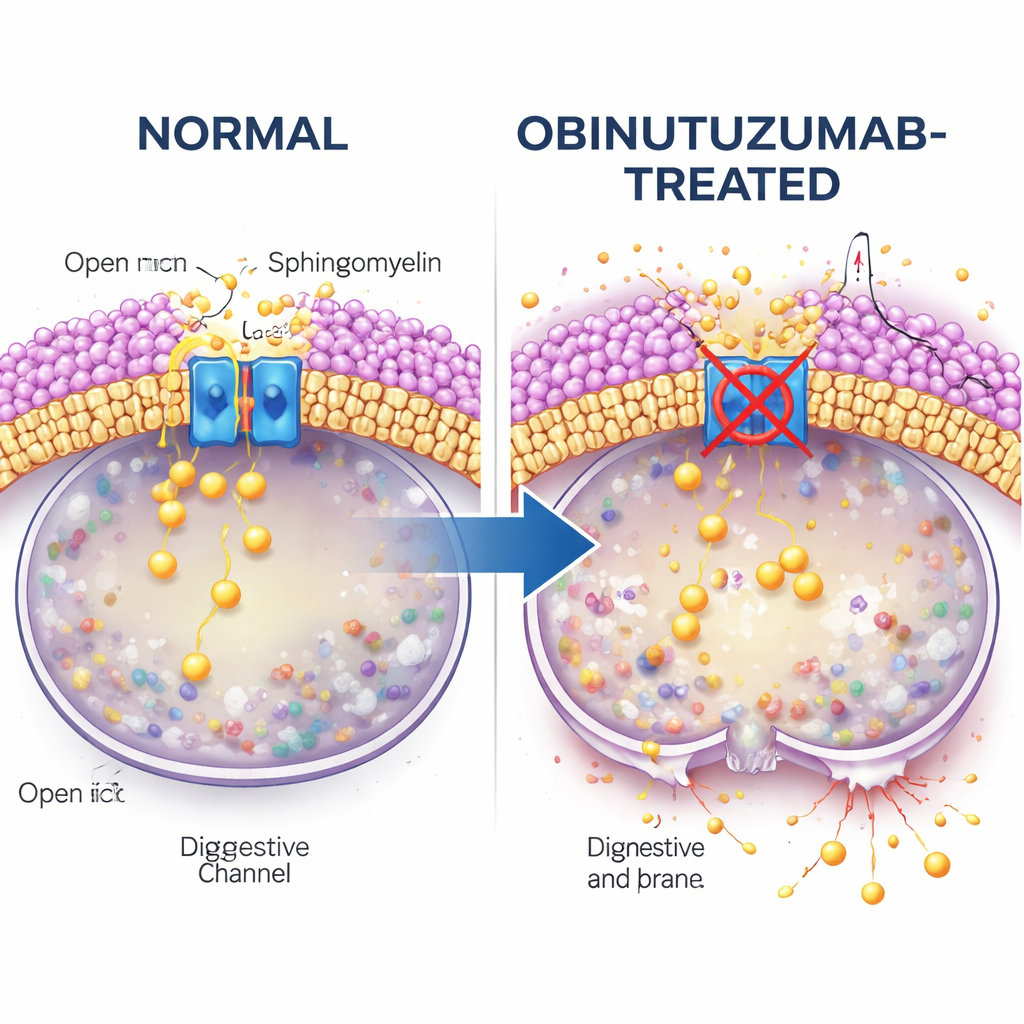
Transportvägar och kolesterolkontroller
Den väg obinutuzumab tar in i cellen spelar också roll. Elektronmikroskopi och pH‑känslig antikroppsmärkning visar att obinutuzumab lämnar cellmembranet och går in i intracellulära vesiklar snabbare än rituximab. När forskarna stör specifika upptagsvägar finner de att blockering av en kolesterolberoende form av endocytos (med ett ämne som heter filipin) förhindrar att obinutuzumab stänger av TRPML2, och delvis minskar lysosomala skador och celldöd. Andra endocytoshämmare har inte denna skyddande effekt. Detta pekar mot en specialiserad, kolesterol‑ och sfingomyelinrik väg som levererar obinutuzumab till lysosomer på ett sätt som möjliggör TRPML2‑hämning och efterföljande membrandestabilisering.
Vad detta betyder för framtida cancerbehandlingar
Enkelt uttryckt visar arbetet att obinutuzumab dödar B‑cellslymfom så effektivt eftersom det tvingar deras lysosomer in i ett ömtåligt tillstånd. Genom att driva antikropp–CD20‑komplex in i sfingomyelinrika compartment stänger läkemedlet indirekt av en skyddande kalciumkanal, TRPML2. När den skyddsmekanismen försvinner är lysosomer mer benägna att brista under stress och släppa ut frätande enzymer som bryter ned cancercellen inifrån. Att förstå denna lipid–jonkanal‑axel förklarar inte bara varför obinutuzumab överträffar rituximab; det föreslår också nya strategier för att göra antikroppsbehandlingar kraftfullare — till exempel genom att kombinera dem med läkemedel som förändrar sfingolipider eller ökar TRPML2‑aktivitet för att finjustera hur och när tumörcellers lysosomer självförstörs.
Citering: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Nyckelord: obinutuzumab, B‑cellslymfom, lysosom, sfingomyelin, TRPML2