Clear Sky Science · sv
Kronisk NH4Cl‑belastning förbättrar glukostolerans utan att förändra insulinkänsligheten hos möss
Varför syra‑bas‑balans spelar roll för blodsocker
Personer med kronisk njursjukdom utvecklar ofta ett tillstånd som kallas metabolisk acidos, där blodet blir något mer surt än normalt. Läkare ser vanligtvis detta som skadligt, delvis därför att korta episoder av acidos är kända för att försämra blodsockerkontrollen. Den här studien vänder dock på den idén: hos möss förbättrade en långvarig, mild acidos faktiskt kroppens förmåga att hantera socker, utan att hormonet insulin fungerade bättre eller sämre. Att förstå denna överraskande vändning kan så småningom hjälpa till att förfina behandlingar för både njursjukdom och typ 2‑diabetes.
En långvarig syrabelastning hos möss
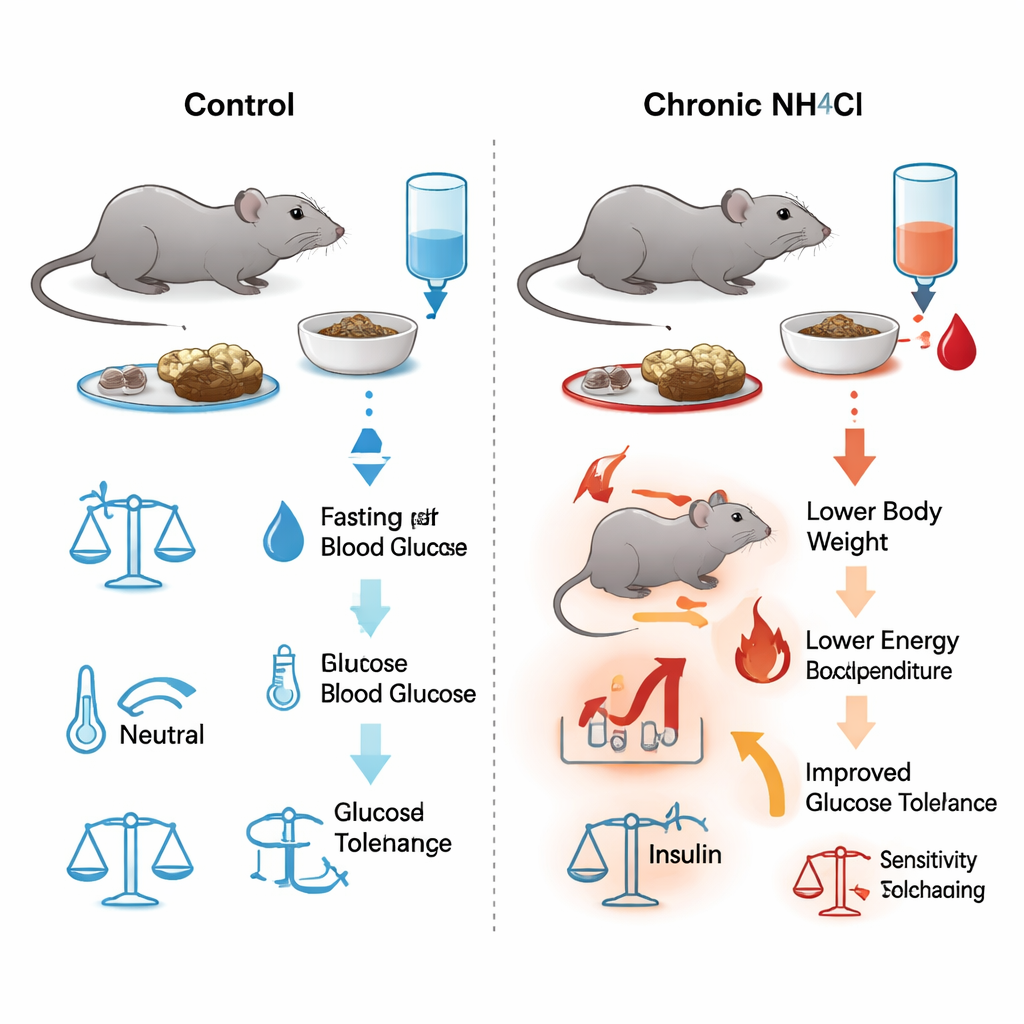
Forskarna gav hanmöss dricksvatten innehållande ammoniumklorid, ett salt som lätt acidifierar blodet, i upp till sex månader. Denna behandling efterliknar den kroniska syrabelastning som ses vid njursjukdom. Blodprover bekräftade en bestående, mild metabolisk acidos: lägre pH och bikarbonat, högre klorid och i övrigt stabila njurrelaterade mått såsom urea och hematokrit. Trots att de åt och drack lika mycket eller mer än obehandlade möss slutade de syrabelastade djuren att gå upp i vikt efter ungefär två månader. Detaljerade mätningar i metabola burar visade att dessa möss förbrände mer energi totalt, hade mindre mager (muskelrik) massa och bar relativt mer fett, vilket pekar på en högre metabol kostnad för att leva under kronisk acidos.
Bättre blodsockerkontroll utan extra insulinhjälp
Teamet testade upprepade gånger hur väl mössen rensade ut socker från blodet genom att injicera glukos och följa blodnivåerna över tid. Redan en vecka efter att den syrabildande drycken påbörjats sänkte de behandlade mössen sitt blodsocker snabbare än kontrollerna, och denna fördel kvarstod vid många tidpunkter upp till 180 dagar. Fastande blodsocker var konsekvent lägre i den acidotiska gruppen. När forskarna mätte insulin i blodet under dessa tester var nivåerna dock desamma i båda grupperna. Separata tester där möss gavs insulin direkt visade också att deras övergripande känslighet för insulin var oförändrad. Med andra ord förbättrade kronisk acidos glukostoleransen utan att kräva att bukspottkörteln producerade mer insulin eller att vävnaderna svarade starkare på det.
Förskjutning av var och hur socker tillverkas och förloras
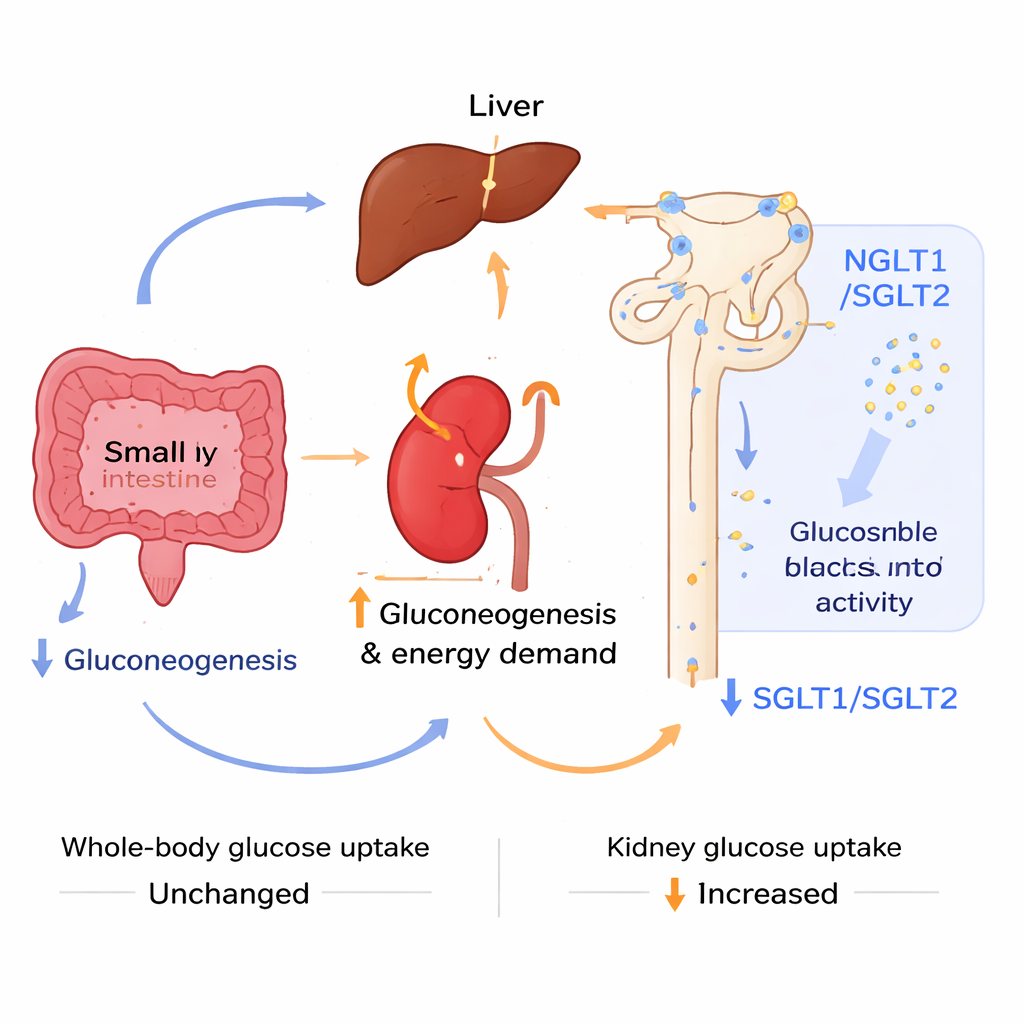
För att ta reda på var den förbättrade sockerregleringen kom ifrån undersökte forskarna hur olika organ producerade glukos. De använde specifika substanser—pyruvat, alanin och glutamin—som matas in i sockerframställande vägar i lever, njure och tarm. Med tiden blev levern och delar av tarmen hos de acidotiska mössen mindre aktiva när det gällde att nysyntetisera glukos, särskilt från alanin och glutamin. Däremot visade njuren tecken på ökat arbete: nyckelgener involverade i glukosproduktion och energitillförsel var uppreglerade, och avbildning med en radioaktiv glukosanalog visade högre sockerupptag i njurarna och urinblåsan, även om totala kroppsupptaget var oförändrat. Samtidigt förlorades mer glukos i urinen efter en sockerbelastning, eftersom njurens huvudsakliga natrium‑glukostransportörer, som normalt återtar filtrerat socker, var nedreglerade på både RNA‑ och proteinnivå. Denna kombination—mindre socker tillverkat av lever och tarm, mer socker förbränt och spillt av njuren—hjälpte till att hålla blodsockernivåerna i schack.
Djupa förändringar inne i njurcellerna
Snapshots av genaktivering i njurarna under de första två månaderna av behandling visade en bred ombyggnad av cellulära maskineriet. Vägbanor involverade i transport av laddade partiklar (anjoner), återupptag av bikarbonat och drift av mitokondrier och oxidativ fosforylering—cellens huvudsakliga energigeneratorer—var upptrissade. Gener kopplade till glukos‑ och fettmetabolism skiftade också uppåt, medan vissa immunsvar och avgiftningsvägar, inklusive delar av komplementsystemet och cytokrom P450‑familjen, dämpades. Dessa mönster stämmer överens med en njure som arbetar hårdare för att utsöndra syra, förbrukar mer bränsle och samtidigt omprogrammerar hur den hanterar socker och lipider för att möta det ökade energibehovet.
Vad detta betyder för personer med njur‑ och sockerproblem
Sammanfattningsvis skadade inte långvarig, mild metabolisk acidos blodsockerkontrollen hos möss—faktum är att den förbättrade den—genom att minska sockerproduktionen i lever och tarm, sänka sockeråterupptaget i njuren och öka njurens egen energianvändning. Insulin själv spelade ingen större roll än vanligt. Detta betyder inte att acidos är bra eller att patienter bör förbli acidotiska; acidos har fortfarande många skadliga effekter. Men fynden visar att kroppen kan anpassa sig på oväntade sätt och lyfter fram njuren som en kraftfull regulator av blodsocker. Framtida arbete kan kanske utnyttja några av dessa njur‑baserade mekanismer—som ökad urinär glukosförlust och förändrad glukosproduktion—utan att utsätta patienter för riskerna med kronisk acidos.
Citering: Zaibi, N., Montaigne, J., Baraka-Vidot, J. et al. Chronic NH4Cl loading improves glucose tolerance without modifying insulin sensitivity in mice. Sci Rep 16, 7048 (2026). https://doi.org/10.1038/s41598-026-38007-7
Nyckelord: metabolisk acidos, glukostolerans, njurfunktion, glukoneogenes, typ 2‑diabetesrisk