Clear Sky Science · sv
Utforskning av dynamiken i vätskors – och kemiska arters – interaktioner i komplexa reaktionsmekanismer: klassificering av snabba och långsamma arter och bifurkationsanalys
Varför reaktionshastigheter spelar roll
Kemiska reaktioner driver allt från bilmotorer till levande celler, men inte alla reagerande partiklar följer samma tidsskala. Vissa arter dyker upp och försvinner i ett ögonblick; andra förändras bara långsamt över tiden. Denna artikel undersöker hur man kan sortera dessa snabba och långsamma aktörer i en nyckelreaktion som omvandlar väte och syre till vatten, och hur den kunskapen kan hjälpa forskare att tygla annars svårhanterliga reaktionsnätverk inom energi, miljö och industriprocesser.
Att reda ut trängseln i kemisk trafik
I komplexa reaktioner bildas, reagerar och försvinner dussintals mellanprodukter långt innan slutprodukterna stabiliseras. Att följa varje detalj blir snabbt överväldigande. Författarna fokuserar på en fyrastegsmekanism för väteoxidation, en klassisk process där väte och syre förenas till vatten. Istället för att behandla alla arter lika använder de matematiska verktyg för att skilja de som reagerar nästan omedelbart från dem som utvecklas mer långsamt. Denna uppdelning låter dem krympa hela modellen till ett lägre-dimensionellt ”skelett” som fortfarande fångar det övergripande beteendet.
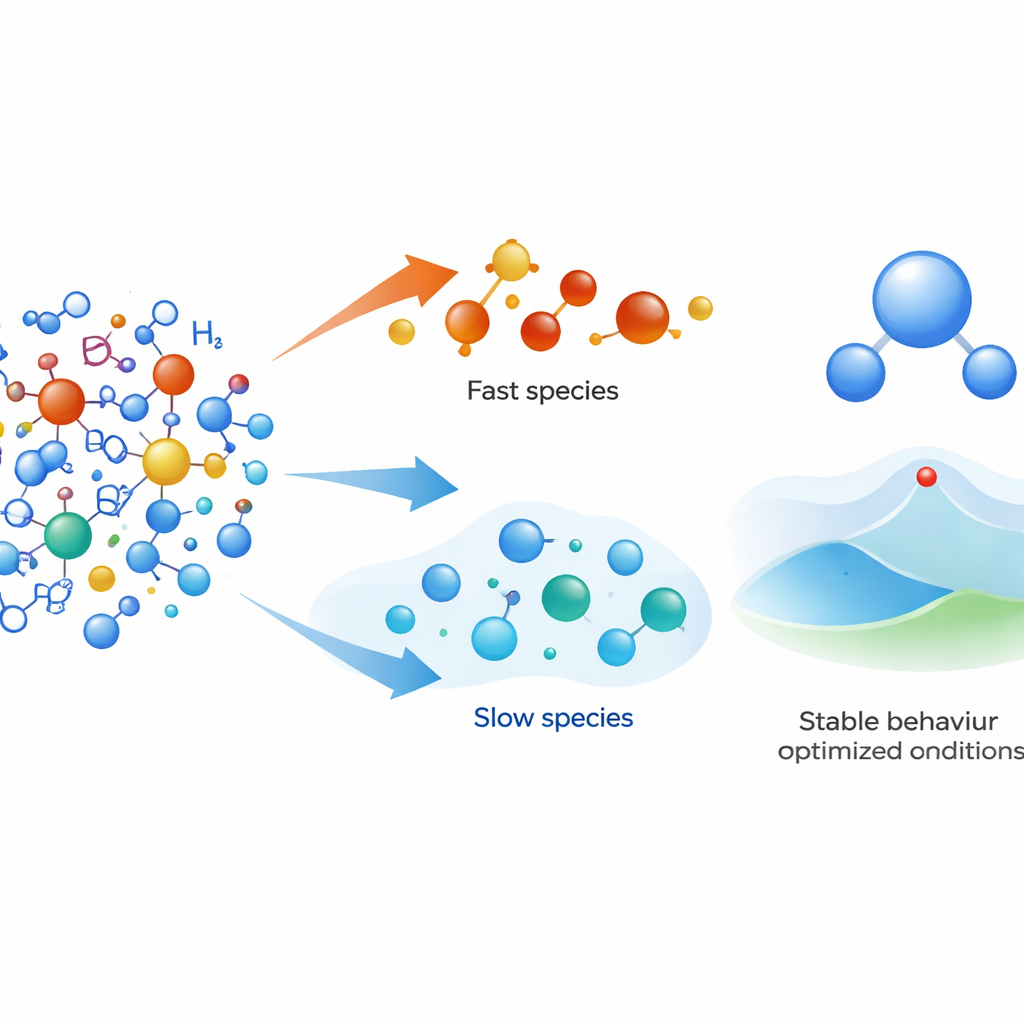
Att hitta de snabba och de långsamma spelarna
För att göra denna separation precis skriver teamet om reaktionslängningarna i skalad, dimensionslös form och tillämpar idéer från singular perturbation-teori och kvasi-steady-state-approximationer. Enkelt uttryckt letar de efter variabler som förändras så snabbt att de, efter en kort uppstartstid, kan behandlas som nära konstanta över tiden. Genom att tillämpa detta ramverk på väte, syre, hydroxyl och relaterade arter visar de att enskilda atomer och radikaler såsom H, O och OH är de snabba aktörerna. Däremot beter sig hela molekyler som H2, O2 och H2O som långsamma arter, som kryper mot sina slutliga värden på mycket längre tidsskalor. Tidsserieplottar och numeriska data bekräftar att radikaler når jämviktsnivåer tidigt, medan molekylära arter fortsätter att förändras långt efteråt.
Att se vilken väg som fyller reservoaren
I denna mekanism kan vatten bildas genom två konkurrerande vägar. I den ena reagerar hydroxyl (OH) med molekylärt väte (H2) för att producera vatten och regenerera en väteatom; i den andra förenas OH direkt med H för att bilda vatten i ett enda radikalrekombinationssteg. Genom att beräkna den omedelbara nettoströmmen längs varje väg spårar författarna vilken bana som bidrar mest vid varje ögonblick. Under de valda förhållandena bär den väteassistade vägen nästan all den effektiva trafiken mot vatten, medan den direkta radikalvägen ligger nära balans, med fram- och återflöden som nästan tar ut varandra. Ett tidsberoende ”dominanskvot” visar att den väteassisterade vägen styr vattenbildningen tidigt och förblir huvudbidragsgivaren när systemet närmar sig stationärt tillstånd.
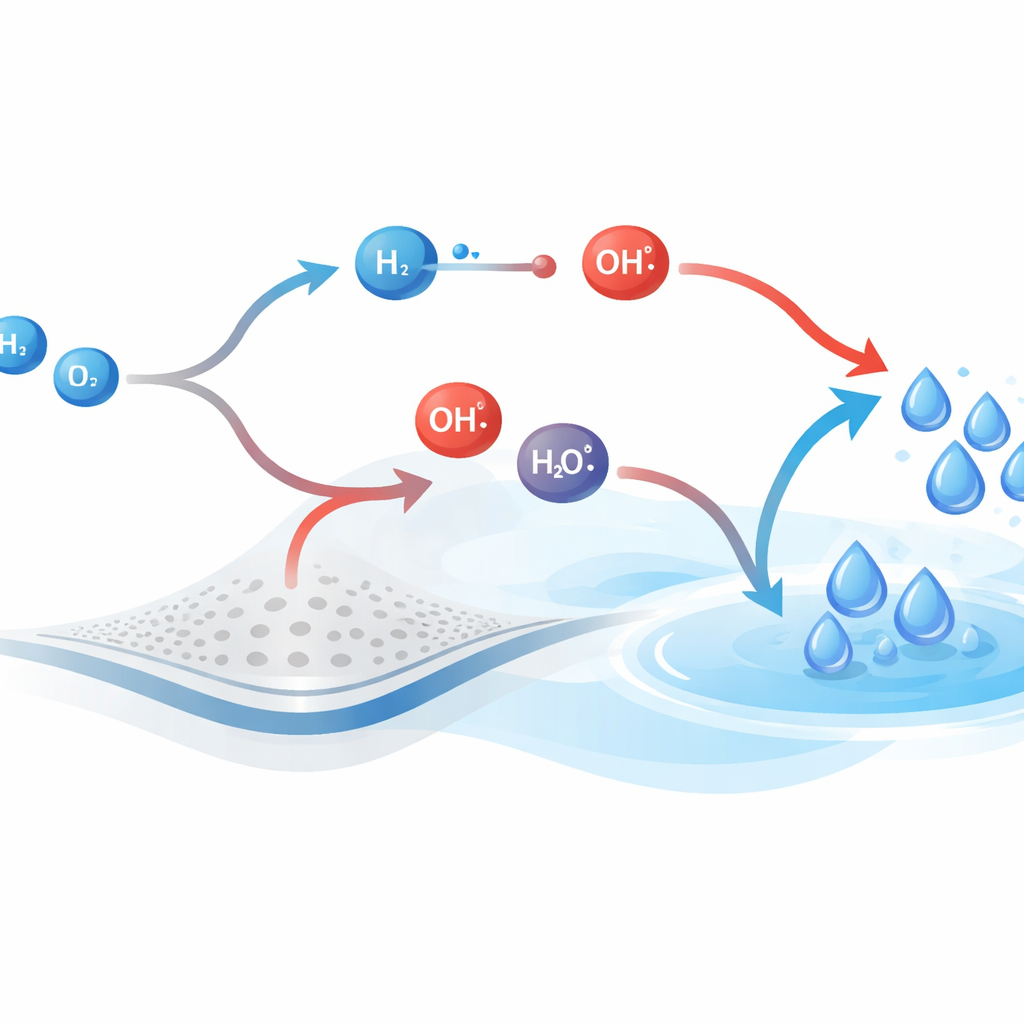
Att pröva vilka rattar som betyder mest
Att veta vilka som är snabba och vilka som är långsamma är bara en del av bilden; ingenjörer behöver också veta vilka parametrar som är värda att justera. Författarna tillämpar både lokal och global känslighetsanalys för att besvara detta. Lokala metoder undersöker hur små förändringar i individuella reaktionskonstanter eller startmängder påverkar specifika arter, och visar att väteatomen är särskilt känslig för variationer i vissa reaktionshastigheter. Globala metoder, baserade på Sobol-index, utforskar hela spannet av parameterosäkerhet och visar att hastighetskonstanter som involverar OH och H2 utövar det starkaste inflytandet över hur mycket vatten som slutligen produceras. Tillsammans lyfter dessa verktyg fram en liten uppsättning inflytelserika parametrar som är dolda i en stor kinetisk modell.
Kartlägga var beteendet plötsligt kan ändras
Slutligen använder studien bifurkationsyta-analys för att utforska hur stationära koncentrationer reagerar när nyckelhastighetskonstanter varierar över breda intervall. Genom att visualisera resultaten som släta ytor hittar författarna att radikaler som H, O och OH är mycket känsliga och visar krökta landskap som blottlägger regioner av potentiell multistabilitet eller skarpa beteendeskift. Däremot ligger de långsamma, stabila produkterna H2 och H2O på mildare ytor som förändras mer gradvis. Denna kontrast förstärker idén att tidsskilsseparation inte bara är ett matematiskt trick utan en strukturell egenskap hos reaktionsnätverket.
Vad detta betyder för reaktioner i verkliga världen
Genom att kombinera teori, dator simuleringar, känslighetstester och bifurkationsanalys presenterar författarna ett praktiskt recept för att förenkla komplexa reaktionssystem utan att förlora deras väsentliga fysik. För väteoxidation visar arbetet att snabba radikaler styr den tidiga dynamiken, att en väteassisterad väg dominerar vattenproduktionen, och att endast ett fåtal hastighetskonstanter verkligen kontrollerar utfallet. För icke-specialister är huvudbudskapet att även mycket komplicerade kemiska nätverk kan reduceras till en hanterbar kärna om vi lär oss identifiera snabba kontra långsamma arter och fokusera på de få parametrar som betyder mest – en strategi som kan vägleda renare förbränning, bättre katalysatorer och mer effektiva industriella processer.
Citering: Khatoon, A., Shahzad, M., Elmasry, Y. et al. Exploring the dynamics of chemical species interactions in complex reaction mechanism: classification of fast and slow species and bifurcation analysis. Sci Rep 16, 9486 (2026). https://doi.org/10.1038/s41598-026-37965-2
Nyckelord: väteoxidation, reaktionskinetik, modellreduktion, känslighetsanalys, bifurkation