Clear Sky Science · sv
Beräkningsbaserad identifiering och mekanistisk karaktärisering av naturproduktbindare som riktar sig mot PDE6D:s prenylbindande tunnel
Att vända cancerens favoritströmbrytare mot sig själv
Många av de dödligaste cancerformerna — från bukspottkörtel- till kolorektala och lungtumörer — är beroende av en enda molekylär ”på/av”‑knapp kallad RAS. När denna knapp fastnar i PÅ‑läge växer celler okontrollerat. Läkemedelsutvecklare har i årtionden kämpat med att slå av RAS direkt. Denna studie utforskar en annan taktik: att leta efter naturföreningar som diskret kan blockera hjälpproteinet som RAS behöver för att nå sin verkningsplats, och därigenom dämpa dess signal utan att behöva angripa RAS direkt. 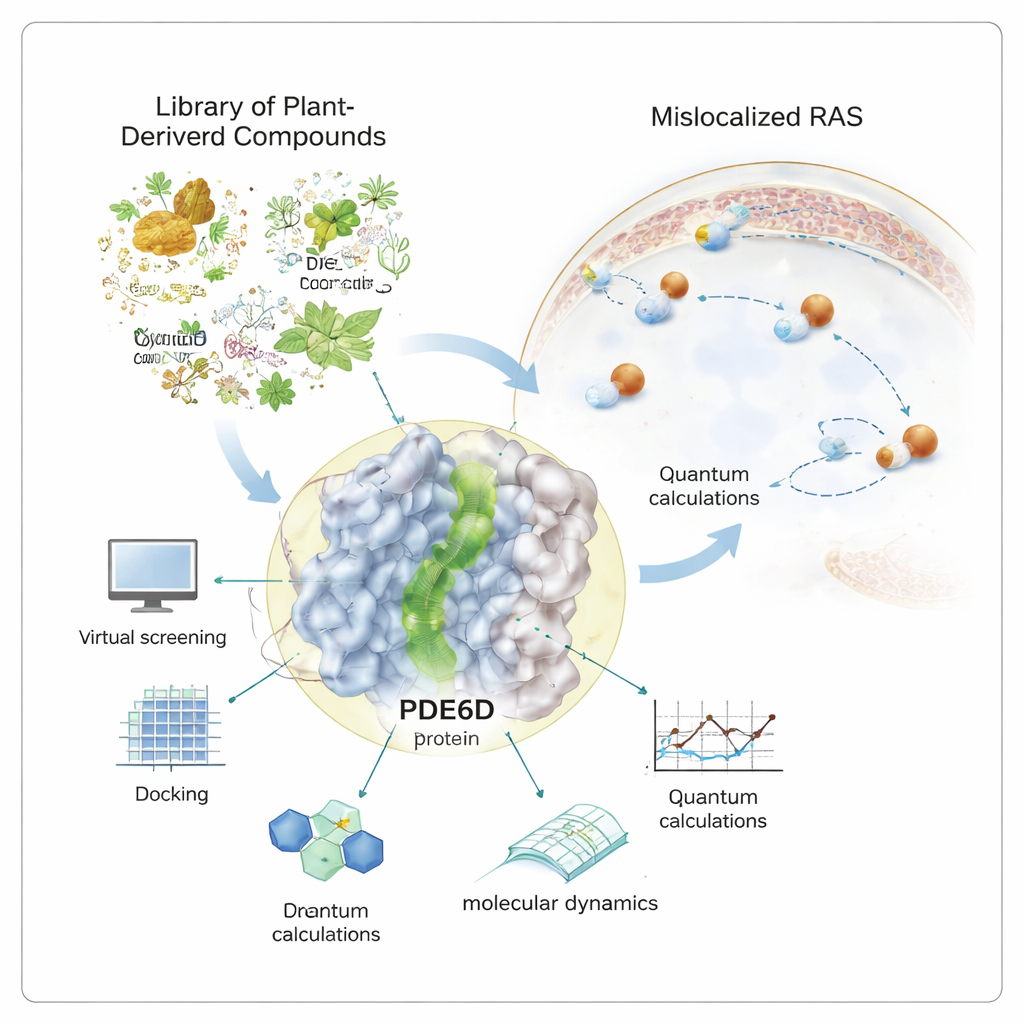
En dold hjälpare i cancerceller
RAS‑proteiner måste sitta på cellmembranets insida för att skicka tillväxtsignaler. För att nå dit bär de en fettrik svans som gör att de kan förankras i membranet. Ett chaperonprotein kallat PDE6D fungerar som en taxi och skärmar av denna svans medan RAS färdas genom cellens vattenrika inre. PDE6D har en smal, oljelinjead tunnel som griper tag i RAS‑svansen. Om tunneln täpps igen är det mer sannolikt att RAS hamnar fel, vilket försvagar dess förmåga att driva cancer. Eftersom många befintliga RAS‑läkemedel bara fungerar för en liten undergrupp av mutationer, är forskare angelägna om att undersöka PDE6D som ett indirekt men bredare relevant mål.
Använda datorer för att prospektera naturens kemiska bibliotek
I stället för att enbart förlita sig på syntetiska kemikalier vände sig författaren till ett kurerat bibliotek med över tusen köpbara naturprodukter — molekyler ursprungligen härledda från växter, mikrober och andra levande källor. Kraftfulla datorverktyg användes för att screena detta bibliotek mot PDE6D:s tredimensionella struktur. I detta virtuella test ”dockades” varje molekyl in i tunneln för att bedöma hur tätt och gynnsamt den kunde binda. De bäst rankade kandidaterna undersöktes sedan närmare med kvantmekaniska beräkningar, som kartlägger hur elektroner är fördelade i varje molekyl och hur lätt de kan bidra till stabiliserande interaktioner inne i proteinfickan.
Stress‑test av lovande kandidater i rörelse
Proteiner och småmolekyler står inte stilla i celler, så studien gick längre än statiska ögonblicksbilder. Med långa molekylärdynamiska simulationer som följer atomrörelser över en halv mikrosekund observerade forskaren hur varje lovande naturförening betedde sig inne i PDE6D‑tunneln över tid. Två kandidater, märkta MolPort-039-052-621 och MolPort-002-507-186, förblev fast förankrade i tunneln med stabila kontaktnätverk, medan en tredje molekyl drev mot tunnelns utgång och blev mer löst bunden. Ytterligare analyser kartlade vilka delar av PDE6D‑strukturen som flexade eller tystnade vid bindning, och hur komplexet utforskade sitt ”energilandskap” — i praktiken vilka konformationer som var mest bekväma och långlivade. 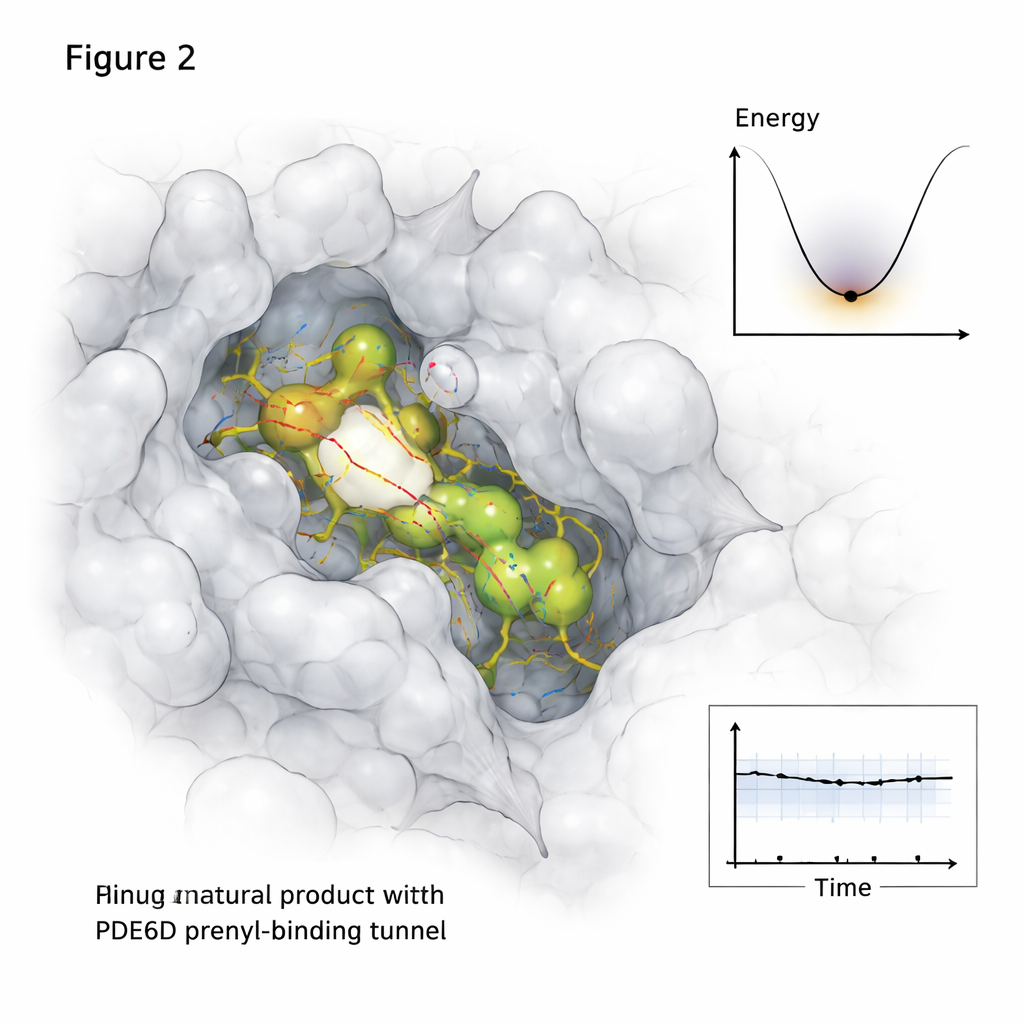
Att balansera bindningsstyrka och läkemedelslika egenskaper
Studien använde också onlineredskap för att förutsäga om dessa naturföreningar verkar vara realistiska utgångspunkter för läkemedel. Alla tre toppträffarna hade kemiska egenskaper förenliga med grundläggande ”drug‑likeness”, men var och en bar på varningsflaggor. Vissa förväntades ha dålig absorption eller löslighet; andra visade tecken på potentiell toxicitet, såsom effekter på hjärtrytm eller DNA. Dessa problem innebär att molekylerna i sin nuvarande form sannolikt inte är färdiga läkemedel. Istället bör de ses som strukturella mallar som kemister kan modifiera — behålla de tunnelpassande egenskaperna samtidigt som man beskär de problematiska delarna.
Vad detta innebär för framtida cancerbehandlingar
Enkelt uttryckt levererar detta arbete inte ett nytt cancerläkemedel, men det kartlägger en lovande väg. Genom att kombinera flera beräkningslager — från snabb dockning till detaljerade simulationer och kvantberäkningar — snävar studien ett omfattande urval av naturmolekyler till en liten grupp som ser väl lämpade ut för att täppa till PDE6D‑tunneln. Om framtida laboratorieexperiment bekräftar att dessa föreningar verkligen felstyr RAS inne i celler och bromsar tillväxten av RAS‑drivna tumörer, kan de inspirera en ny klass behandlingar som riktar in sig på cancerets ”logistik” snarare än dess huvuddrivare direkt.
Citering: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
Nyckelord: RAS-signalering, PDE6D-hämmare, naturprodukter, beräkningsbaserad läkemedelsupptäckt, cancerterapi