Clear Sky Science · sv
Helcellsmodellering förutsäger alternativa strategier för proteomallokering hos arken Methanococcus maripaludis
Varför små metanbildare spelar roll
Methanococcus maripaludis är en mikroskopisk arke som omvandlar enkla kemikalier som koldioxid och format till metan, en huvudkomponent i naturgas. Att förstå hur denna mikroorganism fördelar sina interna resurser—särskilt sina proteiner—kan avslöja allmänna livsregler under energibegränsning och vägleda ansträngningar att utnyttja den som en biologisk metanfabrik eller som plattform för grön kemi.
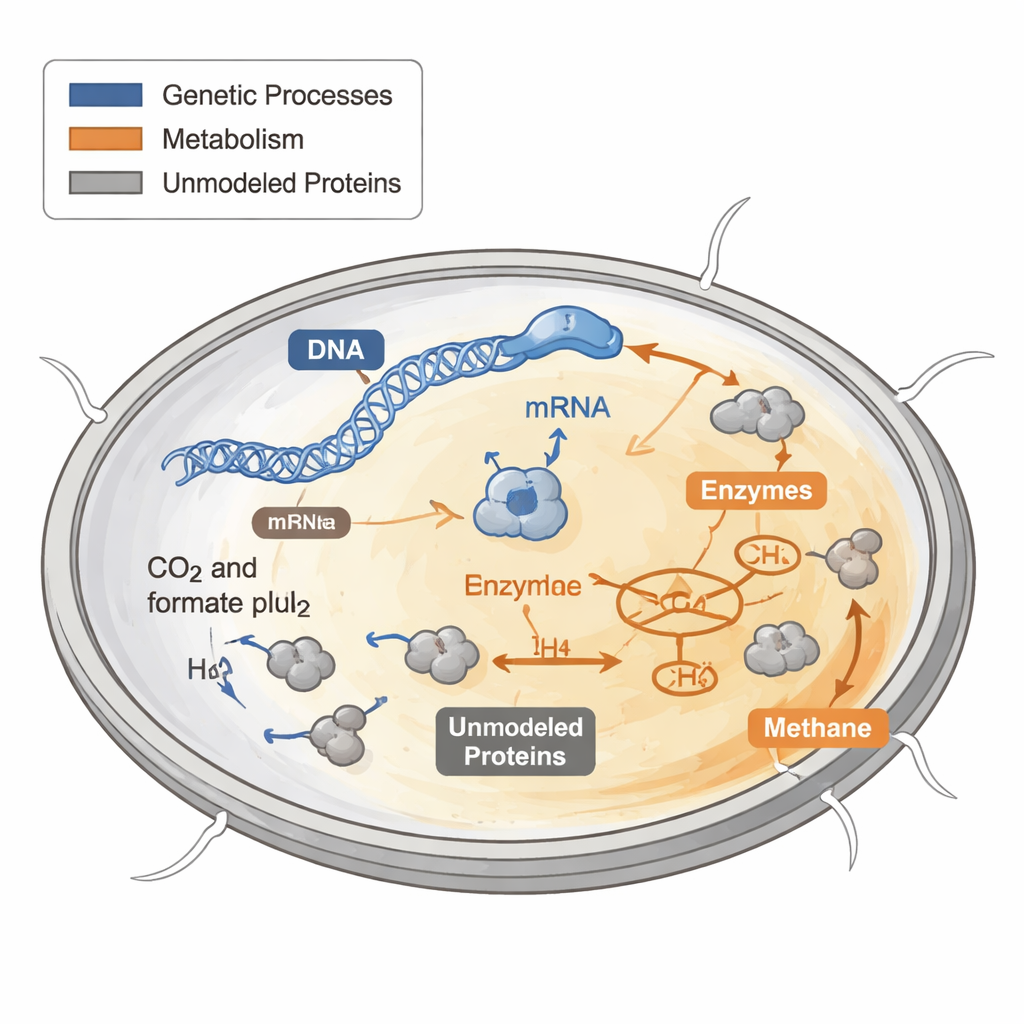
Hur celler använder sin proteinbudget
Varje cell måste bestämma hur den ska använda sin begränsade protein"budget." Vissa proteiner bygger nya celldelar, andra utvinner energi och ytterligare andra sköter underhåll. Tidigare datorbaserade modeller av metabolism behandlade dessa proteiner som om de vore fria och obegränsade, vilket fungerar dåligt när man försöker förutsäga tillväxt under hårda eller näringsfattiga förhållanden. Hos bakterier och jäst har experiment visat att snabbrastande celler avsätter en större del av sin proteinbudget till ribosomerna, de molekylära maskinerna som bygger nya proteiner, medan långsamt växande celler flyttar resurserna till andra funktioner.
En arkee som bryter mot mönstret
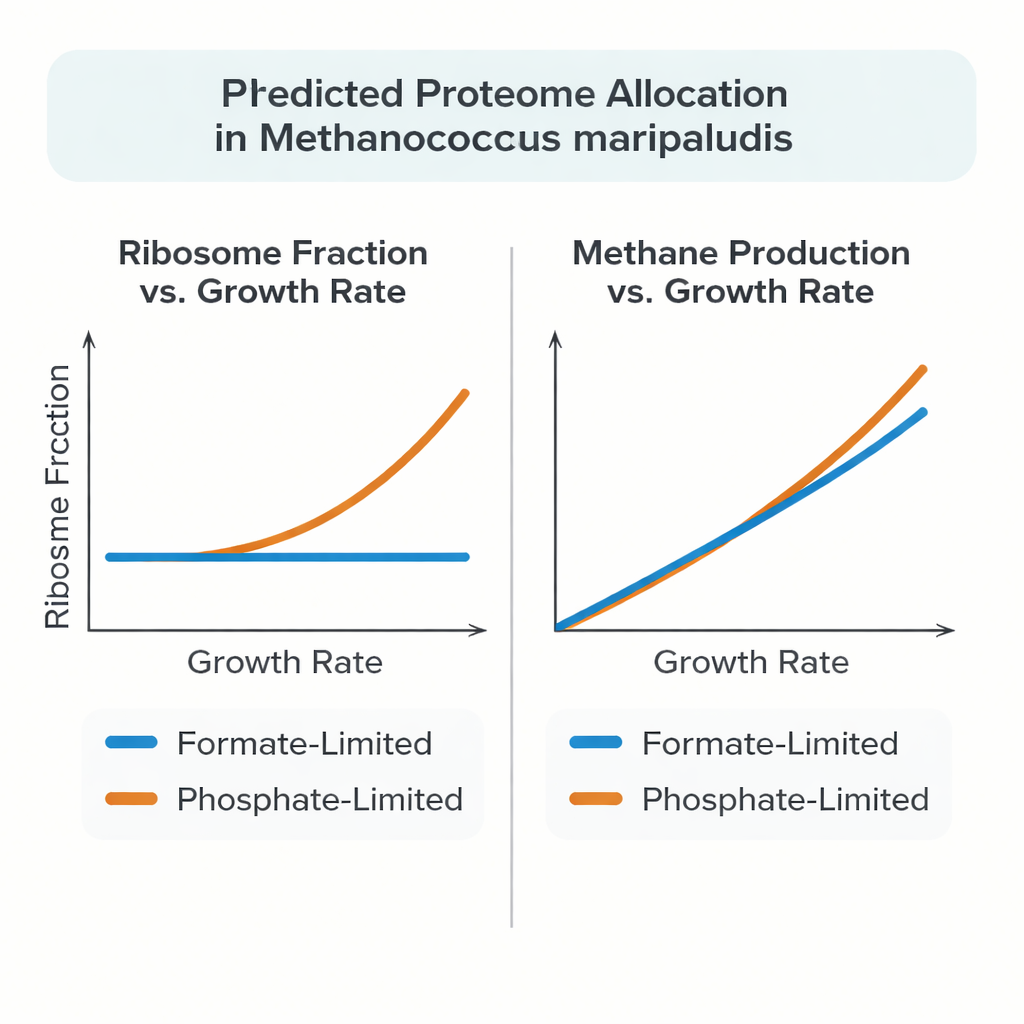
Nyare experiment visade att M. maripaludis inte alltid följer detta mönster. När den växer på format som både näring och energikälla förblir andelen av proteinbudgeten som satsas på ribosomer nära konstant när tillväxten saktar. Vid fosfatbegränsning beter sig däremot arkeen mer konventionellt: andelen ribosomalt protein ökar med tillväxthastigheten, likt Escherichia coli och jäst. För att förklara detta ovanliga beteende byggde författarna en detaljerad helcellsliknande modell som kopplar metabolism till den kostsamma processen att tillverka och montera proteiner och RNA, istället för att behandla proteiner som abstrakta reaktionshastigheter.
Att bygga en helcellsliknande modell
Forskarna utgick från en befintlig metabolisk karta för M. maripaludis och la till tusentals ytterligare reaktioner som beskriver genuttryck: kopiering av DNA till RNA, laddning av transfer-RNA, montering av ribosomer och enzymkomplex, samt utspädning av dessa komponenter vid celldelning. De samlade enzymhastighetsgränser från biokemiska databaser och litteraturen och uppskattade hur stor del av proteinmassan som utgörs av ”omodellerade” proteiner som inte är direkt kopplade till reaktionerna i kartan. Därefter införde de globala begränsningar som sätter gräns för den totala massan av protein och RNA, kopplar reaktionshastigheter till mängden tillgängligt enzym och binder proteinproduktion till ribosomkapacitet. Med dessa begränsningar måste modellen välja hur den ska fördela en fast proteinbudget för att stödja tillväxt.
Vad simuleringarna avslöjade
När modellen testades mot högkvalitativa chemostatexperiment återgav den korrekt uppmätta protein- och RNAmassor, metanproduktionstakter och tillväxtutbyten över ett intervall av låga tillväxthastigheter. Vid formatbegränsning landade den simulerade cellen naturligt i en nästan konstant andel ribosomalt protein när tillväxten förändrades, vilket speglade de experimentella uppgifterna. Vid fosfatbegränsning matchade modellen den observerade ökningen av ribosomandel endast när ribosomer tilläts arbeta snabbare vid låga tillväxthastigheter, i linje med mätningar som visar fler ribosomer aktivt engagerade i proteinsyntes. Modellen föreslog också att en betydande del av proteinet i M. maripaludis inte är strängt nödvändigt för minimal tillväxt, och att överskott av kol och energi kan lagras eller omdirigeras till andra stora molekyler såsom glykogen eller fria aminosyror, beroende på vilken näringsfaktor som är begränsande.
Undersöka mutanter och tillväxtgränser
Eftersom modellen explicit tar hänsyn till proteinkostnaden för varje väg kan den förutsäga inte bara om genetiska mutanter växer, utan hur väl de växer i förhållande till vildtypen. Författarna simulerade stammar som saknar olika vätehanterande enzymer och jämförde förutsagd fitness med laboratoriemätningar över flera tillväxtförhållanden, inklusive närvaro eller frånvaro av vätgas och kolmonoxid. I många fall fångade modellen huruvida mutanter kunde växa och gav rimliga uppskattningar av deras relativa tillväxthastigheter, vilket är en förbättring jämfört med tidigare modeller som bara gav ja-eller-nej-svar. Samma ramverk användes för att uppskatta maximala möjliga tillväxthastigheter under batchförhållanden för olika substratkombinationer.
Vad detta innebär för vetenskap och teknik
I vardagliga termer visar denna studie att M. maripaludis använder en alternativ strategi för att budgetera sin proteinarbetskraft, genom att hålla sina proteinfabriker igång på en jämn andel av budgeten under vissa förhållanden istället för att trappa ned dem när tillväxten avtar. Genom att bädda in detta beteende i en detaljerad, datadriven modell erbjuder arbetet en testbädd för att utforska hur energibegränsade mikrober balanserar tillväxt, underhåll och lagring. För tillämpad forskning ger modellen en färdplan för att konstruera denna arkee så att den producerar mer metan eller andra produkter genom att identifiera vilka enzymer och vägar som är mest kostsamma i termer av proteininvestering. På ett mer övergripande plan utvidgar den kraftfull helcellsliknande modellering bortom bakterier och jäst in i arkeernas domän, och hjälper till att överbrygga gapet mellan molekylära detaljer och storskaligt beteende hos mikrobiella samhällen som påverkar klimat, energi och industriell bioteknik.
Citering: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
Nyckelord: Methanococcus maripaludis, proteomallokering, helcellsmodellering, metanogenes, arkeemetabolism