Clear Sky Science · sv
Beräkningsstrategier för att utröna insikter från kända hämmare för vidare ledoptimering: En fallstudie på celecoxib-analoger
Varför små förändringar i smärtstillande medel spelar roll
Moderna smärtstillande medel dämpar inte bara värk; de finjusterar kroppens kemi på mycket precisa sätt. Celecoxib, ett vanligt antiinflammatoriskt läkemedel, riktar in sig på ett enzym som är involverat i smärta och svullnad samtidigt som det till stor del skonar en närbesläktadzym som skyddar magen. Ändå beter sig dussintals nära kemiska släktingar till celecoxib väldigt olika i kroppen. Denna studie använder datorbaserad modellering för att ställa en bedrägligt enkel fråga med stora konsekvenser för säkrare läkemedel: hur mycket betyder en enda liten förändring i en molekyl?
Enzymet som sätter igång smärta
När vävnad skadas eller inflammeras frisätter kroppen ett fetthaltigt ämne kallat arakidonsyra. Ett enzym som kallas COX-2 omvandlar detta ämne till prostaglandiner, som utlöser smärta, feber och svullnad. Ett närbesläktat enzym, COX-1, hjälper till att skydda magslemhinnan och blodplättarna. Äldre smärtstillande medel som ibuprofen påverkar båda enzymerna, lindrar smärta men irriterar ofta magen. Celecoxib designades för att glida in i ett något större fickformat utrymme som främst finns i COX-2 och därigenom blockera smärtsignaler medan mycket av COX-1:s skyddande funktion lämnas intakt. Att förstå fickans detaljerade form och hur läkemedelsmolekyler ligger i den är centralt för att utforma nya mediciner som är både effektiva och säkra.
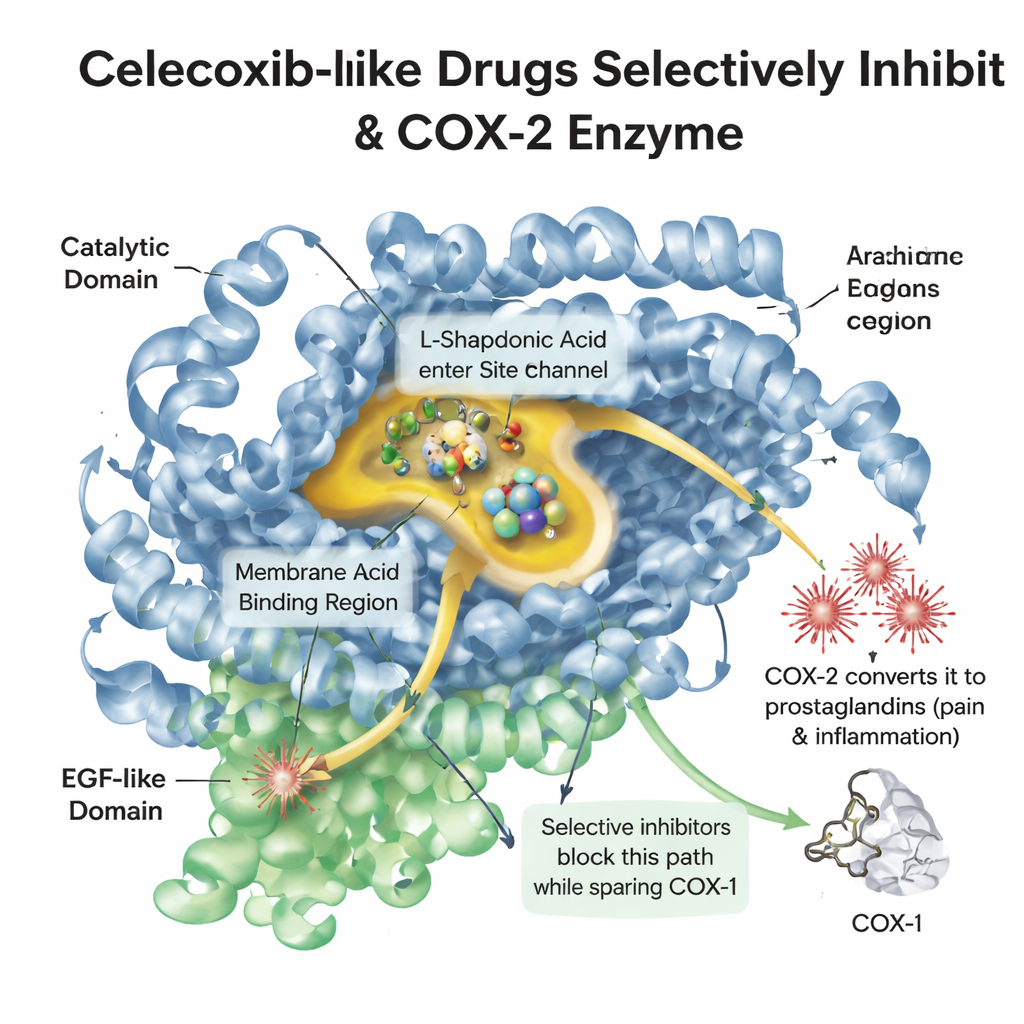
Ett digitalt bibliotek av look‑alike-läkemedel
Forskarna satte samman ett urval av 375 molekyler som alla delar celecoxibs grundläggande tre-ringstruktur men skiljer sig åt i små detaljer, som att byta ut en enda atom eller sidokedja. De hämtade dessa strukturer och deras uppmätta COX-2-hämmande styrka från en offentlig läkemedelsdatabas. Med hjälp av kemiprogram genererade de 3D-modeller av varje molekyl, beräknade nästan 2 000 numeriska deskriptorer för deras form och egenskaper, och dockade dem sedan in i en högupplöst struktur av COX-2-enzymet. Vid dockning skjuter en dator försiktigt in en molekyl i enzymets ficka på många sätt och poängsätter hur tätt varje position passar.
Vad som verkligen styr styrka och selektivitet
Teamet zoomade in på tre nyckelregioner i celecoxib. ”Site‑1” är en ring som sitter i en fettrik fläck i fickan; ”Site‑2” är en ring med en fluorrik svans; och ”Site‑3” är en ring som bär en sulfonamidgrupp som bildar starka vätebindningar. Deras analys visade att Site‑1 föredrar små, opolära grupper som bevarar hydrofoba kontakter; att göra denna region mer vattenälskande, till exempel genom att lägga till en –OH- eller karboxylgrupp, försvagade vanligtvis läkemedlet. Vid Site‑2 förbättrade små elektronegativa grupper såsom fluor ofta potensen genom att förbättra interaktioner i en trång ficka, medan större eller mer polära svansar tenderade att försämra aktiviteten. Vid Site‑3 var sulfonamidens kväve, som kan donera en vätebindning, avgörande; att ersätta det med en icke-bindande version minskade bindningen märkbart.
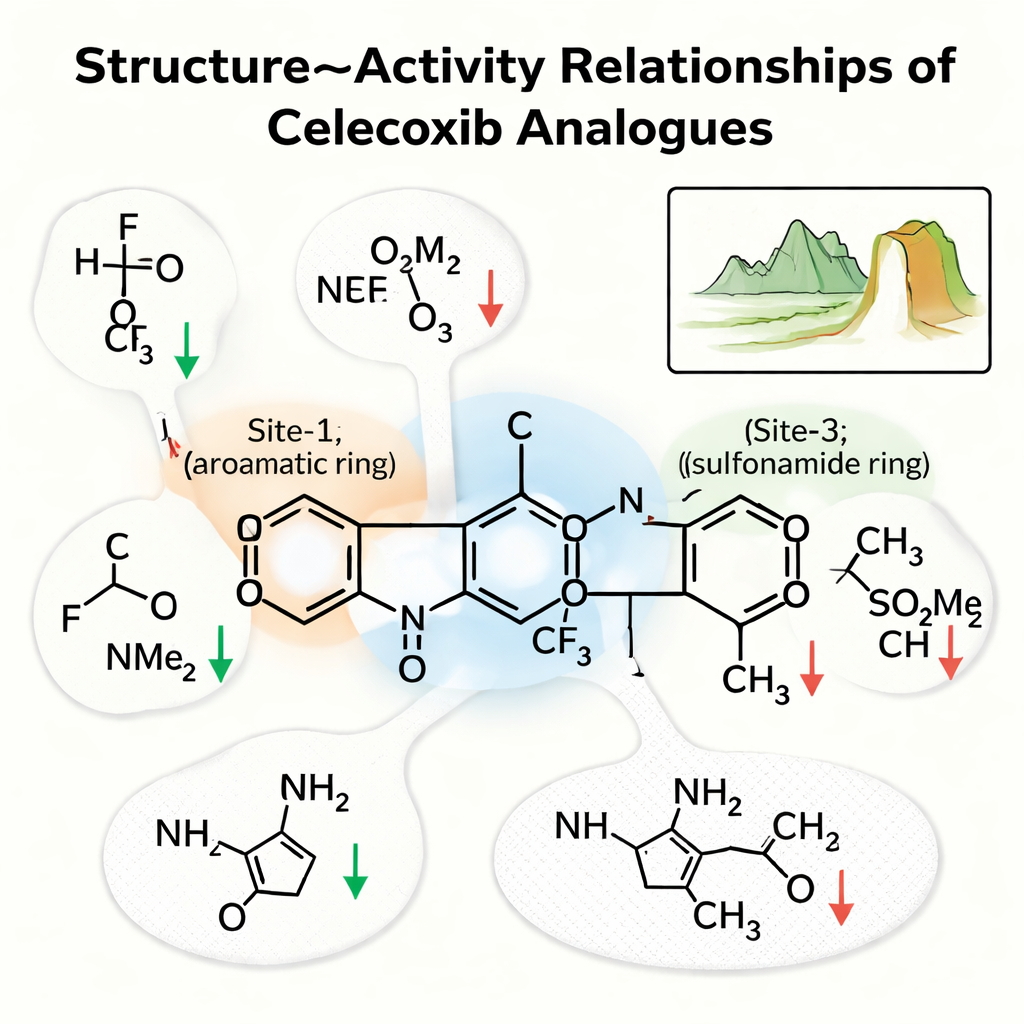
Klipp i det kemiska landskapet
För att gå bortom enkla trender byggde författarna ett ”struktur–aktivitet-landskap” som frågar hur mycket läkemedlets styrka hoppar när strukturen ändras bara lite. I detta perspektiv ligger de flesta celecoxib-liknande föreningar på mjuka kullar: att justera dem—till exempel genom att flytta en halogen eller lägga till en liten flexibel grupp—skjuter potensen upp eller ner på förutsägbara sätt. Men några par bildar skarpa ”aktivitetsskrevor”, där en liten förändring, som att byta en metylgrupp mot en trifluormetylgrupp eller lägga till en enda fluoratomen, orsakar en dramatisk vinst eller förlust av aktivitet. Studien körde också fullständiga molekylära dynamiksimuleringar—virtuella filmer av läkemedels–enzymkomplex i rörelse—which som bekräftade att de bästa analogerna sitter stabilt i fickan under hundratals nanosekunder.
Vägledning för nästa generation säkrare smärtstillare
För en icke-specialist är huvudbudskapet att små detaljer i läkemedelsdesign betyder enormt mycket. Två föreningar som ser nästan identiska ut på papper kan skilja sig med tusenfalt i hur starkt de blockerar COX-2, helt enkelt därför att en extra atom förbättrar passformen i en mikroskopisk ficka eller stör en nyckelkontakt. Genom att systematiskt kartlägga vilka förändringar som hjälper eller skadar vid var och en av celecoxibs tre nyckelplatser, och genom att lyfta fram de farliga ”skrevorna” där små justeringar får outsized effekter, erbjuder detta beräkningsarbete en färdplan för kemister. Det pekar mot nya antiinflammatoriska läkemedel som behåller celecoxibs smärtlindrande effekt samtidigt som de trycker säkerhet och selektivitet ännu längre.
Citering: Grewal, S., Ghosh, B., Narayan, U. et al. Computational strategies for unraveling insights from known inhibitors for further lead optimization: A case study on Celecoxib analogues. Sci Rep 16, 6720 (2026). https://doi.org/10.1038/s41598-026-37798-z
Nyckelord: COX-2-hämmare, celecoxib-analoger, antiinflammatoriska läkemedel, beräkningsbaserad läkemedelsdesign, struktur-aktivitetssamband