Clear Sky Science · sv
Synergistisk målning av ARID2–MYC‑axeln med pomalidomid och panobinostat övervinner inneboende IMiD‑resistens vid multipelt myelom
Varför denna forskning är viktig för patienter
Multipelt myelom är en cancersjukdom i antikroppsproducerande celler i benmärgen som blivit mer behandlingsbar men fortfarande sällan botbar. Många patienter slutar så småningom svara på standardläkemedel, vilket lämnar läkare med färre alternativ. Denna studie undersöker varför kombinationen av två befintliga läkemedelsklasser — så kallade IMiD‑preparat som pomalidomid och läkemedel som påverkar DNA‑paketering, histondeacetylas (HDAC)‑hämmare som panobinostat — kan samverka för att döda myelomceller, även när cancern redan är resistent mot IMiD ensam. Att förstå detta samspel på molekylär nivå kan vägleda bättre kombinationsbehandlingar och hjälpa fler patienter att få nytta av de läkemedel vi redan har.
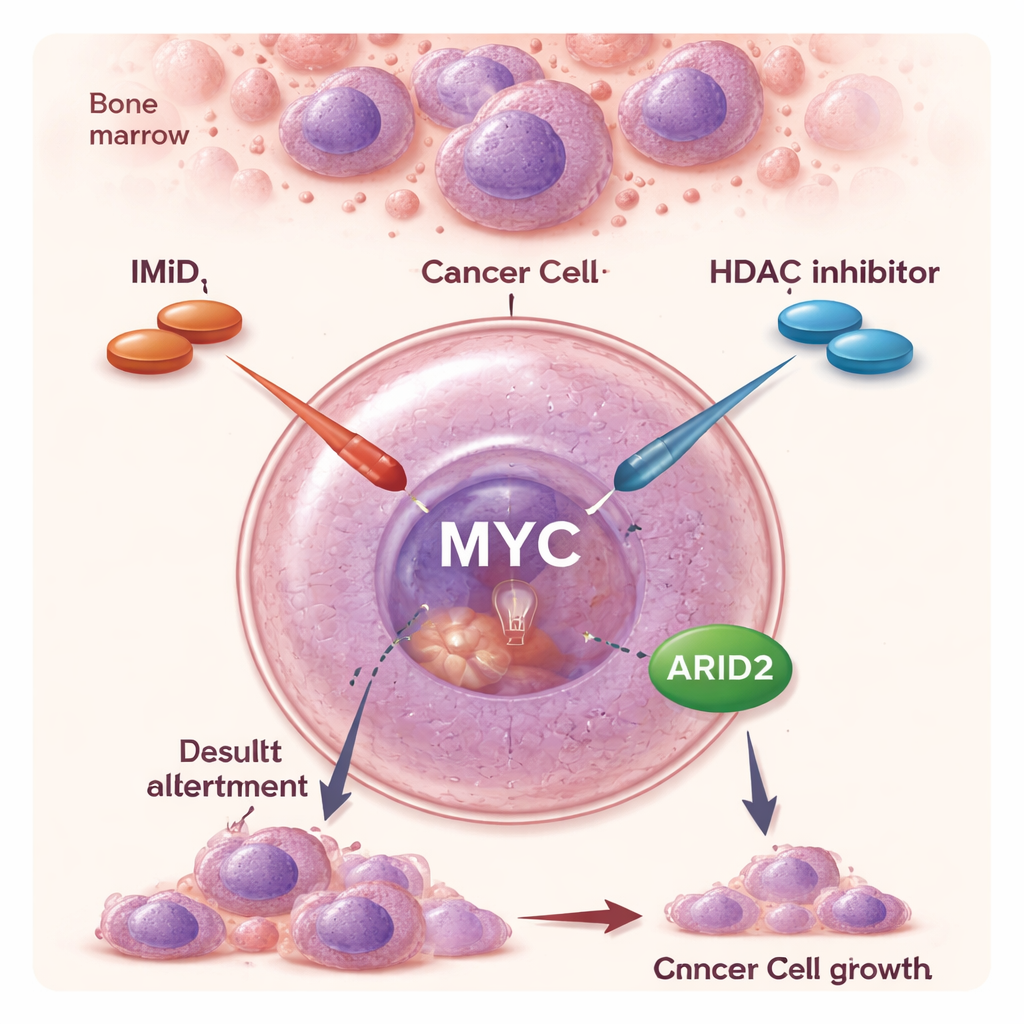
Två äldre läkemedelsklasser, ett nytt partnerskap
Under de senaste två decennierna har IMiD‑preparat och andra riktade läkemedel förlängt överlevnaden betydligt för personer med multipelt myelom. IMiD verkar på ett ovanligt sätt: istället för att enbart blockera ett protein gör de så att vissa proteiner märks för nedbrytning, vilket i praktiken raderar dem från cellen. Genom detta försvagar de viktiga överlevnadssignaler som myelomcellerna är beroende av. HDAC‑hämmare som panobinostat verkar annorlunda. De luckrar upp DNA:s täta paketering och omformar brett vilka gener som är påslagna eller avstängda. Som enskilda läkemedel har HDAC‑hämmare måttliga effekter och kan ge biverkningar, men kliniska prövningar antydde att kombination med IMiD kan ge ett mycket starkare anticancereffekt, även hos patienter vars sjukdom inte längre svarar på IMiD ensam. Den molekylära orsaken till denna synergi hade dock förblivit oklara.
En gemensam brytpunkt: att dämpa MYC
Forskarna testade systematiskt kombinationer av flera IMiD‑preparat med olika HDAC‑hämmare över ett panel av myelomcellinjer, med ett standardiserat poängsystem för att mäta hur mycket starkare kombinationerna var än varje läkemedel för sig. De fann att pomalidomid plus panobinostat visade särskilt stark synergi i de flesta cellmodeller, och att denna effekt var beroende av ett protein kallat cereblon, som IMiD använder för att rikta sina protein"offer" för nedbrytning. Genom att analysera global genaktivitet upptäckte teamet att panobinostat och en närbesläktad bredverkande HDAC‑hämmare kraftigt slog av MYC, en huvudreglerande gen för tillväxt som ofta beskrivs som en "onkogenmotor" i cancerceller, och att IMiD lade ytterligare press på samma nod. När forskarna tvingade myelomceller att fortsätta producera MYC från en läkemedelsokänslig källa försvann den kraftfulla effekten av läkemedelsparet i stort sett, vilket visar att nedreglering av MYC är central för deras samverkan.
Att knäcka resistens via en alternativ väg
Vissa myelomceller är inneboende resistenta mot IMiD: även om de förväntade tidiga målen förstörs, tystas inte MYC och andra överlevnadssignaler ordentligt, så cellerna fortsätter växa. I en sådan resistent modell var den standardiserade IMiD‑vägen som länkar tidiga mål till MYC "frikopplad." Teamet undersökte om en alternativ väg fortfarande kunde koppla IMiD till MYC. De fokuserade på ARID2, en komponent i en stor DNA‑omformasande maskin kallad SWI/SNF‑komplexet. Tidigare arbete hade visat att pomalidomid kan märka ARID2 för nedbrytning och att detta bidrar till att sänka MYC. I resistenta celler reducerade pomalidomid ensam ARID2 endast måttligt, delvis därför att cellen ökade sin ARID2‑produktion som svar. När panobinostat tillsattes undertryckte det själva ARID2‑genen, vilket övervann denna feedback‑slinga. Tillsammans minskade de två läkemedlen kraftigt ARID2‑proteinet och därefter MYC, vilket ledde till potent celldöd även i IMiD‑resistenta cellinjer.
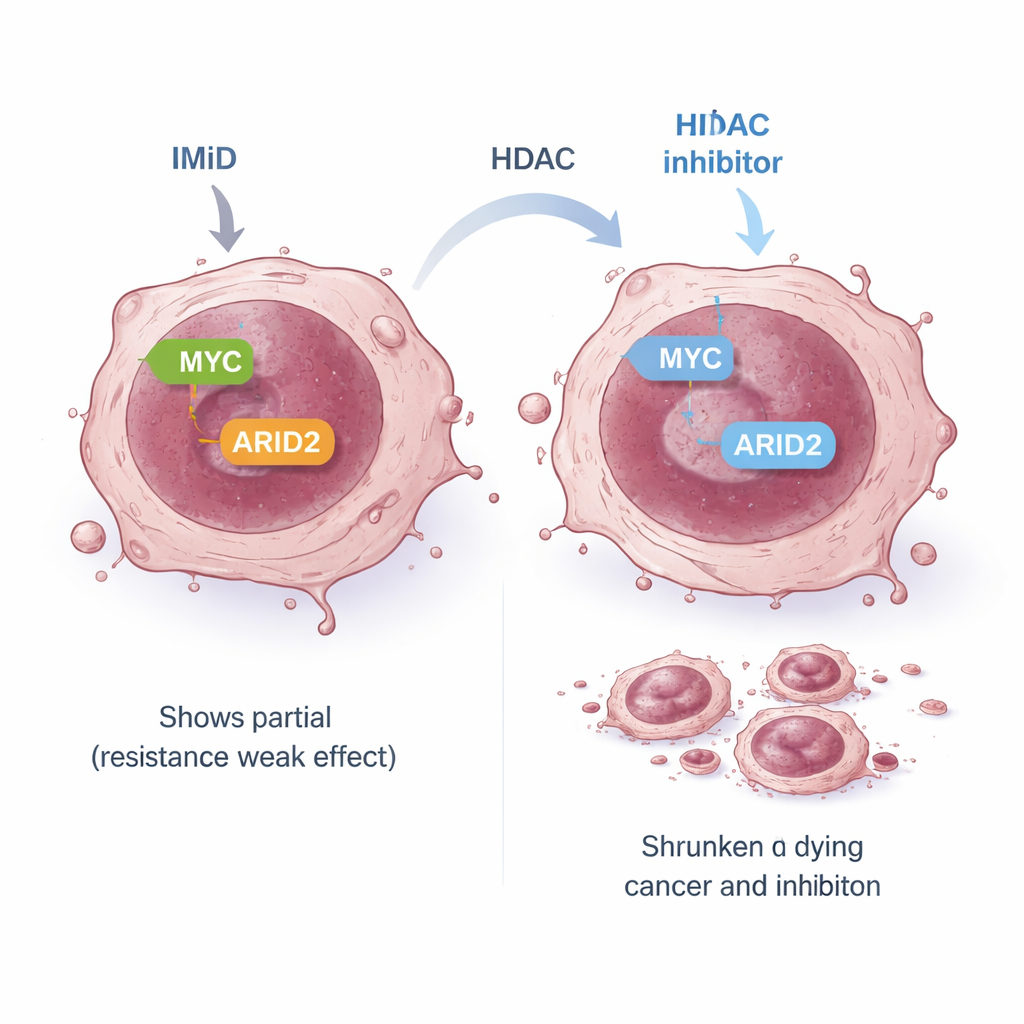
Att blottlägga en bredare svag punkt i cancerceller
Eftersom ARID2 bara är en medlem i SWI/SNF‑komplexet undrade författarna om hela komplexet kunde vara en terapeutisk svag punkt. De fann att HDAC‑hämmare sänker nivåerna av flera SWI/SNF‑komponenter, och att ett separat småmolekylärt läkemedel utformat för att blockera komplexets kärnmotorer (BRG1/BRM) ensamt kan bromsa myelomcellstillväxt och minska MYC. Viktigt är att denna SWI/SNF‑hämmare också fungerade synergistiskt med både pomalidomid och panobinostat, och en tremedicinsk kombination pressade ner ARID2 och MYC ännu mer samtidigt som den starkt undertryckte cellproliferation. Genom att undersöka vilka specifika HDAC‑enzymer som var inblandade lyfte forskarna fram HDAC1 som en nyckelspelare som hjälper till att upprätthålla ARID2–MYC‑vägen, medan andra HDAC:er verkar påverka MYC genom parallella rutter.
Vad detta betyder för framtida myelombehandling
För icke‑specialister är huvudbudskapet att myelomceller tycks vara beroende av en gemensam "tillväxtkontrollknutpunkt" centrerad kring MYC, och att det finns mer än en väg in till den knutpunkten. Standard IMiD‑terapi träffar främst en väg; i vissa resistenta cancerformer är den vägen blockerad, så MYC förblir aktivt. Denna studie visar att en alternativ väg — som går genom ARID2 och SWI/SNF‑komplexet — är kvar och att användning av panobinostat tillsammans med pomalidomid kan stänga den. Genom att medvetet kombinera läkemedel som påverkar MYC från flera håll kan kliniker kanske övervinna vissa former av inneboende läkemedelsresistens samtidigt som man potentiellt använder lägre doser av varje läkemedel. Trots att ytterligare preklinisk och klinisk forskning krävs, ger fynden en tydligare ritning för att utforma smartare, mekanismbaserade kombinationer för patienter med svårbehandlat multipelt myelom.
Citering: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Nyckelord: multipelt myelom, läkemedelsresistens, pomalidomid, panobinostat, MYC