Clear Sky Science · sv
Mekanism och evolutionär divergens hos en ny oxiderad polyvinylalkoholhydrolas i Stenotrophomonas rhizophila QL-P4
Varför en vanlig ”grön” plast ändå dröjer kvar i naturen
Polyvinylalkohol, eller PVA, förekommer i allt från tvättmedelspods till textilbeläggningar och papper. Den marknadsförs ofta som miljövänlig eftersom mikrober i princip kan bryta ner den. Ändå sönderdelas detta plastliknande material mycket långsamt i verkliga floder, jordar och hav och kan bestå i årtionden som mikro- och nanoplastfragment. Denna studie granskar ett av naturens verktyg för att ta itu med PVA: ett nyligen upptäckt enzym från en jordbakterie som kan klyva detta envisa polymer till mindre, säkrare bitar.
En liten jordhjälpare med ett stort uppdrag
Forskare isolerade tidigare en bakterie kallad Stenotrophomonas rhizophila QL-P4 från bergjord i Kina och upptäckte att den kan växa genom att använda PVA som föda. I det nya arbetet fokuserade de på en enskild misstänkt gen, benämnd BAY15_0160, som såg ut att kunna koda för ett enzym som skär oxiderat PVA. Genom att noggrant ta bort denna gen, lägga tillbaka den och tvinga bakterien att överproducera den visade de att BAY15_0160 är avgörande för effektiv PVA-nedbrytning. När genen togs bort förlorade mikroben ungefär 40 % av sin förmåga att konsumera PVA; återställande av genen återförde aktiviteten, vilket bekräftar att dess produkt är en nyckelspelare i degraderingsvägen.
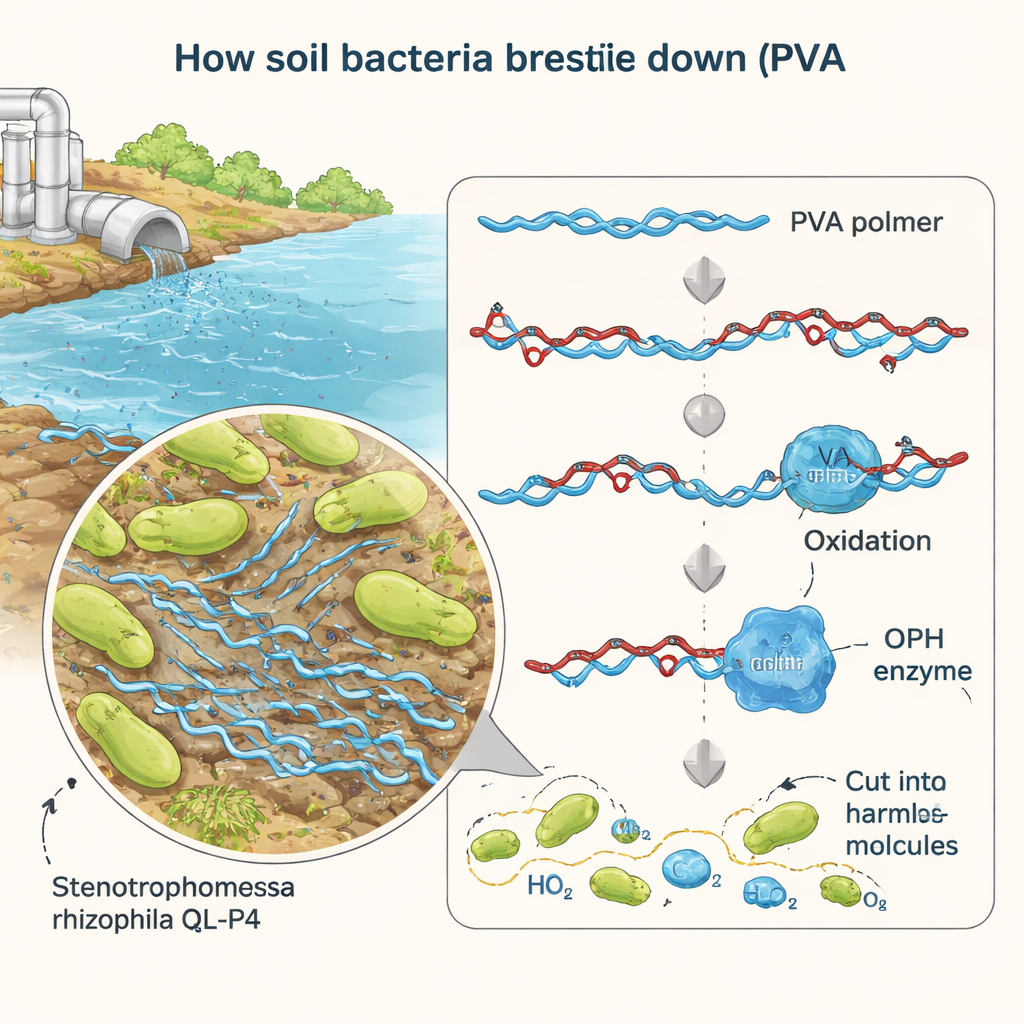
Mätning av hur enzymet utför sitt arbete
För att studera enzymet i detalj producerade teamet det i stora mängder med laboratoriestammar av Escherichia coli. De renade proteinet, som visade sig vara omkring 35 kilodalton stort, och testade dess aktivitet under olika förhållanden. Med en enkel testmolekyl som frigör ett gult färgämne vid klyvning följde de hur snabbt enzymet arbetade vid olika temperaturer och pH-värden. Enzymet var mest aktivt vid ungefär rumstemperatur (30 °C) och vid ett neutralt pH liknande många naturliga vatten. Under dessa milda förhållanden visade det hög katalytisk effektivitet, vilket innebär att varje enzymmolekyl kan bearbeta många substratmolekyler per sekund — lovande nyheter för potentiella reningsapplikationer i verkliga miljöer.
Zooma in på de molekylära saxarna
Enzymer är naturens miniatyrmaskiner, och deras form avgör vad de kan göra. Forskarna använde toppmoderna prediktionsprogram, RoseTTAFold och AlphaFold, för att bygga tredimensionella modeller av PVA-klyvande enzymet, nu känt som en ny oxiderad PVA-hydrolas, eller OPH. Båda verktygen var ense om att enzymet har en klassisk ”alfa/beta-hydrolas”-veckning som återfinns i många biologiska saxar. I dess kärna finns ett kort motiv — ofta skrivet som Gly–X–Ser–X–Gly — som hjälper till att positionera en trio aminosyror (serin, aspartat och histidin) för att attackera kemiska bindningar. Datorsimuleringar visade oxiderade PVA-fragment som vilar i denna fåra, där den nyckelserin som sannolikt gör den första klyvningen i kedjan identifierades.
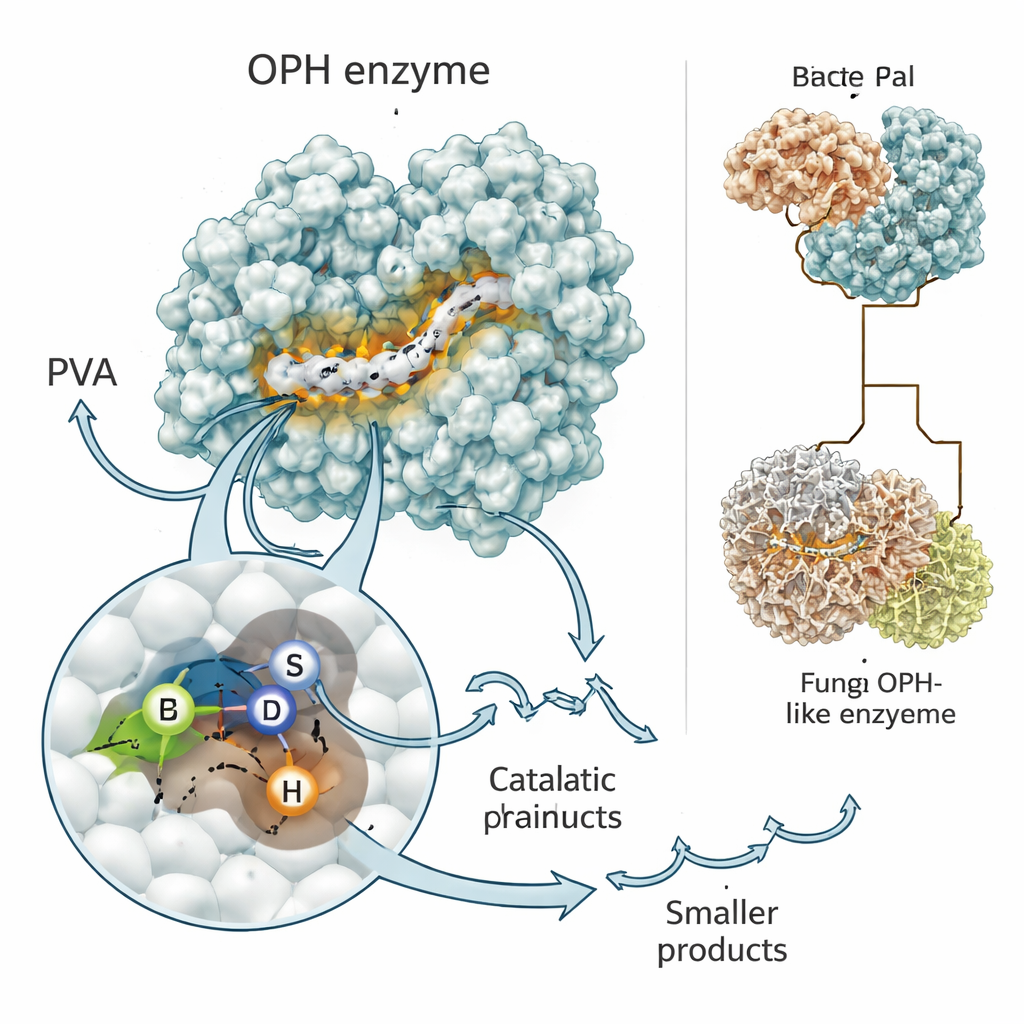
Signaler, switchar och evolutionära tvistar
Teamet undersökte också vilka delar av enzymet som är absolut nödvändiga för att det ska fungera i bakterien. Ett område nära proteinets början fungerar som en adresskod och dirigerar enzymet utanför cellen där själva PVA-polymeren finns. Ett annat område innehåller det aktiva motivet som greppar och klyver plastens kol–kol-bindningar. När forskarna konstruerade versioner av genen som saknade antingen signalsegmentet eller det aktiva motivationsmotivet producerade bakterien fortfarande RNA från genen men kunde inte längre effektivt smälta PVA. Genom att jämföra med många bakterier och svampar fann de släktingar till detta enzym som delar samma centrala ”klyvande” region men skiljer sig i tilläggsdelar, inklusive en anmärkningsvärd svampversion som förenar klyvdomänen med en inbyggd transportör — vilket antyder en ännu effektivare import-och-förtäringsstrategi i extrema miljöer som antarktiska stenar.
Vad detta betyder för att städa upp plastföroreningar
För icke-specialister är huvudbudskapet att forskare lär sig hur vissa mikrober naturligt bryter ner en till synes biologiskt nedbrytbar plast som annars ligger kvar alldeles för länge. Denna studie identifierar ett enskilt enzym, OPH från S. rhizophila QL-P4, som en kraftfull molekylär sax som verkar under milda förhållanden och riktar in sig på ett avgörande steg i PVA-nedbrytningen. Genom att förstå dess struktur, arbetsförhållanden och evolutionära släktingar kan forskare börja utforma bättre mikrobiella stammar eller enzymblandningar anpassade för reningsverk, industriella utflöden eller förorenade jordar. På längre sikt för oss dessa insikter närmare praktiska, biologibaserade lösningar för hantering av plastavfall istället för att låta det ansamlas i miljön.
Citering: Zhou, Y., Bold, N., Feng, J. et al. Mechanism and evolutionary divergence of a novel oxidized polyvinyl alcohol hydrolase in Stenotrophomonas rhizophila QL-P4. Sci Rep 16, 6411 (2026). https://doi.org/10.1038/s41598-026-37715-4
Nyckelord: polyvinylalkohol, biologisk nedbrytning, plastförorening, mikrobiella enzymer, bioremediering