Clear Sky Science · sv
Lipidmetabolisk klassificering av gliom
Varför fetter i hjärntumörer spelar roll
Hjärntumörer som kallas gliom hör till de farligaste cancerformerna, ändå kan patienter med till synes samma diagnos få mycket olika utfall. Denna studie ställer en till synes enkel fråga med stora konsekvenser: hur påverkar de sätt som tumörer använder fetter — kroppens lipider — deras aggressivitet, hur de svarar på behandling och om vi kan se dessa skillnader på vanliga hjärnscanningar? Genom att följa lipidanvändning i hundratals tumörer avslöjar författarna dolda undergrupper av gliom som kan förändra hur läkare förutspår prognos och utformar behandlingar.
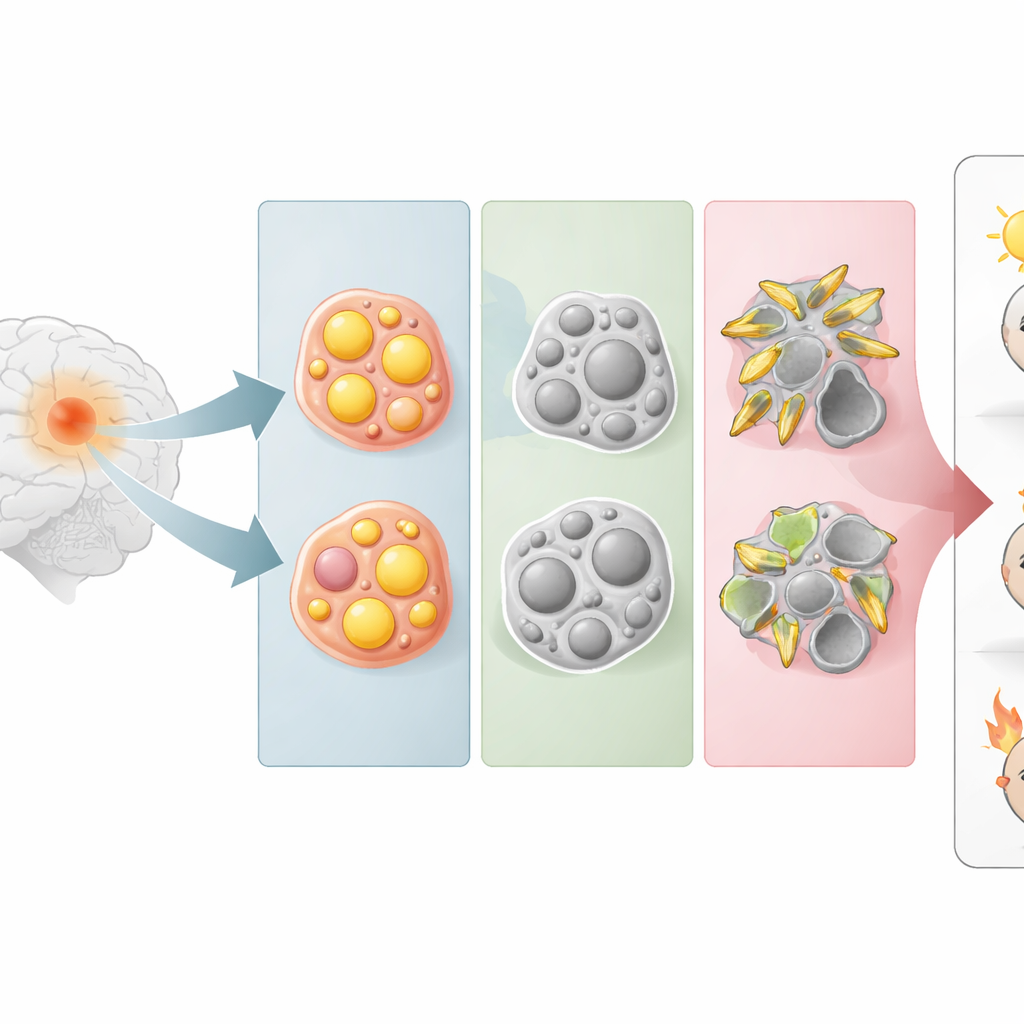
Tre dolda ansikten av samma hjärntumör
I stället för att utgå från hur tumörceller ser ut i mikroskop grupperade forskarna gliom efter hur starkt de aktiverar fem stora lipidvägar, inklusive de som hanterar steroidfetter, triglycerider och sfingolipider (viktiga byggstenar i cellmembran). Med hjälp av genaktivitetsprofiler från stora publika tumördatabaser fann de att gliom naturligt föll i tre grupper. En grupp lutade kraftigt mot steroidmetabolism (ST-typ), en annan mot triglyceridmetabolism (TC-typ) och en tredje mot sfingolipidmetabolism (SP-typ). Dessa metabola grupperingar korsar klassiska tumörkategorier och visar att celler med liknande lipidvanor kan finnas i annars olika gliom.
Från metabolism till patientutfall
Teamet undersökte sedan hur dessa tre fetthanteringsstilar förhåller sig till verkliga utfall. Patienter vars tumörer tillhörde ST-typen hade generellt längst överlevnad, och deras tumörer var oftare lågrastade och bar välkända gynnsamma genetiska förändringar. I andra änden av spektrumet var SP-typ tumörer vanligtvis höggradiga glioblastom som saknade skyddande mutationer och oftare förekom hos äldre patienter. Även efter statistisk justering för tumörgrad och centrala genetiska markörer förutsade medlemskap i SP-typen fortfarande en avsevärt sämre prognos, vilket tyder på att hur tumören hanterar sfingolipider fångar en oberoende riskdimension som standardtester missar.
En fientlig närmiljö i hjärnan
För att gå djupare undersökte författarna tumörmikromiljön — blandningen av immunceller, blodkärl och stödjevävnad runt cancern. SP-typ tumörer uppvisade en tät och konfliktfylld immunmiljö, med både angreppsorienterade och suppressiva immunceller närvarande, samt starka signaler som dämpar effektiva antitumörsvar. Banor kopplade till snabb celltillväxt, invasion, ny blodkärlsbildning, ärrbildning och inflammation var alla mer aktiva i denna subtype. Mått som uppskattar hur tumörer svarar på strålbehandling antydde att SP-typ gliom är mest resistenta mot radioterapi, i linje med deras sämre överlevnad. I kontrast framstod ST-typ tumörer som mer ”lugnare”, med lägre nivåer av dessa aggressiva egenskaper.
Läsa tumörmetabolism från MR-bilder
Eftersom kirurgiskt borttagande av tumörvävnad är invasivt och inte alltid möjligt undersökte forskarna om standard magnetresonansavbildning (MRI) kunde antyda en tumörs lipidbeteende. De extraherade mer än tvåtusen subtila textur- och formegenskaper från två vanliga MRI-sekvenser och tränade en maskininlärningsmodell för att särskilja SP-typ från alla andra tumörer. Modellen presterade väl både i ett sjukhusbaserat träningsset och i ett oberoende publikt valideringsset och separerade korrekt SP-typ tumörer betydligt oftare än slumpen. Detta tyder på att det metabola fingeravtrycket av en särskilt aggressiv gliomsubtyp lämnar ett detekterbart avtryck på rutinmässiga hjärnscanningar.
En nyckelgen i centrum för ett aggressivt nätverk
För att gå från breda banor till konkreta mål sökte teamet efter gener som var centrala i lipidrelaterade nätverk, starkt överaktiva i SP-typ tumörer, kopplade till sämre överlevnad och kapabla att särskilja SP-typ tumörer från andra. Tre gener — GLA, GLB1 och HSD3B7 — uppfyllde alla kriterier. Samtliga var mer aktiva i SP-typ gliom och bildade tillsammans ett kraftfullt diagnostiskt signum. Författarna fokuserade på HSD3B7, vars roll i hjärntumörer till stor del varit outforskad. Vävnadsfärgning från 100 gliompatienter visade att HSD3B7-proteinet var högre i mer avancerade och mer maligna tumörer, och patienter vars tumörer hade höga nivåer av detta protein levde signifikant kortare.
Hur en lipidgen omformar tumörekosystemet
Encellsanalyser, som profilerar individuella celler inom tumörer, visade att HSD3B7 är aktiv inte bara i cancerceller utan också i flera typer av immunceller och stödjeceller. Höga nivåer av denna gen var associerade med ett nätverk av signaler som främjar blodkärlsbildning, kronisk inflammation och immunevasion. Kommunikation mellan vissa skyddande celltyper tycktes försvagad, medan självförstärkande kretsar inom tumörstödceller stärkts. Tillsammans tyder dessa mönster på att förhöjd HSD3B7-aktivitet bidrar till att skapa och upprätthålla en fientlig mikromiljö som gynnar tumörtillväxt och resistens mot behandling.
Vad detta betyder för patienter och framtida vård
I praktiska termer visar arbetet att gliom meningsfullt kan delas in i tre lipidbaserade subtyper, där den sfingolipid-tunga SP-typen framstår som särskilt farlig och behandlingsresistent. Dessa skillnader är inte bara teoretiska: de kan avläsas från rutinmässiga MR-bilder med avancerad bildanalys och spåras till specifika gener som HSD3B7 som kan bli framtida läkemedelsmål. Även om experimentella studier fortfarande behövs för att testa om blockering av dessa lipidvägar kan bromsa tumörer eller förbättra strålbehandling, erbjuder studien en ny metabolisk lins för att betrakta hjärncancrar och förflyttar fältet närmare mer personligt och biologiskt grundade behandlingsbeslut.
Citering: Tu, S., Zhang, P., Chi, X. et al. Lipid metabolism classification of gliomas. Sci Rep 16, 8219 (2026). https://doi.org/10.1038/s41598-026-37697-3
Nyckelord: gliom, lipidmetabolism, hjärntumöravbildning, radiomik, tumörmikromiljö