Clear Sky Science · sv
Högt fetthaltigt kost omformar genregleringsnätverk i preoptiska området
Varför din hjärna spelar roll vid diabetes
De flesta ser diabetes som ett problem i bukspottkörteln och blodsockret, men hjärnan är djupt engagerad också. Den här studien undersöker hur en kost rik på fett och en kraftfull experimentell behandling förändrar genaktiviteten i ett litet men betydelsefullt hjärnområde som kallas preoptiska området. Genom att kartlägga vilka hjärnceller som ”återställs” när diabetes går i remission hoppas forskarna peka ut nya terapier som utnyttjar hjärnans egen förmåga att hjälpa till att reglera blodsockret.
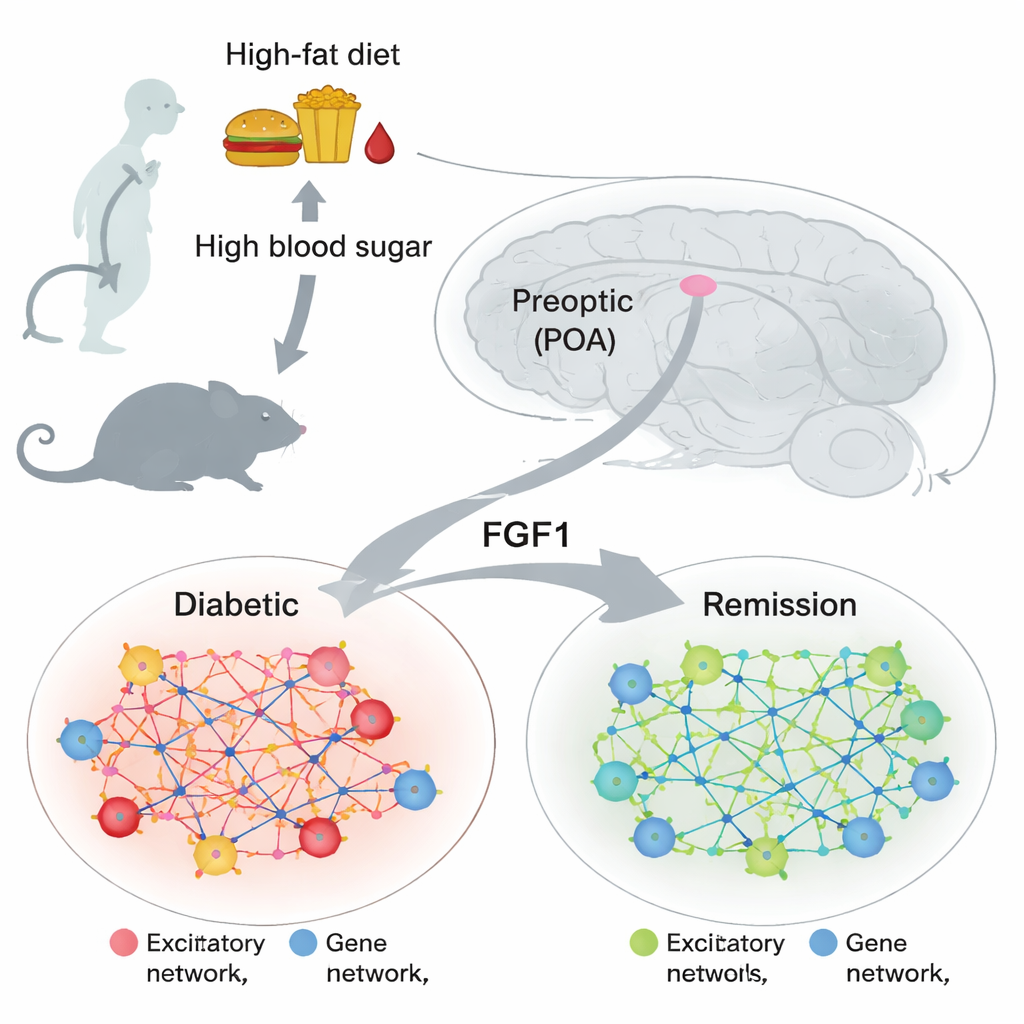
En liten hjärnknut med stort metabolt inflytande
Det preoptiska området ligger längst fram i hypotalamus, en del av hjärnan som hjälper till att reglera kroppstemperatur, sömn, födointag och hormonsignaler. Tidigare arbete visade att celler i denna region kan påverka hur kroppen hanterar glukos och svarar på värme, men deras roll i diabetes var dåligt förstådd. Samtidigt visade andra studier att en enda dos av ett protein kallat fibroblasttillväxtfaktor 1 (FGF1), givet i hjärnan, kan föra feta diabetiska möss i långvarig remission. Det väckte en nyckelfråga: vilka hjärnceller och genprogram ändras när blodsockret normaliseras, och dyker liknande förändringar upp i det preoptiska området?
Läsa genaktivitet cell för cell
För att besvara detta använde teamet single-cell RNA-sekvensering, en teknik som mäter vilka gener som är aktiva i tusentals enskilda celler samtidigt. De återanalyserade en befintlig datamängd från möss vars diabetes hade gått i remission efter FGF1-behandling, med fokus på nervceller i hypotalamus. Med statistiska verktyg identifierade de grupper av gener som steg eller sjönk i samklang när djuren gick från diabetiskt till remissionstillstånd. Dessa ”remissionsmoduler” fungerar som återhämtningens fingeravtryck: i stället för att följa en gen i taget fångar de koordinerade skift över många gener inom särskilda neuron-typer.
Högfettsdiet, hjärnceller och nedjusterad energianvändning
Forskarna jämförde sedan dessa remissionsmoduler med genaktivitet i en annan datamängd som provtagit celler från det preoptiska området hos normala möss. De delade först upp neuroner i två breda klasser: excitatoriska celler, som tenderar att öka aktivitet i sina kretsar, och inhibitoriska celler, som dämpar den. Hos diabetiska möss behandlade med FGF1 visade båda typerna av neuroner generella minskningar i gener kopplade till energiproduktion—särskilt de som är involverade i oxidativ fosforylering, cellulär respiration och det mitokondriella maskineriet som driver aktiva celler. I excitatoriska neuroner var en stor ”turkos” genmodul kopplad till energianvändning och synaptisk aktivitet starkt nedreglerad i remission, vilket antyder att dessa celler blir mindre metaboliskt krävande när blodsockret bringas under kontroll.
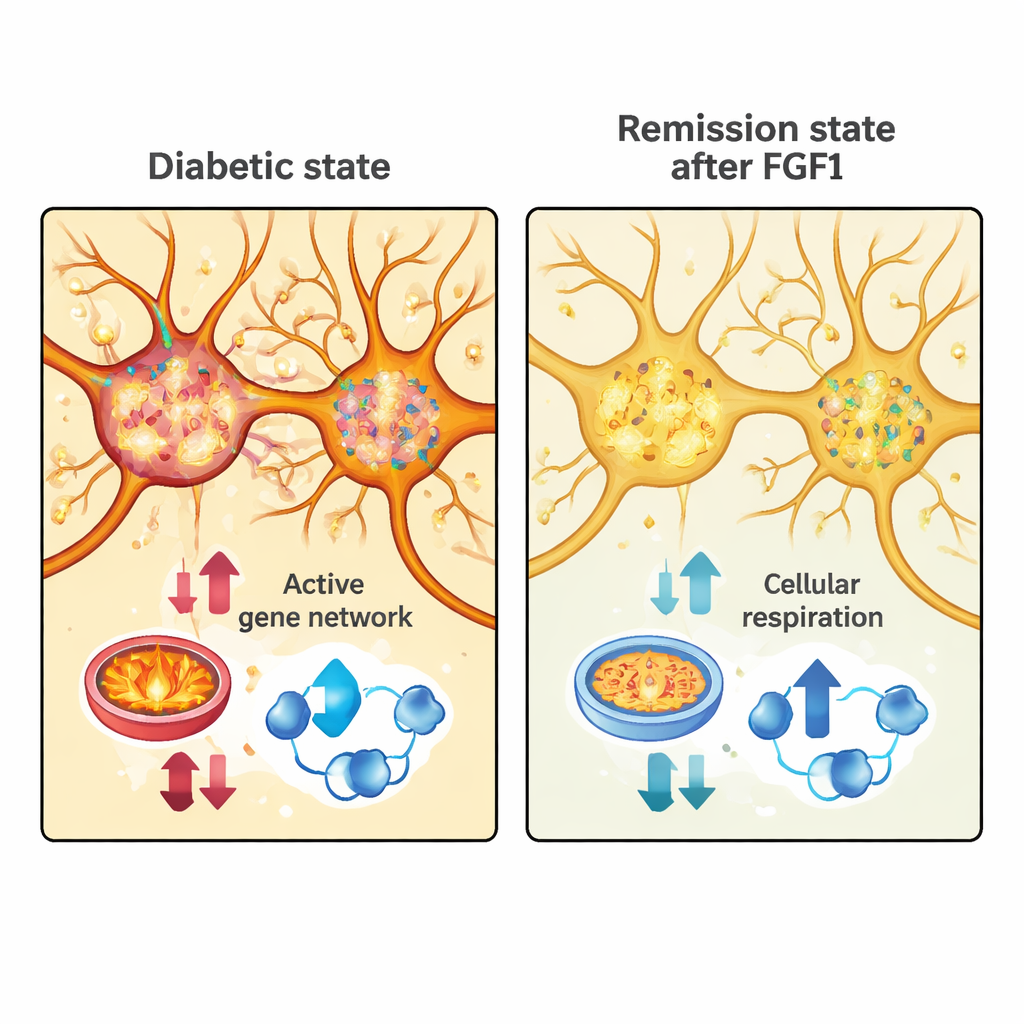
Spåra remissionssignaturer till specifika neurongrupper
Därefter frågade teamet om dessa remissionsrelaterade genmönster stämde överens med särskilda cellpopulationer i det preoptiska området. Genom att datorbaserat slå samman de två datamängderna fann de att vissa preoptiska neuronkluster uttryckte många av samma gener som förändrades vid FGF1-inducerad remission. De lyfte fram flera gener—såsom Trpc4, Dgkg och Ryr3—som befann sig i korsningen för dessa analyser. Med en mycket känslig mikroskopimetod kallad RNAscope visade de att dessa gener faktiskt uttrycks i distinkta zoner i musens preoptiska område, främst i dorsala subregioner. Detta validerar dem som verkliga markörer för specifika neurongrupper som kan delta i hjärnans respons på metabol sjukdom.
Vad detta betyder för framtida diabetesbehandlingar
För icke-specialister är slutsatsen att diabetes inte bara är ett blodsockerproblem—det är också ett problem i hjärnans nätverk. Studien visar att när diabetes går i remission hos möss, skiftar vissa preoptiska neuroner till ett lägre energitillstånd och förändrar sin genaktivitet på koordinerade sätt. Genom att definiera dessa remissionsmoduler och koppla dem till konkreta celltyper och markörgener ger arbetet en färdplan för framtida experiment: forskare kan nu rikta in sig på dessa specifika neuroner för att testa hur de påverkar glukoskontroll, fetma och relaterade komplikationer. På längre sikt kan en bättre förståelse av dessa hjärncirkuiter bidra till behandlingar som kompletterar eller till och med kringgår sviktande organ genom att utnyttja hjärnans inbyggda kontroll över ämnesomsättningen.
Citering: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Nyckelord: hjärnan och diabetes, preoptiska området, högt fetthaltigt kost, gennätverk, FGF1-remission