Clear Sky Science · sv
En metod för att upptäcka strukturella varianter med Hi-C-kontaktmatris och neurala nätverk
Varför DNA:s 3D-böjning spelar roll
Vårt DNA avbildas ofta som en enkel sträng av bokstäver, men inne i varje cell veckas det till en komplex tredimensionell form. När stora bitar av denna sträng raderas, vänds eller flyttas—förändringar kallade strukturella varianter—kan de störa gener och bidra till cancer. Denna studie presenterar VarHiCNet, ett nytt artificiellt intelligenssystem som läser 3D-kartor över DNA-fällning och upptäcker dessa riskfyllda storskaliga förändringar mer noggrant än befintliga verktyg, vilket erbjuder ett nytt sätt att studera cancergenom och andra sjukdomar.
Att se genom genomeförändringar i 3D-kontaktkartor
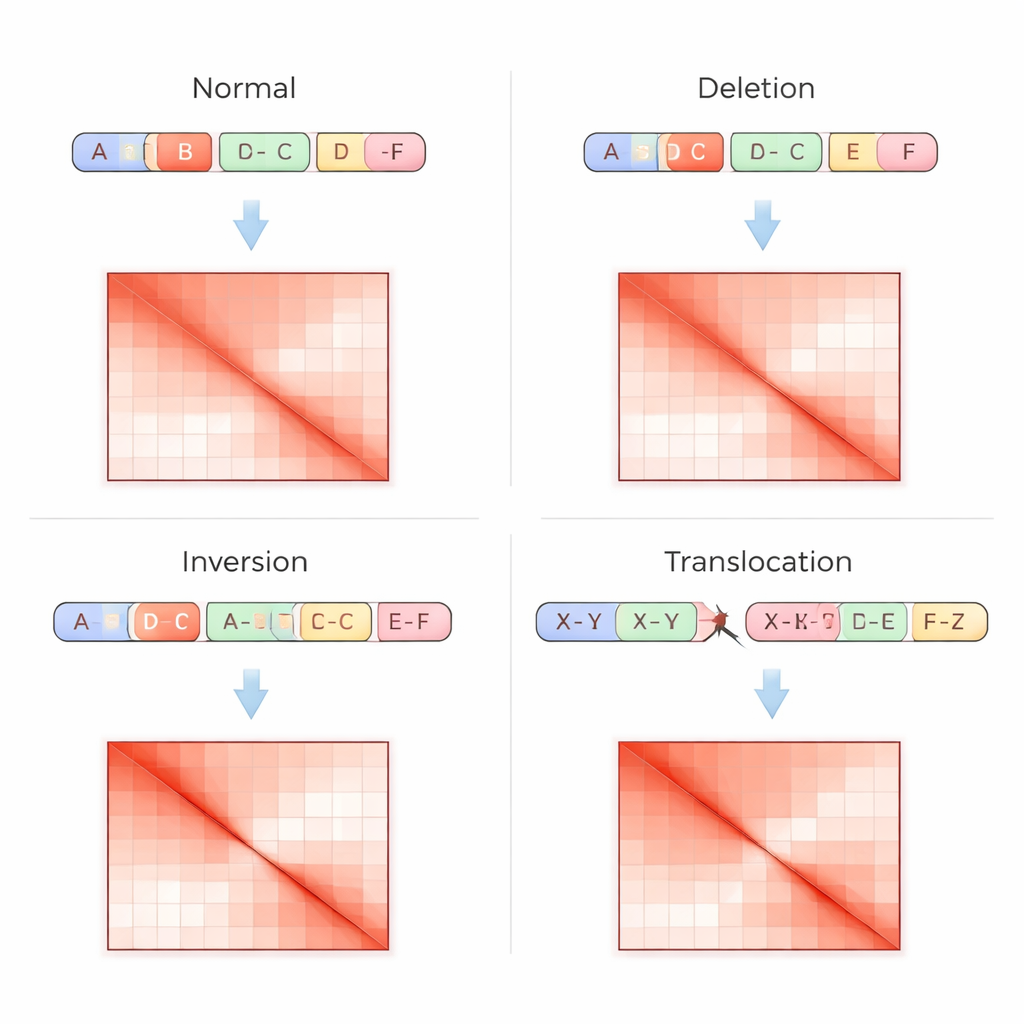
Traditionella genomanalyser läser DNA som en rak sekvens, vilket gör det svårt att upptäcka komplexa omarrangemang, särskilt i repetitiva regioner eller när segment flyttas utan att deras kopietal ändras. Hi-C-tekniken angriper problemet annorlunda: den mäter hur ofta avlägsna delar av DNA fysiskt rör vid varandra inne i kärnan och sparar dessa kontakter som ett rutnät, eller en kontaktmatris, där starkare interaktioner syns som klarare punkter. Strukturella varianter lämnar särskilda fingeravtryck i dessa matriser—såsom försvunna ränder där en region tagits bort, speglade mönster när ett segment vänds, eller off-diagonal-hetar där två kromosomer fusionerats. VarHiCNet är utformat för att automatiskt känna igen dessa visuella mönster.
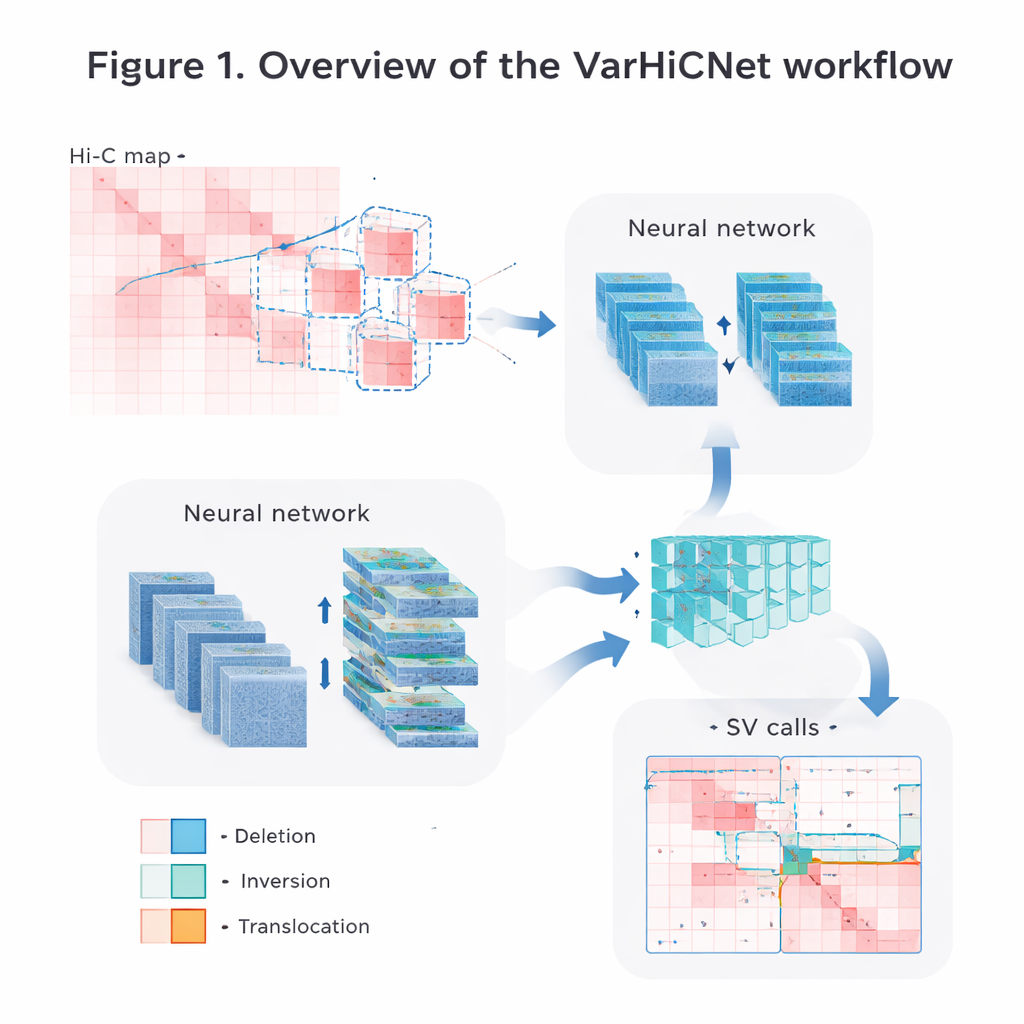
Att göra genomkartor till bilder för AI
Författarna omvandlar de råa Hi-C-kontaktdatat till bilder som datorseendesystem enkelt kan bearbeta. Först normaliserar de matriserna noggrant för att korrigera den naturliga minskningen i kontaktfrekvens när DNA-segment blir längre ifrån varandra, samtidigt som både närliggande och långdistansinteraktioner bevaras. Därefter skannar de varje kromosom med överlappande fyrkantiga fönster och klipper ut många mindre submatriser. Varje submatris skalas till en standardiserad 800 × 800-pixel färgbild, där olika kontaktstyrkor mappas till rödtonade intensiteter över tre färgkanaler. Denna bildliknande representation gör det möjligt för modellen att återanvända kraftfulla tekniker som ursprungligen utvecklats för att känna igen objekt i fotografier.
Låna trick från objektdetektion
VarHiCNet behandlar varje möjlig strukturell variant som om det vore ett ”objekt” i en bild. Den bygger på ett modernt objektdetekteringsramverk kallat RT-DETR, som använder en kombination av konvolutionella neurala nätverk och Transformers för att framhäva viktiga regioner. Ett ResNet-backbone extraherar först flerskaliga funktioner: ytliga lager behåller fin detalj som behövs för att exakt lokalisera brytpunkter, medan djupare lager fångar bredare mönster som signalerar stora händelser. En funktionsfusionsmodul blandar sedan information från flera lager så att både lokala och globala ledtrådar bevaras. En annan anpassad block, inspirerad av spatial pyramid pooling, justerar hur mycket av omgivningen modellen ”ser” på en gång, vilket gör den känslig för varianter som sträcker sig från relativt korta till mycket långa DNA-avsnitt.
Från kandidatregioner till precisa varianttyper
När VarHiCNet har föreslagit kandidatregioner i Hi-C-bilden måste den förfina dem till exakta brytpunkter och specifika varianttyper, såsom deletioner, inversioner, duplikationer eller translokationer. För att göra detta zoomar systemet in på grannskapet kring varje förutsagd brytpunkt och reducerar komplexiteten med en matematisk teknik kallad huvudkomponentanalys (PCA), som framhäver var kontaktmönstret ändras skarpt. Dessa kompakta representationer matas sedan in i en Transformer-baserad klassificerare som lär sig subtila skillnader i de lokala mönstren för varje variantkategori. Resultatet är ett detaljerat anrop för varje händelse: var den sker i genomet och vilken typ av strukturell förändring den representerar.
Prestanda över olika cancercellinjer
Forskarlaget testade VarHiCNet på Hi-C-data från sex olika mänskliga cancercellinjer, som omfattar blod-, bröst-, hjärn-, njur-, lunga- och prostata-tumörer. Genom att använda en högkonfidenslista över kända strukturella varianter som guldstandard jämförde de sin metod mot flera ledande verktyg som också analyserar Hi-C-data. Både för händelser inom kromosomer och mellan kromosomer uppnådde VarHiCNet generellt högre eller jämförbara F1-poäng, vilket betyder att den balanserade känslighet och noggrannhet bättre än andra tillvägagångssätt. Den var särskilt stark på att upptäcka balanserade translokationer och inversioner—omarrangemang som ofta lämnar lite spår i standardsekvensering men som ger tydliga 3D-fällningssignaturer. Författarna visade också att deras designval, såsom bildupplösning och funktionsfusionsmoduler, konsekvent förbättrade prestandan i kontrollerade tester.
Vad detta innebär för förståelsen av sjukdom
I praktiska termer ger VarHiCNet forskare ett smartare sätt att ”titta” på hur genomet veckas i 3D och att upptäcka stora, sjukdomsrelaterade omarrangemang som kan missas av konventionell sekvensering ensam. Genom att omvandla komplexa kontaktkartor till bilder och använda moderna vision-liknande neurala nätverk kan metoden upptäcka och kategorisera många typer av strukturella variationer med hög tillförlitlighet över olika cancercelltyper. Även om den fortfarande har svårigheter med mycket små eller starkt intrasslade förändringar och är beroende av riklig träningsdata, pekar VarHiCNet mot en framtid där 3D-genomarkitektur blir en rutindel av hur vi läser, tolkar och slutligen riktar in oss på de genetiska förändringar som ligger bakom cancer och andra sjukdomar.
Citering: Shen, J., Wang, H., Zhai, H. et al. A method for structural variant detection using Hi-C contact matrix and neural networks. Sci Rep 16, 7324 (2026). https://doi.org/10.1038/s41598-026-37678-6
Nyckelord: strukturell variation, Hi-C, deep learning, cancergenomik, 3D-genom