Clear Sky Science · sv
Identifiering av skadliga varianter i hela transkriptomet i kandidatgener kopplade till bovin paratuberkulos
Gömda gener bakom en kostsam kohälsa
Bovin paratuberkulos, även kallad Johnes sjukdom, underminerar tyst hälsa och produktivitet i mjölkbesättningar världen över, kostar bönder hundratals miljoner dollar varje år och väcker oro för kopplingar till mänskliga tarmstörningar. Denna studie skrapar under ytan i genomet hos Holsteinkor för att ställa en enkel men avgörande fråga: vilka skillnader i deras gener kan hjälpa vissa djur att motstå infektionen medan andra faller offer? Genom att läsa RNA — genernas arbetskopior — i blod och tarmvävnad spårade forskarna hur subtila DNA-förändringar i viktiga immungener kan styra sjukdomens förlopp.
Varför denna kosjukdom spelar roll
Paratuberkulos orsakas av bakterien Mycobacterium avium underarten paratuberculosis (MAP). Kor blir vanligen infekterade tidigt i livet, men symtomen visar sig ofta först år senare. I de tysta och subkliniska stadierna ser djuren friska ut men kan utsöndra låga nivåer bakterier och ge mindre mjölk. I kliniska stadier utvecklar de kronisk diarré, kraftig viktnedgång och stora droppar i mjölkproduktion. Infektionsnivåer på besättningsnivå kan överstiga 50 % i många regioner, inklusive delar av Europa och Nordamerika, vilket skapar ett ekonomiskt och djurvälfärdsmässigt problem. Eftersom bakterien också kan fungera som en miljömässig trigger för mänskliga inflammatoriska sjukdomar som Crohns sjukdom, finns ett växande tryck att förbättra kontrollstrategier hos nötkreatur.
Att läsa det arbetande genomet
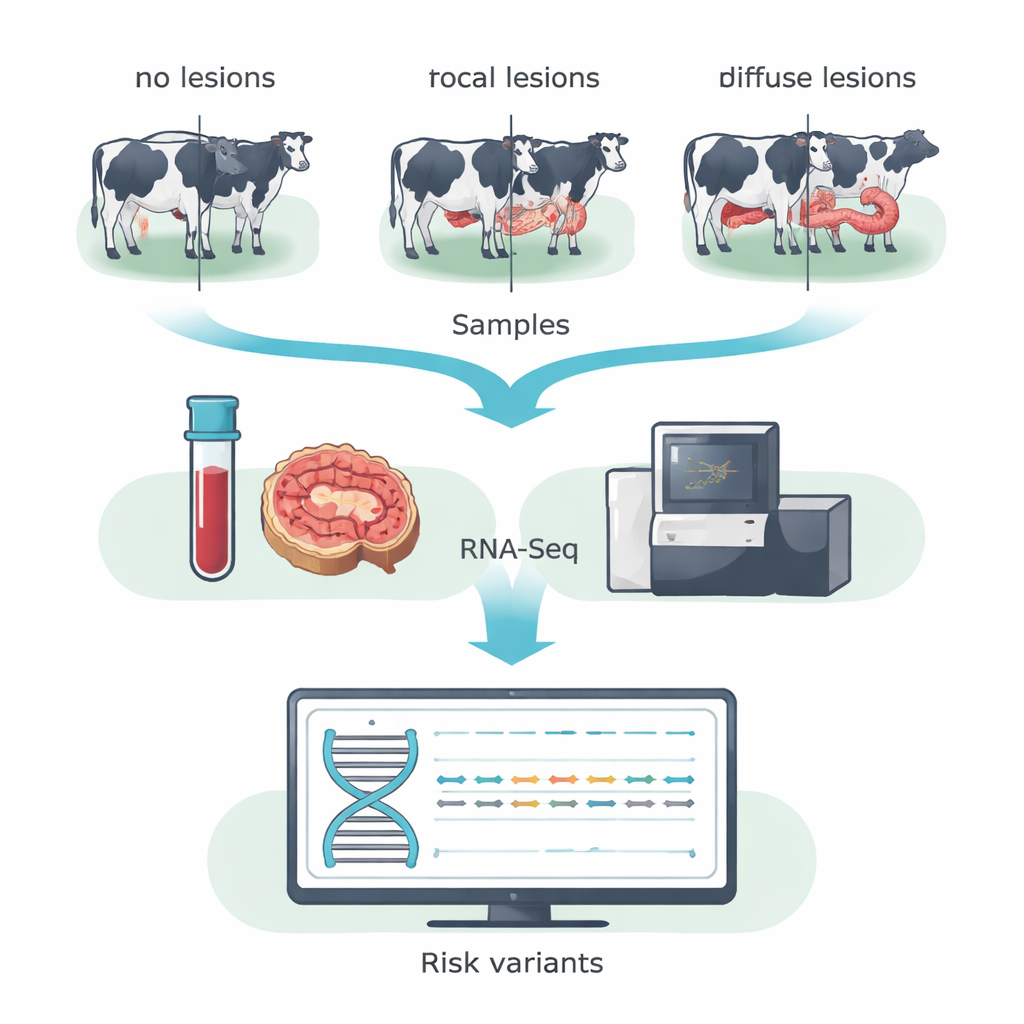
I stället för att skanna hela DNA-sekvensen använde teamet RNA-sekvensering (RNA-Seq) för att fokusera på de gener som faktiskt är aktiva i djuret. De samlade blod och prover från ileocecala valvet — en tarmregion starkt påverkad av MAP — från 14 Holsteinkor i en spansk mjölkbesättning. Baserat på mikroskopisk undersökning av tarmvävnader grupperades korna i tre kategorier: djur utan påvisbara lesioner, djur med små, lokaliserade (fokala) lesioner typiska för lång subklinisk infektion, och djur med svåra, utbredda (diffusa) lesioner kopplade till klinisk sjukdom. Genom att slå samman data från blod och tarm inom varje grupp ökade forskarna sin förmåga att upptäcka enkelbokstavsförändringar i DNA i uttryckta gener, så kallade kodande SNP:er.
Att hitta skadliga förändringar i viktiga immungener
Av hundratusentals varianter fokuserade teamet på dem som förändrar proteinsekvensen och förväntas skada proteinfunktionen — så kallade deleterious-varianter. De tillämpade strikta filter för att säkerställa hög tillförlitlighet och använde etablerade prediktionsverktyg för att flagga riskfyllda förändringar. Denna gallringsprocess avslöjade 31 sådana varianter unika för kor utan lesioner, 15 unika för kor med fokala lesioner och 31 unika för kor med diffusa lesioner. Många av dessa föll i gener som styr hur immunceller känner igen och rensar infektioner, reglerar celldöd och hanterar metabolism. Ett framstående exempel var BOLA-genfamiljen, den bovina motsvarigheten till major histocompatibility complex klass II, som hjälper immunceller att presentera bakteriefragment för T-celler. Olika potentiellt skadliga varianter i BOLA hittades i alla tre kokategorier, vilket tyder på att specifika BOLA-varianter kan luta djur mot resistens, kontrollerad infektion eller skadlig inflammation.
Från DNA-varianter till sjukdomsvägar
För att förstå vad dessa genförändringar kan innebära i praktiken undersökte forskarna vilka biologiska vägar som var överrepresenterade i varje grupp. Kor utan lesioner visade förändrade varianter i gener kopplade till antigenbearbetning, vesikeltrafikering och tarmens immunbalans, inklusive BOLA, AP3B1 och CHGA. Dessa förändringar kan främja effektiv nedbrytning av bakterier inom immunceller och en stabil tarmmiljö som begränsar skada. Hos kor med fokala lesioner klustrade skadliga varianter i gener (ORMDL3 och KANK2) som dämpar programmerad celldöd och finjusterar cellmetabolismen, vilket potentiellt hjälper värden att hålla bakterienivåer låga under en lång, subklinisk fas. Hos kor med diffusa lesioner pekade de påverkade generna mot överaktiva immunsystemsvägar såsom Th1/Th2-cellernas differentiering och antigenpresentation, tillsammans med galla-transport och läkemedelsresponsvägar. Här kan förändrade BOLA-familjegener driva en stark, ibland självskadande inflammatorisk reaktion, vilket påminner om mönster som ses i många mänskliga autoimmuna och inflammatoriska sjukdomar.
Ledtrådar för att avla mer motståndskraftiga besättningar
Utöver att belysa hur olika genetiska varianter formar immunsvaret mot MAP kopplade studien också dessa riskfyllda förändringar till kända områden i det bovina genomet som är associerade med hälsotrait, inklusive känslighet för paratuberkulos och andra infektioner. Även om dessa resultat fortfarande kräver validering i större besättningar och ännu inte kan användas som fristående diagnostiska markörer, erbjuder de en lovande katalog av kandidatvarianter och gener. Enkelt uttryckt antyder arbetet att vissa kor bär genvarianter som hjälper dem att tyst kontrollera infektion, medan andra bär varianter som gynnar okontrollerad inflammation och allvarlig sjukdom. I framtiden skulle sådan information kunna stödja selektiv avel och genetiska tester som skiftar besättningar mot större naturlig resistens, vilket minskar både ekonomiska förluster och behovet av intensiv sjukdomshantering.
Citering: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
Nyckelord: bovin paratuberkulos, Johnes sjukdom genetik, immunitet hos mjölkkor, RNA-sekvensering, avel för sjukdomsresistens