Clear Sky Science · sv
Utnyttja medicinsk avbildning och djupinlärning för diagnostik av bröstcancer med hjälp av histopatologiska bilder
Varför tidig upptäckt spelar roll
Bröstcancer är en av de ledande orsakerna till cancerdöd bland kvinnor globalt, men prognosen förbättras dramatiskt när sjukdomen upptäcks tidigt. Läkare diagnostiserar vanligen bröstcancer genom att granska tunna vävnadsskivor i mikroskop, en process som kallas histopatologi. Dessa bilder innehåller riklig information om huruvida celler är ofarliga eller farliga, men att läsa dem är tidskrävande och kan variera mellan olika specialister. Denna studie undersöker hur modern artificiell intelligens kan hjälpa patologer att upptäcka bröstcancer snabbare och mer konsekvent, vilket potentiellt kan ge patienter snabbare besked och effektivare behandlingsalternativ.
En närmare titt på vävnadsbilder
I mikroskopet delar inte bröstvävnad upp sig i tydliga kategorier som ”frisk” och ”cancerös”. Celler överlappar, färger varierar mellan laboratorier, och subtila förändringar i form eller struktur kan ha avgörande betydelse. Traditionella datorstödda system hade svårt med denna komplexitet eftersom ingenjörer var tvungna att manuellt utforma de kännetecken som datorn skulle leta efter, och små förändringar i färgning eller bildkvalitet kunde störa dem. Djupinlärning, en gren av artificiell intelligens som lär sig mönster direkt från data, har nyligen förändrat hur datorer tolkar bilder, inklusive medicinska skanningar. Författarna bygger vidare på denna utveckling för att utforma ett system anpassat till den röriga verkligheten i bröstvävnadssnitt.
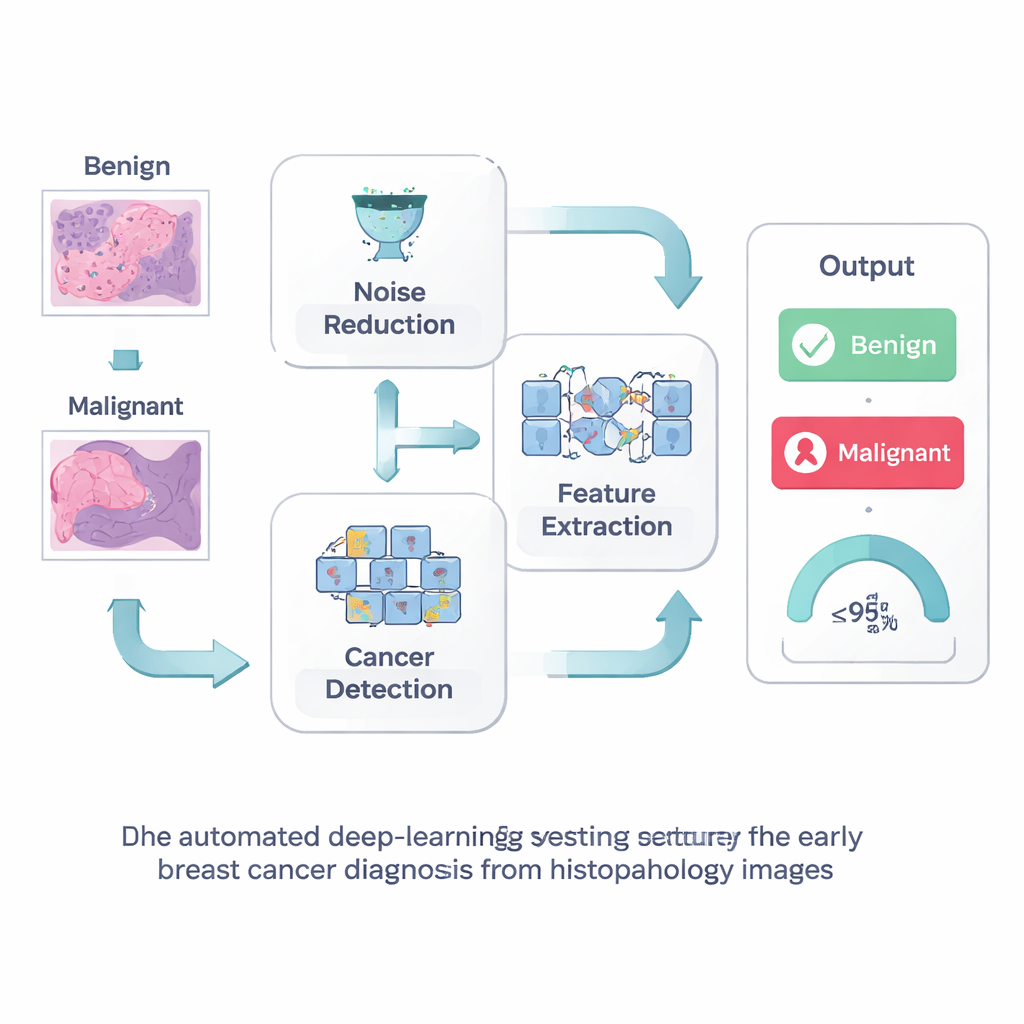
Rensa bilden innan den tolkas
Det första steget i deras metod är enkelt men kraftfullt: rensa upp bilden innan en dator får tolka den. Histopatologiska preparat innehåller ofta visuellt ”brus” från färgnings- och avbildningsprocessen som kan dölja de fina strukturer som signalerar tidig cancer. Forskarna använder en teknik kallad Wiener‑filtrering, som slätar ut slumpmässiga prickar samtidigt som skarpa kanter och små detaljer, såsom cellgränser och små kluster, bevaras. Genom att ge datorn en tydligare bild hjälper detta steg till att undvika både missade cancerfall och falska larm som skulle kunna leda till onödiga undersökningar för patienter.
Lära datorn vad den ska uppmärksamma
Därefter använder teamet en avancerad djupinlärningsmodell känd som SE‑ResNet för att analysera de rengjorda bilderna. I enkla termer skannar modellen preparatet bit för bit och bygger gradvis upp ett internt ”vokabulär” av visuella mönster: hur normala kanaler ser ut, hur tumörceller grupperar sig och hur texturer förändras när cancer blir mer aggressiv. En inbyggd uppmärksamhetsmekanism hjälper nätverket att framhäva de mest informativa bildkanalerna och tona ner irrelevant bakgrund. Detta gör modellen mer känslig för subtila, sjukdomsrelaterade mönster samtidigt som beräkningarna hålls tillräckligt effektiva för att kunna köras på verklig sjukhushårdvara.
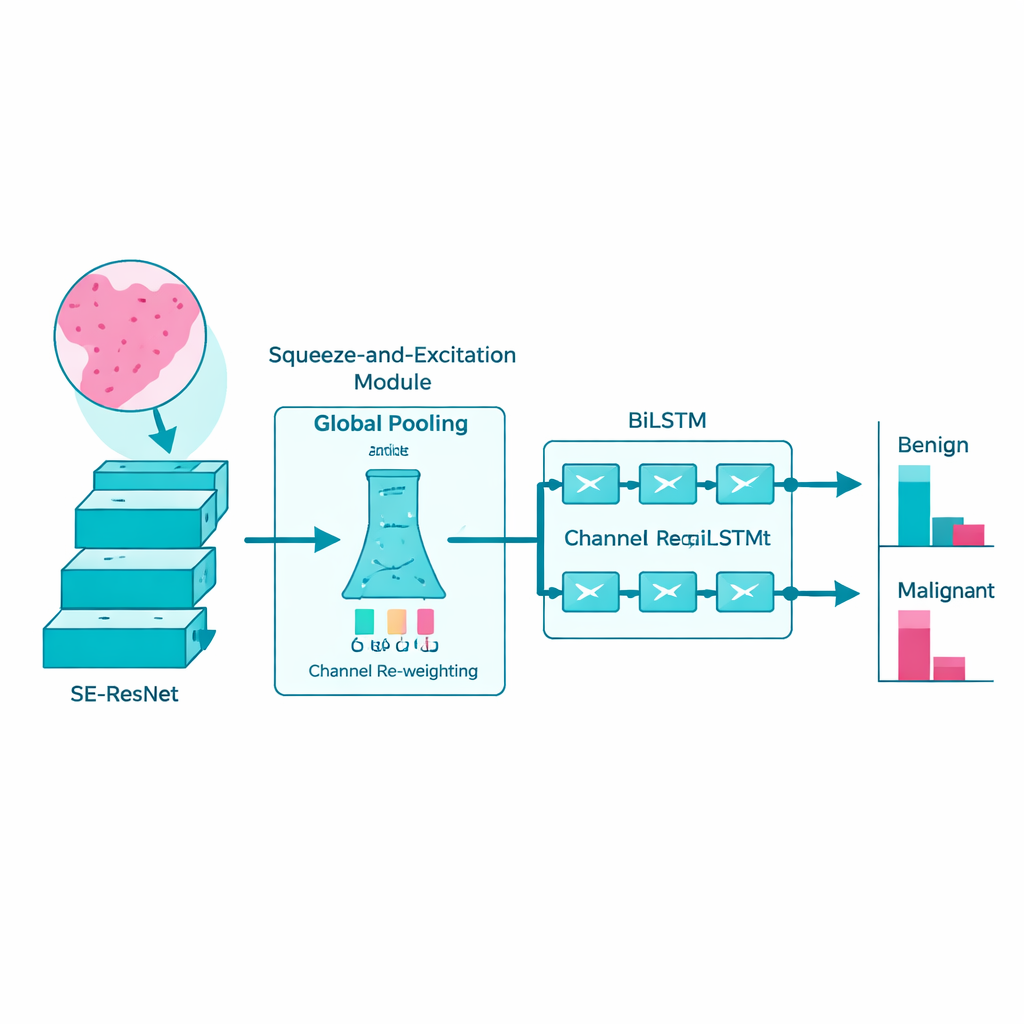
Följa mönster över ytan som en berättelse
I stället för att behandla varje vävnadsfläck som en isolerad ögonblicksbild, inser forskarna att sjukdomstecken ofta utvecklas som en berättelse över preparatet. För att fånga detta matar de funktioner som extraherats av SE‑ResNet in i ett bi‑direktionellt long short‑term memory‑nätverk, eller BiLSTM. Denna typ av modell är utformad för att förstå sekvenser: den ser hur mönster förändras från en region till nästa, både framåt och bakåt, ungefär som att läsa en mening i båda riktningar för att förstå dess fulla innebörd. Genom att lära sig dessa rumsliga relationer blir BiLSTM bättre på att skilja godartade förändringar från verkligt maligna.
Hur väl systemet fungerar i praktiken
Författarna testade hela sin pipeline—brusreducering, funktionsinlärning och sekvensmodellering—på stora offentliga samlingar av bröstvävnadsbilder, inklusive det ofta använda BreakHis‑datasetet. De delade upp data i tränings‑ och testgrupper i olika proportioner och jämförde sin metod med många etablerade djupinlärningsmodeller. I dessa experiment klassificerade deras system korrekt godartade mot maligna prover i nästan 99 % av fallen, och överträffade konkurrerande metoder samtidigt som det också körde snabbare. Modellen bibehöll god prestanda vid olika förstoringar av vävnaden, vilket tyder på att den kan anpassa sig till preparat framställda under skiftande förhållanden. Studien noterar dock också begränsningar: datamängderna är fortfarande måttliga i storlek, modellen fokuserar på ett enkelt tvåklassbeslut snarare än detaljerade tumörsubtyper, och den är ännu inte bevisad i verkliga kliniska arbetsflöden.
Vad detta innebär för patienter och läkare
För en lekman är huvudbudskapet att datorer blir mycket bättre på att läsa mikroskopbilder av bröstvävnad och markera misstänkta områden. Det föreslagna systemet ersätter inte patologen; det fungerar snarare som en mycket uppmärksam assistent som framhäver regioner som sannolikt är cancerösa och ger en andra åsikt med mycket hög noggrannhet. Om metoden valideras i större och mer varierade patientgrupper skulle sådana verktyg kunna förkorta tiden till diagnos, minska risken att en liten cancer missas och hjälpa överbelastade sjukhus att hantera växande mängder fall. Framtida arbete måste testa metoden på mer varierade preparat och integrera den i vardagliga laboratorierutiner, men denna studie visar att noggrant utformade djupinlärningssystem kan vara en kraftfull allierad i kampen mot bröstcancer.
Citering: Nagalakshmi, V., Ahammad, S.H. Leveraging medical imaging and deep learning for diagnosis of breast cancer using histopathological images. Sci Rep 16, 6236 (2026). https://doi.org/10.1038/s41598-026-37663-z
Nyckelord: diagnostik av bröstcancer, histopatologiska bilder, djupinlärning, medicinsk avbildning, datorstödd detektion