Clear Sky Science · sv
Typ I-interferon-signalering definierar ett nytt sjukdomssignatur i xeroderma pigmentosum C mänskliga keratinocyter
Varför solljus kan vara så farligt för vissa personer
För de flesta av oss innebär solljus värme och vitamin D. Men för personer med en sällsynt genetisk sjukdom kallad xeroderma pigmentosum C (XP‑C) kan även måttligt dagsljus orsaka svåra hudskador och en extrem risk för hudcancer. Denna studie går bortom det välkända problemet med DNA-reparation i XP‑C och avslöjar ett dolt lager av överaktiv, immunsystemliknande signalering inne i deras hudceller, vilket ger nya ledtrådar till varför deras hud är så sårbar och inflammerad efter solexponering.
När DNA-reparationen misslyckas i huden
Våra hudceller reparerar ständigt DNA‑skador orsakade av ultraviolett B (UVB)‑strålning från solen. Ett protein kallat XPC är en av de första ”sensorerna” som upptäcker UV‑inducerade skador och sätter igång ett stort reparationslag. Vid XP‑C förstörs detta tidiga varningssteg av mutationer i XPC‑genen, så UV‑skador samlas på istället för att repareras. Patienter med XP‑C utvecklar hudcancer tusentals gånger oftare än befolkningen i stort och måste undvika solljus mycket noggrant. Även om denna defekt i DNA‑reparation är välkänd har det varit mycket mindre klart hur den omprogrammerar cellernas interna kommunikationssystem—särskilt de system som styr inflammation.
Undersöka cellsignaler över tid
För att angripa problemet konstruerade forskarna mänskliga keratinocyter—de huvudsakliga cellerna i det yttersta hudlagret—som helt saknade XPC, och jämförde dem med annars identiska normala celler. De exponerade båda celltyperna för en noggrant vald, verklighetsnära nivå av UVB liknande en måttlig solbränna. Därefter undersökte de cellerna i två steg. En timme efter bestrålning mätte de aktiviteten hos många enzymer kallade protein‑tyrosinkinaser, som slår på och av signaler genom att lägga till små fosfattaggar. Tjugofyra timmar senare använde de avancerad masspektrometri för att ta en bred ögonblicksbild av tusentals proteiner och se vilka som ökade eller minskade i mängd. Denna tvåstegsmetod gjorde det möjligt att följa både de tidiga ”larmklockorna” och de senare ”nedströms‑svaren” i cellerna.
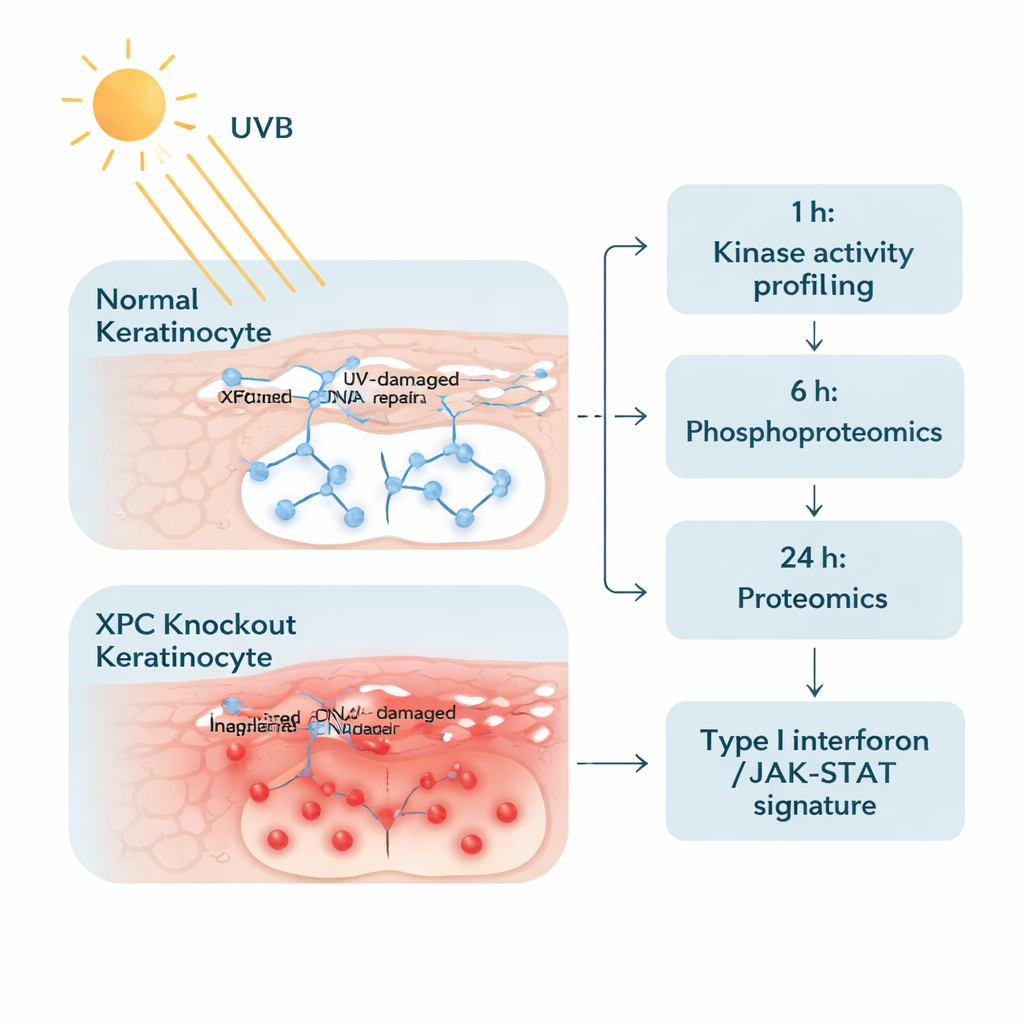
En inflammatorisk väg tänds
Den tidiga kinasanalysen visade att XPC‑defekta keratinocyter svarar på UVB med en våg av fosforylering på mer än hundra platser jämfört med normala celler. Föga förvånande samlades många av dessa förändringar i JAK/STAT‑signalvägen—en central kommunikationsrutt som vanligtvis används av immunsignaler som interferoner. Markörer kopplade till JAK1, JAK2, JAK3, TYK2 och STAT‑proteiner var mer aktiva i XP‑C‑celler, även före UVB, och stärktes ytterligare efter bestrålning. Det föreslog att cellerna var i ett förberett ”högalarmtillstånd”, redo att förstärka inflammatoriska budskap när de mötte UV‑inducerad stress.
Interferonliknande larmsvar i hudceller
Den senare, bredare proteinscreeningen bekräftade och utvidgade denna bild. I XPC‑knockoutceller, särskilt efter UVB, påverkades hundratals proteiner, och en stor kluster motsvarade gener som normalt aktiveras av typ I‑interferoner—samma antivirala signaler som kroppen använder för att bekämpa infektioner. Proteiner som MX1, MX2, IFIT1, IFIT2, IFIT3, ISG15, OAS1 och IRF9, klassiska ”interferon‑stimulerade gener”, var starkt uppreglerade. Nätverks‑ och väganalys kopplade dessa proteiner tillbaka till JAK/STAT och typ I‑interferon‑signalering som det dominerande temat. Uppföljande western blot‑experiment bekräftade att nyckel‑STAT‑proteiner var mer fosforylerade, och att dessa interferon‑responsiva proteiner producerades i mycket högre nivåer i XP‑C‑celler än i normala keratinocyter, både i vila och särskilt efter UVB.
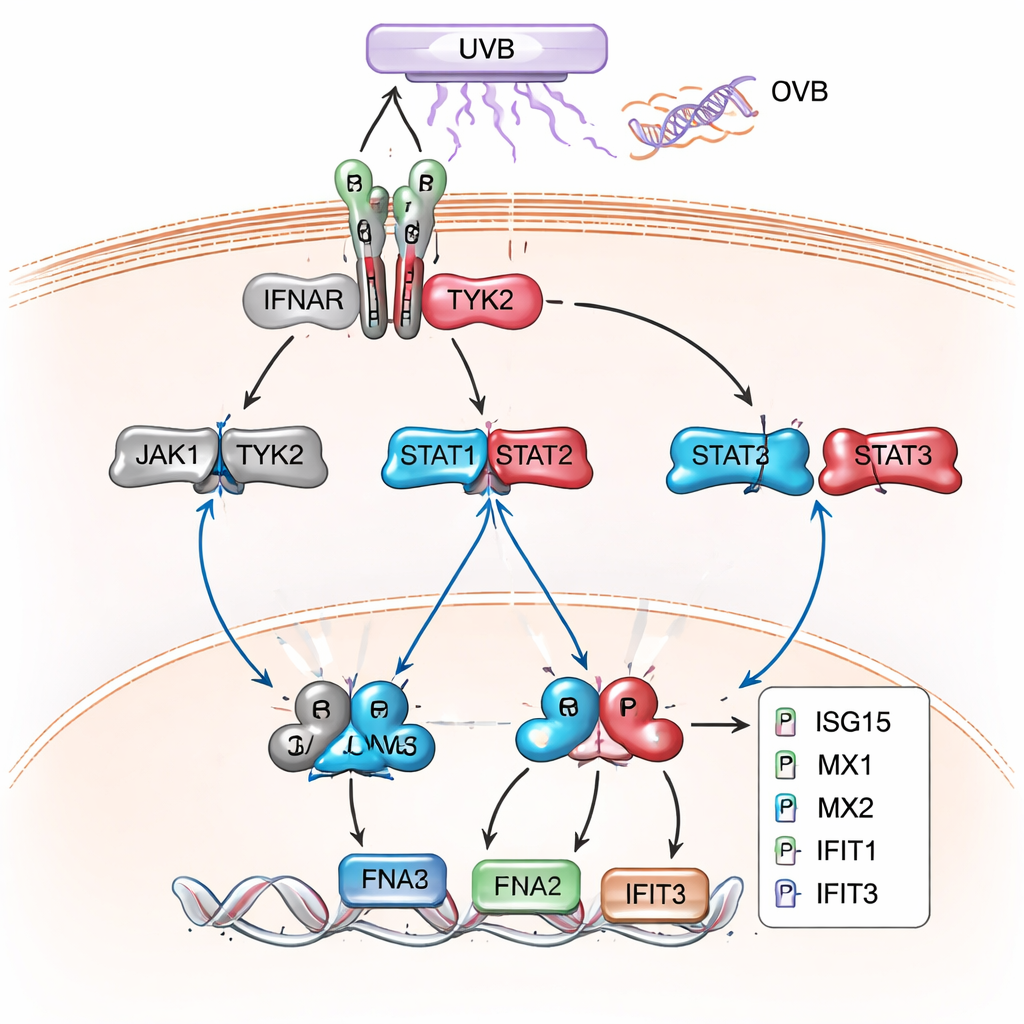
Vad detta betyder för patienter och framtida behandlingar
Tillsammans visar dessa resultat att XP‑C inte bara är en sjukdom av bristfällig DNA‑reparation; den kännetecknas också av ett bestående, interferon‑liknande inflammatoriskt tillstånd inne i hudceller, drivet genom JAK/STAT‑vägen och förvärrat av UV‑ljus. För en lekmannaläsare betyder det att XP‑C‑keratinocyter beter sig som om de ständigt kämpar mot en osynlig infektion när de utsätts för solljus, vilket lägger kronisk inflammation ovanpå oåtgärdade DNA‑skador. Även om studien inte testar behandlingar direkt öppnar den möjligheten att noggrant avvägda läkemedel som riktar in sig på JAK/STAT eller närliggande inflammatoriska kretsar en dag kan bidra till att minska UV‑utlösta skador vid XP‑C och kanske även vid andra inflammatoriska hudtillstånd som delar denna molekylära signatur.
Citering: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
Nyckelord: xeroderma pigmentosum, hudcancer, DNA-reparation, interferon-signalering, JAK STAT-vägen