Clear Sky Science · sv
Wnt-3a förvärrar produktionen av TNF-α i LPS-stimulerade mikroglia oberoende av den kanoniska β‑catenin‑vägen
Varför hjärninflammation spelar roll
Många hjärnsjukdomar, inklusive Parkinsons sjukdom, innefattar numera känd kronisk inflammation. I den processen kan hjärnans egna immunceller, kallade mikroglia, gå från att vara skyddande medhjälpare till att bli överaktiva angripare som skadar närliggande neuroner. Denna studie ställer en aktuell fråga: kan en signalmolekyl kallad Wnt‑3a, som länge antagits ha lugnande, skyddande effekter, faktiskt förvärra inflammationen under vissa förhållanden? Svaret visar sig vara mer komplicerat än väntat och belyser varför samma molekyl kan vara hjälpsam i ett sammanhang och skadlig i ett annat.
En budbärare med två ansikten
Wnt‑proteiner utgör en familj av kemiska budbärare som hjälper till att styra hjärnans utveckling, bevara hjärnceller i vuxen ålder och påverka hur celler svarar på skador. En av de mest studerade medlemmarna, Wnt‑3a, förknippas vanligtvis med en ”kanonisk” signalväg som stabiliserar ett protein kallat β‑catenin inne i cellerna. I många system tycks aktivering av denna väg dämpa inflammation och stödja neuronernas överlevnad, varför vissa forskare har undrat om förstärkning av Wnt‑3a skulle kunna skydda sårbara dopaminproducerande neuroner i Parkinsons sjukdom. Wnt‑proteiner kan dock också signalera via alternativa, ”icke‑kanoniska” vägar som istället kan driva inflammation, och vilken väg som dominerar kan bero på celltyp och dess tillstånd.
När lugna celler förblir lugna
För att utforska dessa möjligheter studerade forskarna primära mikroglia odlade från musexperiment. De undersökte först mikroglia i ett vilande, homeostatiskt tillstånd och exponerade dem endast för Wnt‑3a. Under dessa lugna förhållanden ökade inte Wnt‑3a frisättningen av centrala inflammatoriska molekyler som TNF‑α eller IL‑1β. Trots att viss intracellulär signalering aktiverades, skiftade inte mikroglian till ett kraftigt inflammatoriskt läge. Det antyder att i en frisk, icke‑inflammerad hjärna kan tillskott av Wnt‑3a i sig ha liten direkt inverkan på mikroglians inflammatoriska utsläpp.
När inflammerade celler pressas vidare
Bilden förändrades dramatiskt när mikroglian först aktiverades till ett inflammatoriskt tillstånd med bakteriellt lipopolysackarid (LPS), ett standardverktyg i laboratoriet för att efterlikna infektion. Som förväntat drev LPS ensamt en kraftig ökning av TNF‑α‑produktionen. Men när Wnt‑3a tillsattes tillsammans med LPS släppte mikroglian ut signifikant mer TNF‑α än vid LPS ensamt, medan IL‑1β inte ökade ytterligare. Detaljerade mätningar visade att denna ökade TNF‑α‑produktion inte berodde på större aktivering av den vanliga NFκB‑inflammationsvägen eller på extra aktivering av den kanoniska β‑catenin‑vägen. Blockering av β‑catenin‑vägen med ett protein kallat DKK1 lämnade Wnt‑3a‑drivna TNF‑α‑ökningen intakt, vilket visar att den förväntade ”anti‑inflammatoriska” vägen inte var ansvarig.
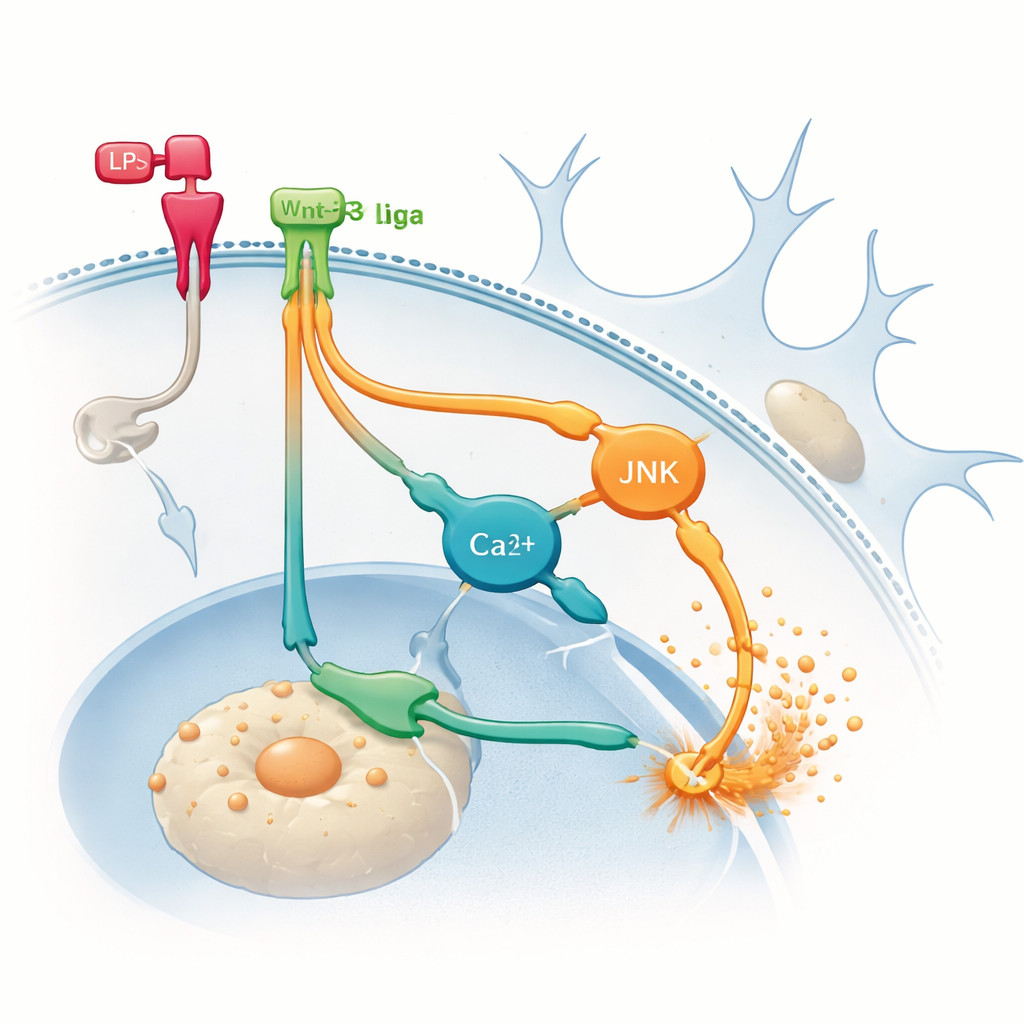
Dolda vägar som blåser upp elden
För att hitta var den extra inflammationen kom från vände teamet sig till de alternativa icke‑kanoniska vägar som Wnt‑proteiner kan använda. De blockerade farmakologiskt två signalgrenar inne i mikroglian: en som involverade ett protein kallat JNK och en annan som var kopplad till förändringar i cellens kalciumnivåer. Att hämma någon av dessa grenar minskade LPS‑inducerad TNF‑α‑produktion och, viktigt, förhindrade att Wnt‑3a ytterligare ökade TNF‑α. Dessa resultat tyder på att när mikroglia redan är inflammerade kan Wnt‑3a börja utnyttja icke‑kanoniska vägar i första hand, som förstärker inflammatoriska signaler snarare än att dämpa dem. Med andra ord kan samma budbärare ta en annan intern väg beroende på cellens utgångstillstånd, med mycket olika utfall.
Testning i en Parkinsonsmodell
Forskarna frågade sedan om detta beteende hos Wnt‑3a i mikroglia skulle översättas till större effekter på neuroner i en levande hjärna. De infunderade Wnt‑3a direkt i hjärnventriklarna hos möss som fick toxinet MPTP, en mycket använd modell för Parkinson‑liknande skador på dopaminneuroner och mikroglial aktivering. Som förväntat minskade MPTP antalet dopaminneuroner och ökade mikroglialtalet i ett mellanhjärneområde som är centralt för rörelse. Extra Wnt‑3a förvärrade dock inte neuronförlusten ytterligare eller ändrade mikroglialtalen signifikant jämfört med fordon‑behandlade djur. I denna komplexa in vivo‑situation räddade inte Wnt‑3a uppenbarligen och förvärrade inte heller tydligt toxinets skadliga effekter under den studerade tidsramen.
Vad detta betyder för framtida terapier
Sammantaget visar studien att Wnt‑3a inte är en enkel av/på‑brytare för hjärninflammation. I lugna mikroglia har den liten effekt, men i redan inflammerade celler kan den selektivt öka frisättningen av TNF‑α via icke‑kanoniska signalvägar, oberoende av den klassiska β‑catenin‑vägen. Samtidigt gav tillskott av Wnt‑3a i en Parkinson‑lik modell hos möss inte ett tydligt skydd eller en kortsiktig förvärring av dopaminneuronernas uppgång. För dem som intresserar sig för framtida behandlingar är huvudbudskapet att målinriktning av Wnt‑signalering kräver en noggrann förståelse för cellulärt sammanhang. Terapier baserade på Wnt‑3a eller besläktade molekyler kan hjälpa i vissa situationer men riskerar att slå fel i andra om de oavsiktligt förstärker skadlig inflammation.
Citering: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
Nyckelord: hjärnans inflammation, mikroglia, Wnt-signalering, Parkinsons sjukdom, TNF-alfa