Clear Sky Science · sv
APOL1-plasmamembranpooler motstår snabb proteinnedbrytning
Varför en njurproteins ”försvinnande” spelar roll
En stor del av svåra njursjukdomar hos personer med nylig afrikansk härkomst har kopplats till två varianter av en enda gen, APOL1. Trots det kämpar forskare fortfarande med att förklara exakt hur denna gen skadar njurceller utan att träffa de flesta bärare. Denna studie ställer en förrädiskt enkel fråga med stora följder: när APOL1-proteinet väl har bildats i cellerna, hur länge stannar det kvar, och var är det mest stabilt? Svaren avslöjar en överraskande dubbelnatur—APOL1 bryts snabbt ner inne i cellerna men förblir förvånansvärt stabilt när det är inbäddat i cellens yttre membran, en ledtråd som kan vägleda framtida terapier.
Riskgen med dubbel egg
APOL1-genen hjälper till att skydda människor mot vissa parasiter, en evolutionär fördel som sannolikt förklarar varför dess riskvarianter, kallade G1 och G2, är vanliga i afrikanska populationer. Tyvärr löper personer som ärver två kopior av dessa varianter en kraftigt ökad risk för njursjukdomar som grupperas som APOL1-medierade njursjukdomar. Tidigare arbete visade att när APOL1-nivåerna stiger—ofta som svar på inflammation—kan proteinet bli giftigt, särskilt i de känsliga njurfiltrecellerna som kallas podocyter. Men de flesta studier har fokuserat på vad som slår på APOL1. Mycket mindre var känt om hur cellerna stänger av det igen, till exempel genom att bryta ner proteinet.
Spåra ett skört protein inne i cellerna
För att undersöka APOL1:s stabilitet konstruerade forskarna humana cellinjer som producerade fluorescerande märkta varianter av APOL1 och dess närmaste släkting, APOL2. Detta gjorde det möjligt att följa hur mycket av varje protein som ackumulerades eller försvann under olika förhållanden med hjälp av western blot, mikroskopi och flödescytometri. De hämmade cellens huvudmaskineri för proteinnedbrytning, proteasomen, och blockerade separat nysyntes av protein. När proteasomerna hämmades steg APOL1-nivåerna snabbt, vilket visar att det normalt bryts ner i snabb takt. När ny proteinsyntes stoppades föll APOL1-nivåerna snabbt. I skarp kontrast förändrades APOL2 knappt under någon av behandlingarna, vilket visar att det är ett mycket mer stabilt protein. Viktigt är att APOL1:s höga omsättning var densamma för den normala varianten (G0) och riskvarianterna (G1 och G2), och att detta gällde flera naturligt förekommande APOL1-former som skiljer sig åt i hur de ligger i membran.
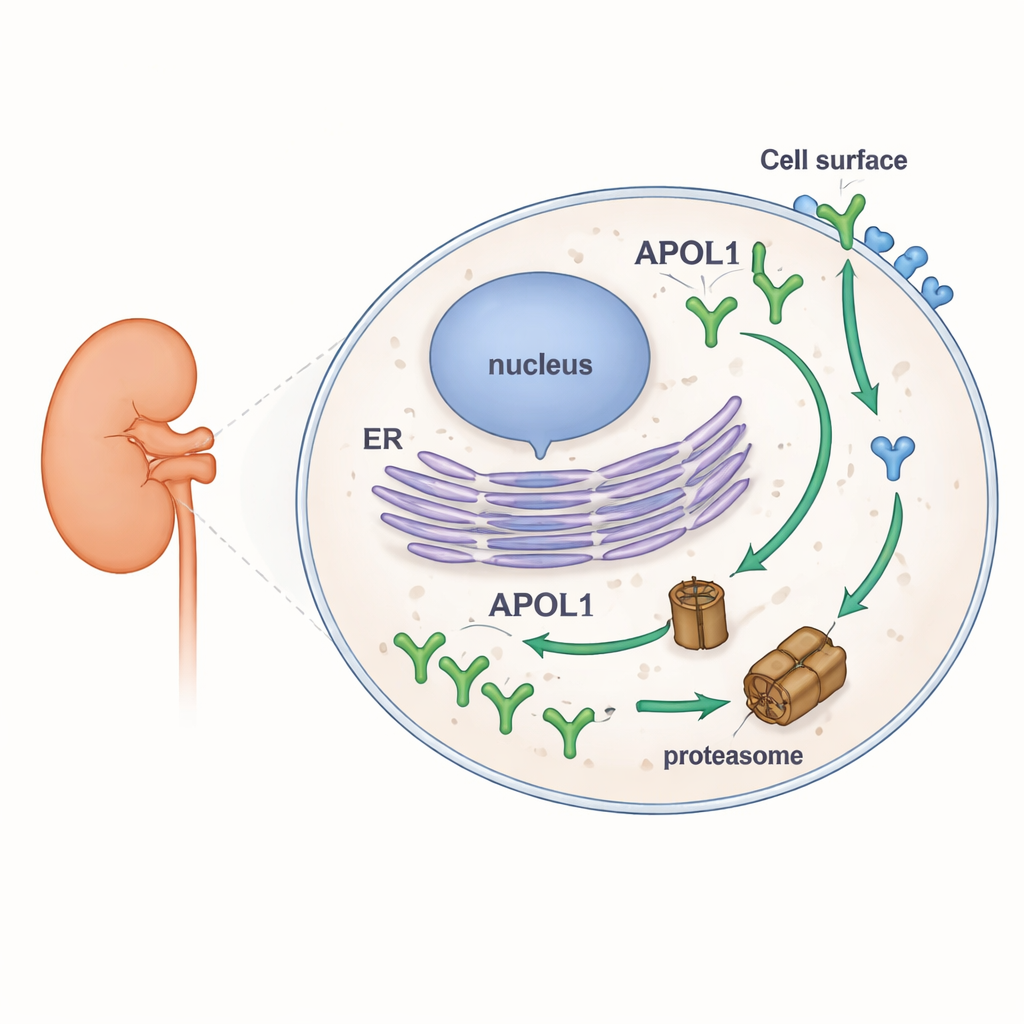
Sekvensledtrådar och en berättelse om två kvarter
Genom att gräva i proteinets struktur använde teamet datorverktyg för att söka efter lösa, ostrukturerade segment i APOL1 och APOL2, så kallade intrinsically disordered regions. Sådana regioner fungerar ofta som ”ät mig”-signaler för proteasomen. De identifierade två starka kandidatregioner i APOL1 som till stora delar saknades i APOL2. För att testa om APOL1:s unika frampart bidrar till dess skörhet skapade de hybrider: ett förkortat APOL1 som saknade sina första 59 aminosyror, och en APOL2-kimera som bar det APOL1-segmentet. Att lägga till APOL1:s N-terminala bit till APOL2 fick APOL2 att brytas ner snabbare, medan det trunkerade APOL1 förblev instabilt, vilket tyder på att mer än en del av APOL1 uppmuntrar snabb nedbrytning. Tillsammans kopplar dessa resultat APOL1:s ovanliga flexibla segment till dess snabba omsättning, utan att binda detta beteende specifikt till de sjukdomsframkallande varianterna.
Motståndskraftigt protein vid cellytan
Det mest anmärkningsvärda fyndet framträdde när författarna skiljde mellan APOL1 inne i cellen och APOL1 på cellytan. Genom att använda antikroppar som endast känner igen den del av APOL1 som exponeras utåt mätte de ytnivåerna separat från totalnivåerna. Inne i cellen uppförde sig APOL1 som väntat: det ackumulerades när proteasomer blockerades och försvann snabbt när nysyntesen stoppades. Ytbundet APOL1 rörde sig dock knappt vid någon av behandlingarna. När APOL1-molekyler väl nått plasmamembranet visade de sig vara starkt motståndskraftiga mot snabb nedbrytning. Dessutom, även om riskvarianterna producerade mindre total APOL1 än den normala varianten, var deras ytnivåer liknande. Detta tyder på att risk- och normal APOL1 rensas bort i jämförbara hastigheter inne i cellen, men att de membranbundna poolerna—som man tror bildar jonkanaler och driver toxicitet—bevaras i alla varianter.
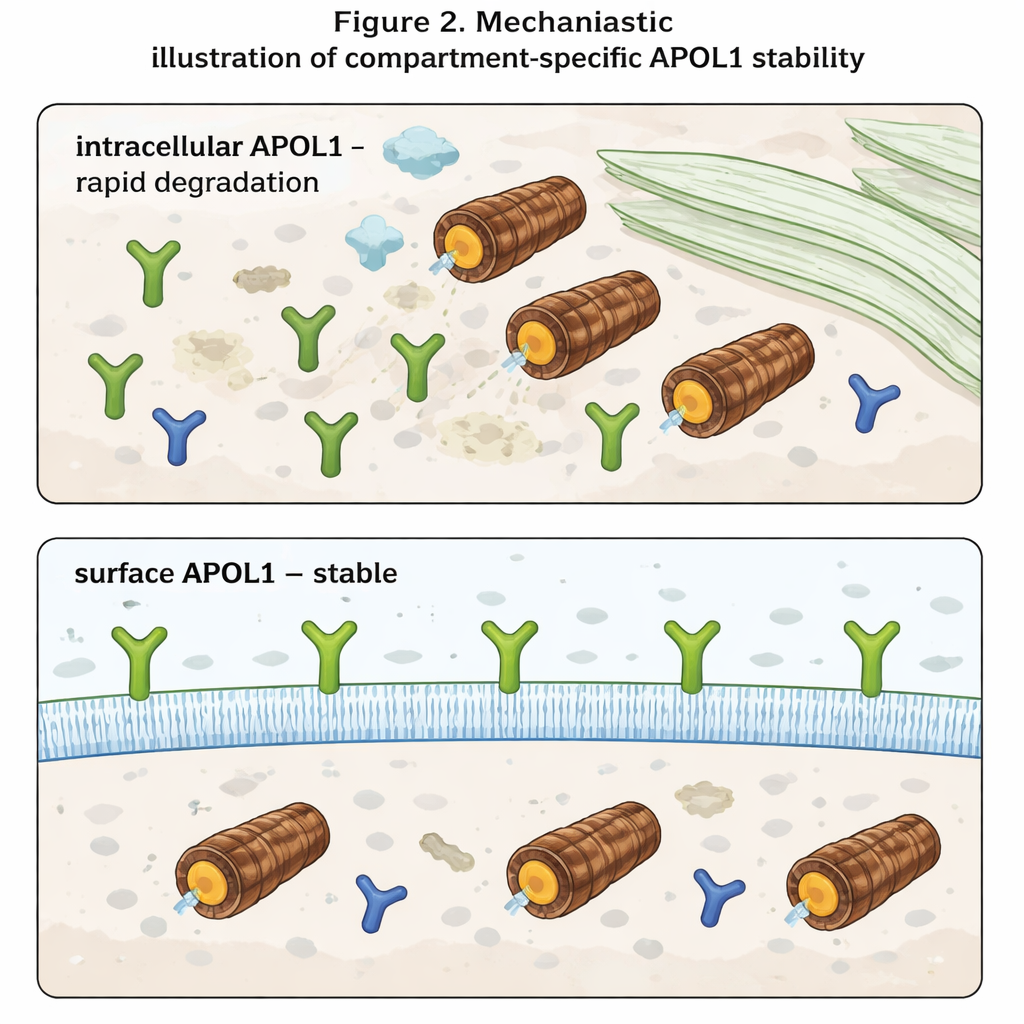
Vad detta betyder för framtida behandlingar
För icke-specialister är huvudbudskapet att APOL1 beter sig mycket olika beroende på var det befinner sig. Inne i cellen är det ett kortlivat protein, snabbt igenkänt och nedbrutet. Vid cellytan blir det långlivat och relativt skyddat, även när cellens nedbrytningsmaskineri förändras. Eftersom sjukdom verkar uppstå när APOL1-kanaler vid ytan rubbar balansen av joner som natrium och kalium, kan terapier behöva fokusera mindre på total APOL1-mängd och mer på hur mycket som når och kvarstår i plasmamembranet. Strategier som minskar transporten av APOL1 till ytan eller selektivt destabliserar ytpoolen skulle i princip kunna dämpa njurskada utan att helt blockera genens fördelaktiga immunfunktioner.
Citering: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
Nyckelord: APOL1, njursjukdom, proteinnedbrytning, plasmamembran, proteasom