Clear Sky Science · sv
In vitro-karakterisering av den katalytiska domen hos mänsklig histondeacetylas 5
Varför små omkopplare i vår DNA-förpackning spelar roll
Inuti varje cell är vårt DNA lindat runt proteiner som fungerar som spolar och hjälper till att få meter av genetiskt material att rymmas i ett mikroskopiskt utrymme. Om en gen är på eller av beror ofta på små kemiska märken på dessa spolproteiner. Denna studie fördjupar sig i en särskild protein"omkopplare" kallad HDAC5, som kopplats till hjärtsjukdom, hjärnstörningar, cancer och mer. Genom att förstå hur HDAC5 fungerar på molekylär nivå hoppas forskarna bana väg för mer precisa läkemedel med färre biverkningar.
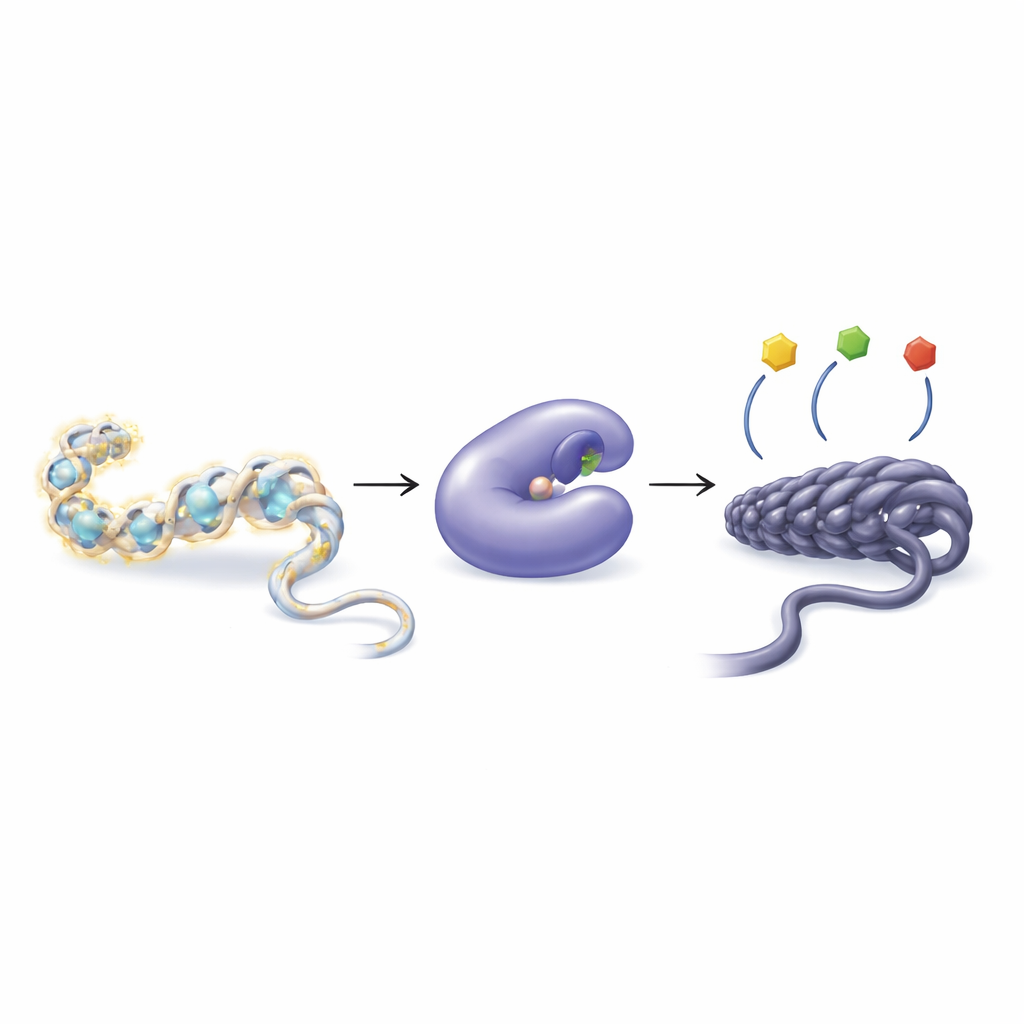
Hur celler finjusterar gener med små kemiska märken
Vårt DNA flyter inte fritt utan är lindat runt proteiner kallade histoner och bildar en struktur som kallas kromatin. Celler kan fästa eller ta bort små kemiska grupper, såsom acetylgrupper, från histonernas svansar för att göra kromatinet lösare eller tätare. Lösare paketering gör gener lättare att läsa; tätare paketering tenderar att tysta dem. Två grupper av enzymer hanterar denna balans: histonacetyltransferaser lägger till acetylgrupper, medan histondeacetylaser (HDACs) tar bort dem. När denna balans rubbas kan det bidra till en rad sjukdomar, inklusive cancer, hjärtproblem, muskelförtvining och immunrubbningar.
Varför HDAC5 är ett lovande men knepigt läkemedelsmål
HDACs bildar en stor familj av besläktade enzymer indelade i flera klasser. Många av de läkemedel som används kliniskt blockerar flera HDAC-typer samtidigt, vilket kan slå ut viktiga normala funktioner och orsaka kraftiga biverkningar. Klass IIa HDACs, inklusive HDAC5, sticker ut eftersom de är rikliga i specifika vävnader som hjärna, hjärta och skelettmuskulatur och samarbetar med andra proteiner för att reglera viktiga gen-nätverk. HDAC5 fungerar ofta som en brygga som för en mycket aktiv partnerenzym (HDAC3) till vissa gener så att kromatin kan bli tätare och dessa gener tystas. På grund av dessa fokuserade roller ses HDAC5 som ett attraktivt mål för mer selektiva läkemedel, men det har saknats detaljerade biokemiska data och ingen högupplöst struktur av dess aktiva kärna, vilket gör rationell läkemedelsdesign svår.
Återskapa HDAC5 i ett provrör
För att ta itu med denna kunskapslucka producerade forskarna endast den katalytiska kärnan av mänsklig HDAC5 – den del som utför den kemiska reaktionen – i bakterier, renade den och bekräftade att den bildar ett stabilt, enhetsligt protein i lösning. De testade sedan hur väl den fungerar under olika saltnivåer och surhetsgrader. HDAC5:s aktivitet förblev robust över ett brett spann av saltkoncentrationer och nådde en topp vid svagt basiska förhållanden, liknande dem i många celler. Med hjälp av särskilda fluorescerande testmolekyler fann de att den naturliga formen av HDAC5 känner igen endast en särskild typ av substrat som ofta används för att undersöka klass IIa-enzymer. Med ledning av tidigare arbete på närbesläktade HDACs bytte de ut en enda aminosyra (histidin) mot tyrosin på en kritisk plats. Anmärkningsvärt nog gjorde denna lilla förändring att den mutanta versionen av HDAC5 kunde bearbeta båda typerna av testsubstrat effektivt, vilket visar hur en enda rest i det aktiva sätet styr enzymets kemiska preferenser.
Testa och jämföra två nya läkemedelskandidater
Teamet undersökte sedan två experimentella HDAC5-blockerande molekyler, kända som NT160 och FFK24. Dessa föreningar använder en nyare zinkbindande grupp som undviker vissa av de toxiska effekter och dåliga selektivitetsproblem som ses med äldre, hydroxamatbaserade läkemedel. Genom att mäta hur varje inhibitor bromsade HDAC5 i noggrant kontrollerade reaktioner bestämde författarna extremt låga inhibitionskonstanter i nanomolärområdet, vilket innebär att båda föreningarna binder hårt till enzymet. NT160 band konsekvent ungefär tio gånger starkare än FFK24. För att förstå varför använde forskarna datorbaserad dockning med en AlphaFold-predicerad struktur av HDAC5:s kärna. Båda inhibitorerna delade ett gemensamt huvudområde som låg djupt i det aktiva facket och kontaktade metalljonen, men NT160:s svans skapade extra stabiliserande kontakter med specifika aminosyror i facket. Dessa ytterligare interaktioner förklarar sannolikt dess större potens.
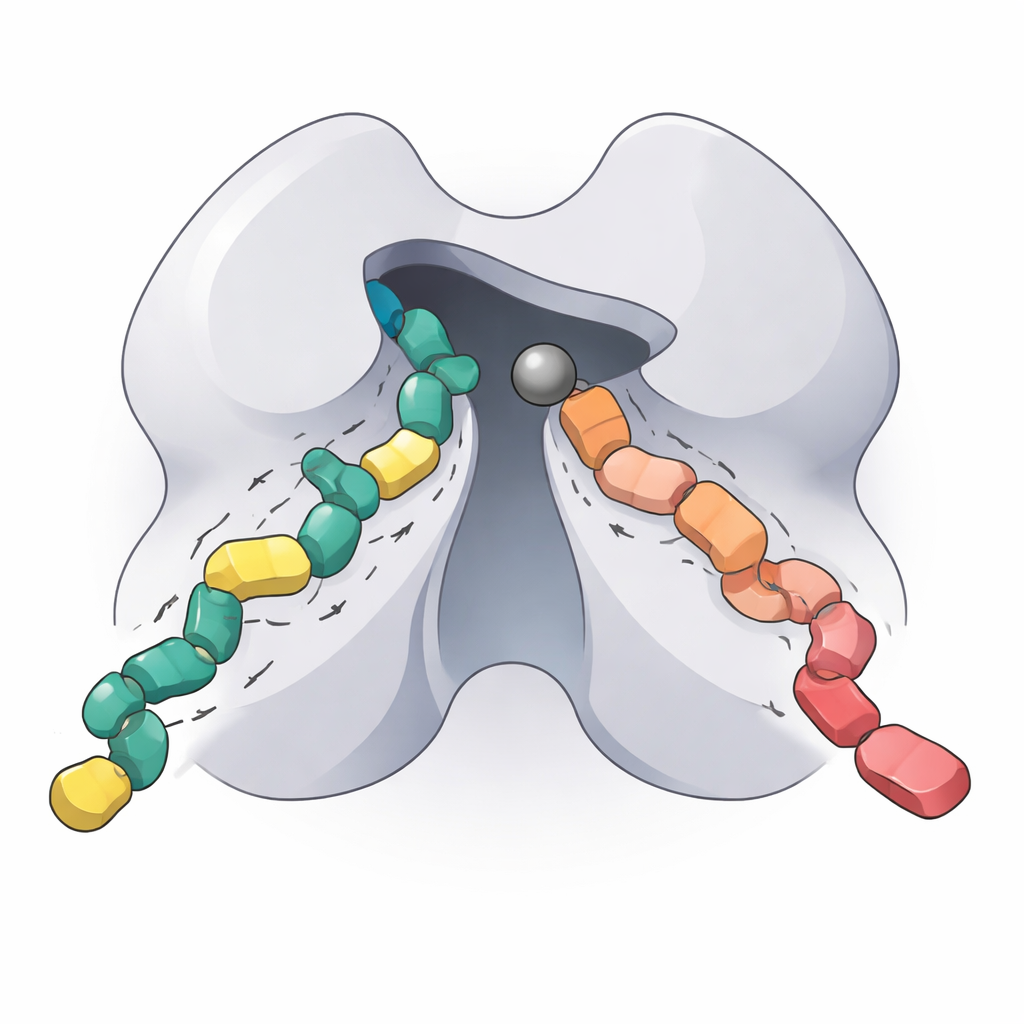
Vad detta betyder för framtida målinriktade terapier
Genom att återuppbygga den fungerande kärnan av HDAC5, kartlägga dess optimala arbetsförhållanden, dissekera hur en enda aminosyraförändring ändrar dess beteende och kvantifiera hur två nästa generationens inhibitorer binder, levererar denna studie ett detaljerat biokemiskt "fingeravtryck" av ett viktigt men tidigare dåligt karaktäriserat enzym. För icke-specialister är huvudbudskapet att HDAC5 hjälper till att avgöra om vissa gener är på eller av, och att en noggrann inställning av denna omkopplare kan vara värdefull vid behandling av hjärtsjukdom, neurodegeneration, cancer och immunrubbningar. De nya insikterna och verktygen som presenteras här bör hjälpa forskare att designa HDAC5- och klass IIa-selektiva läkemedel som verkar där de behövs samtidigt som oönskade effekter på andra håll i kroppen minimeras.
Citering: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
Nyckelord: histondeacetylas 5, epigenetisk reglering, HDAC-hämmare, målinriktad cancerterapi, kromatinstruktur