Clear Sky Science · sv
Beräkningsbaserad identifiering av multitarget-naturliga föreningar från Sesbania grandiflora som potentiella terapeutiska medel mot Klebsiella pneumoniae
Varför ett gammalt botemedel är relevant för nya superbakterier
Infektioner som är resistenta mot antibiotika blir allt svårare att behandla, och en av de värsta förövarna är en sjukhusbakterie kallad Klebsiella pneumoniae. När denna bakterie överlistar våra bästa läkemedel kan läkarna stå utan alternativ. Den här studien ställer en hoppfull fråga: skulle naturliga kemikalier från ett traditionellt medicinskt träd, Sesbania grandiflora (även kallat vegetable hummingbird), kunna omarbetas till moderna läkemedel som samtidigt angriper bakterien på flera svaga punkter?
En svår bakterie som överlistar läkemedel
Klebsiella pneumoniae orsakar allvarliga sjukdomar såsom lunginflammation, urinvägsinfektioner, sepsis och hjärnhinneinflammation, särskilt hos personer med nedsatt immunförsvar. Under det senaste decenniet har många stammar blivit resistenta även mot karbapenemer, antibiotika som vanligtvis sparas som en "sista utväg." Bakterien försvarar sig genom att bryta ner läkemedel, pumpa ut dem, täta sitt yttre membran och bilda skyddande biofilmer. Eftersom den använder många olika knep samtidigt är ett läkemedel som har ett enda mål lätt att undfly. Författarna hävdar att en bättre strategi är att blockera flera viktiga processer tillsammans, vilket gör det mycket svårare för mikroben att utveckla resistens.
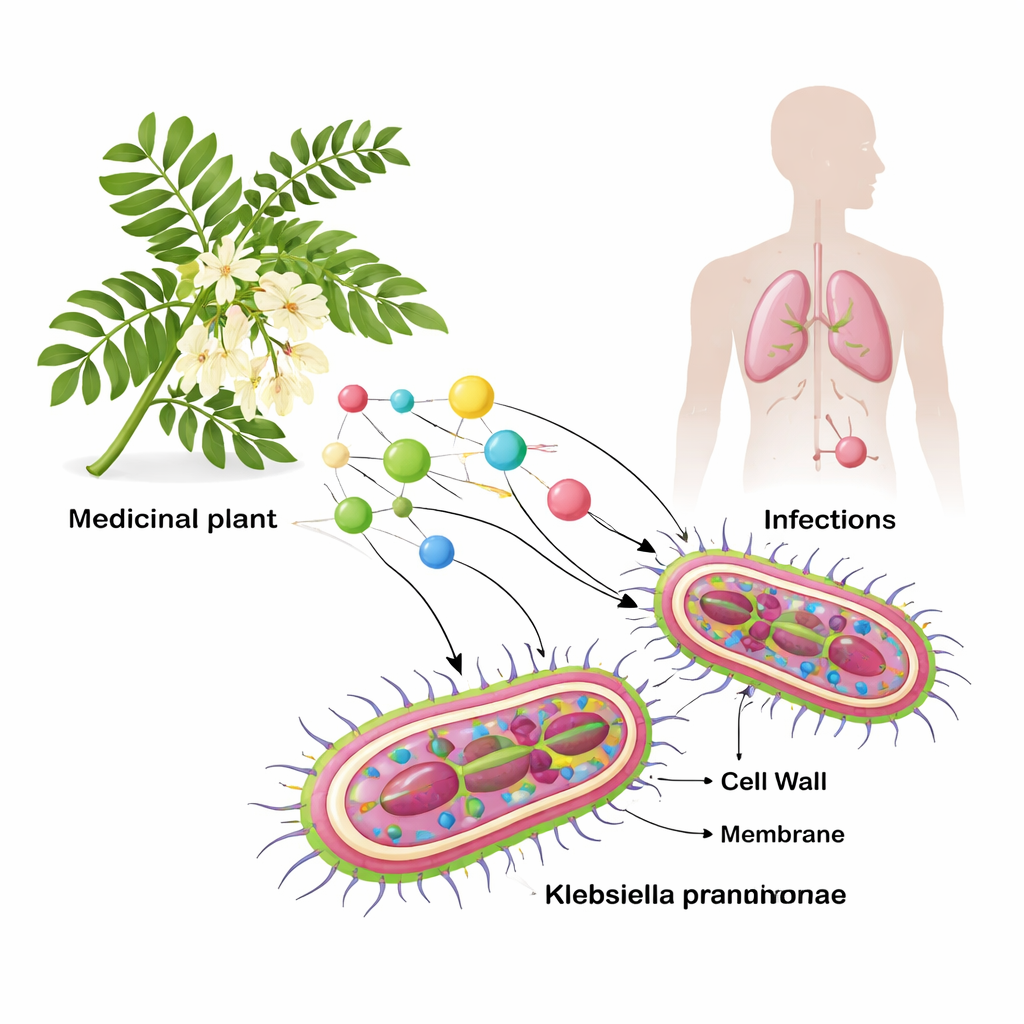
Söker ledtrådar i ett medicinskt träd
Sesbania grandiflora har en lång historia inom traditionell medicin och har visat aktivitet mot olika sjukdomsalstrande mikrober. Istället för att testa växtextrakt direkt i laboratorium använde forskarna datorer för att genomföra en omfattande virtuell screening. De genomsökte först hela uppsättningen av Klebsiella-proteiner och, med strikta kvalitets- och litteraturfilter, begränsade listan till sex särskilt viktiga bakteriella komponenter. Dessa inkluderar enzymer som behövs för att bygga det yttre skalet och cellväggen, ett resistensenzym som förstör kraftfulla antibiotika och ett strukturellt protein som hjälper bakterien att interagera med mänskliga celler. Parallellt samlade de 73 kända växtkemikalier från S. grandiflora och förberedde tredimensionella modeller av både föreningarna och de bakteriella målen.
Hitta växtföreningar som träffar många mål
Teamet använde molekylär dockning, en teknik som förutsäger hur väl varje växtmolekyl kan passa in i fickorna hos varje bakteriellt protein. De flesta av de testade föreningarna kunde fästa vid alla sex målen med gynnsamt förutspänd styrka, och en mindre grupp visade särskilt stark bindning. En nätverksanalys avslöjade att tre mål i synnerhet—FabG, KPC‑2 och OmpA—var kopplade till nästan alla föreningar, vilket antyder bred täckning. Forskarna tillämpade sedan standardregler för "drug-likeness" och datoriserade modeller för absorption och toxicitet för att sålla bort molekyler som sannolikt inte fungerar säkert i kroppen. Denna gallringsprocess reducerade listan till nio lovande kandidater, många med gemensamma strukturella drag—såsom ringformade kärnor och flera syre-rika grupper—som hjälper dem att bilda stabila kontakter med proteiner.
Närbild på en stjärnkandidat
Av dessa nio stack en förening, Sonchuionoside A, ut eftersom den dokade starkt till alla sex bakteriella mål samtidigt som den uppfyllde säkerhets- och användbarhetsfiltret. För att testa hur robusta dessa interaktioner kan vara körde författarna långa molekyldynamiksimuleringar, i praktiken genom att observera hur varje protein och föreningen rör sig tillsammans över hundratals nanosekunder i en virtuell vattenbox. Över alla sex målen förblev Sonchuionoside A bundet utan att störa proteinernas stabilitet och gjorde ofta proteinerna något mer kompakta och ordnade. Detaljerade analyser av rörelse, ytexponering, vätebindningar och uppskattade bindningsenergier föreslog särskilt starka och gynnsamma interaktioner med två enzymer som deltar i byggandet av essentiella cellekomponenter (LpxH och FabG), tillsammans med stabil bindning till resistensenzymet KPC‑2 och yttre-membranproteinet OmpA.
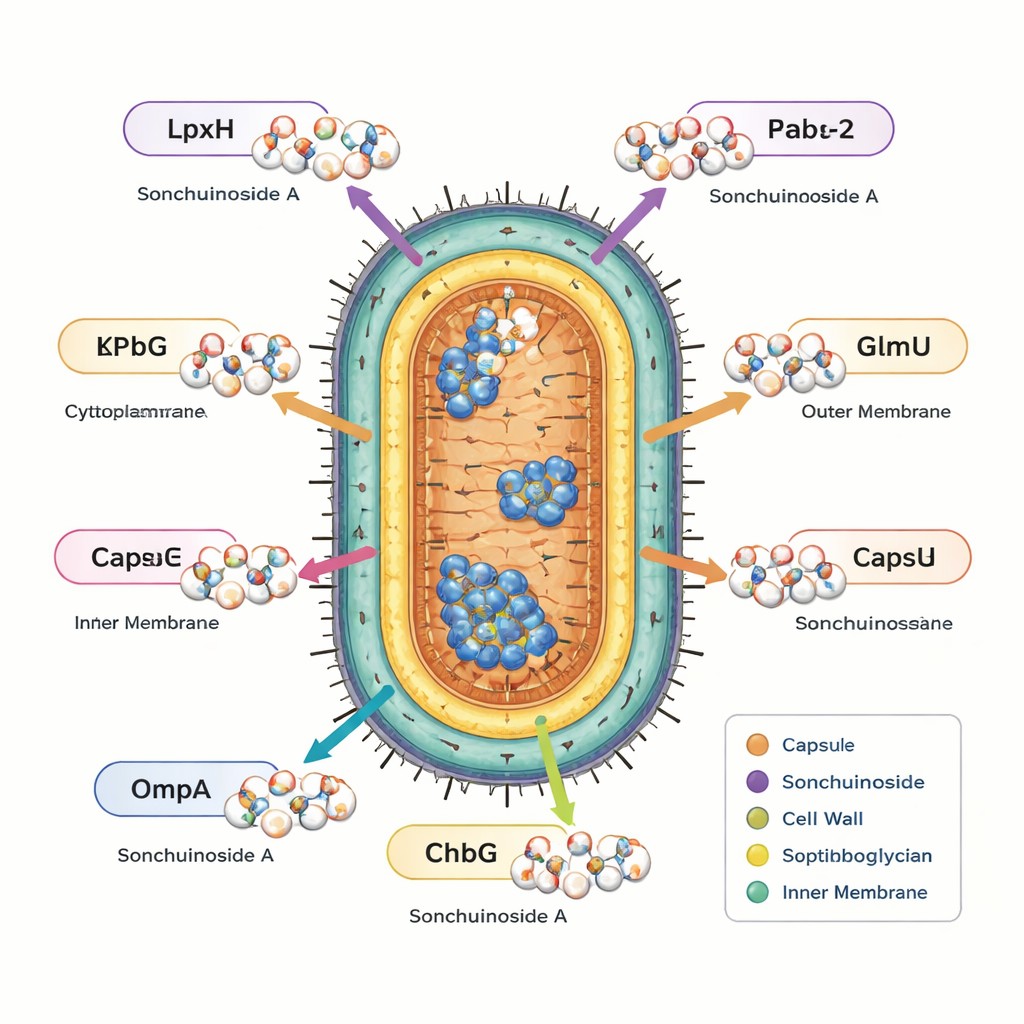
Vad detta kan innebära för framtida behandlingar
Denne forskning levererar ännu inget färdigt läkemedel, och alla resultat kommer från datormodeller snarare än från djur- eller humana studier. Trots det ger den en övertygande vägkarta. Arbetet visar att en enskild växtförening som Sonchuionoside A skulle kunna utformas för att angripa Klebsiella pneumoniae på flera fronter—svekta dess cellförsvar, underminera dess resistensmaskineri och försvaga dess förmåga att orsaka sjukdom. Enkelt uttryckt antyder studien att ett traditionellt medicinskt träd kan inspirera framtida flerfaldiga antibiotika, och hjälpa läkare att ligga ett steg före farliga, läkemedelsresistenta infektioner.
Citering: Sajal, H., Mohan, A., Ravi, V. et al. Computational identification of multi-target natural compounds from Sesbania grandiflora as potential therapeutic agents against Klebsiella pneumoniae. Sci Rep 16, 7782 (2026). https://doi.org/10.1038/s41598-026-37613-9
Nyckelord: antibiotikaresistens, Klebsiella pneumoniae, läkande växter, naturliga föreningar, multimålsläkemedel