Clear Sky Science · sv
SMAD2-ubikvitinering via PY-motiv reglerar skelettmuskelmassa och fibrotisk degeneration
Varför denna muskelstudie är viktig
När vi blir äldre märker många att våra muskler blir svagare och mindre, och vid kronisk sjukdom eller skada kan muskelvävnad gradvis ersättas av stel ärrvävnad. Denna studie tar sig an en grundläggande fråga bakom dessa förändringar: hur ser muskelceller till att en kraftfull tillväxtreglerande signal, kallad TGF‑beta, inte går för långt och orsakar muskelförtvining och fibros (ärrbildning)? Genom att avtäcka en liten inbyggd ”avstängningsknapp” i ett nyckelprotein i TGF‑beta‑vägen visar författarna en ny mekanism som hjälper till att bevara muskelmassa och en frisk vävnadsstruktur.
En inbyggd broms på en kraftfull signal
TGF‑beta är ett signalsubstans som berättar för celler när de ska bromsa tillväxt, ändra identitet eller producera bindväv. I skelettmuskulatur krymper för mycket TGF‑beta muskelfibrer och främjar fibros; för lite kan störa normal tillväxtkontroll. Inuti cellerna fungerar TGF‑beta huvudsakligen via ett reläprotein kallat SMAD2. Efter att TGF‑beta bundit sina receptorer vid cellmembranet aktiveras SMAD2 och rör sig in i kärnan för att ändra genaktivitet. För att förhindra att detta blir permanent markerar cellerna SMAD2 kemiskt med små ubikvitinmolekyler, vilket flaggar det för nedbrytning. En kort sekvens i SMAD2, känd som PY‑motivet, är dokningsplatsen för enzymer som fäster dessa ubikvitintaggar. Forskarna frågade: om denna dokningsplats tas bort i ett levande djur, fallerar då SMAD2‑bromsen, och vad händer med musklerna över tid?
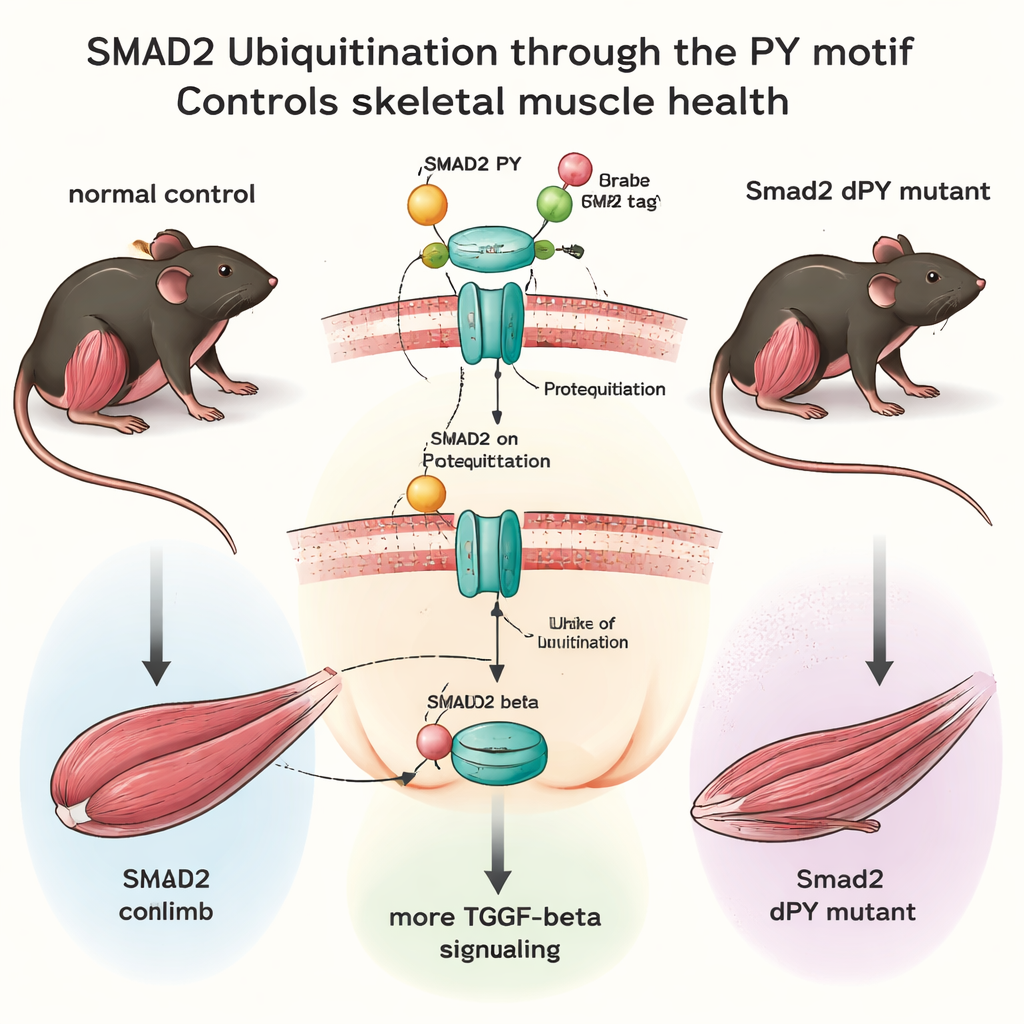
Skapa möss utan säkerhetsmärkning
Med moderna genredigeringsverktyg skapade teamet möss där endast 15 DNA‑bokstäver tagits bort från Smad2‑genen, vilket exakt avlägsnade PY‑motivet utan att störa resten av proteinet. Dessa Smad2dPY‑möss föddes normalt, utvecklades till vuxna och var fertila, vilket visar att detta finjusteringssystem inte är nödvändigt för grundläggande utveckling under standard laboratorieförhållanden. När forskarna dock undersökte deras muskler närmare framträdde en annan bild. Unga vuxna möss visade endast subtila förändringar, men vid 12 månader—ungefär medelålder för en mus—vägde stora bakbensmuskler mindre och enskilda fibrer var mindre jämfört med normala syskon. Inuti dessa muskler var SMAD2‑proteinnivåerna högre, medan dess ubikvitinering var minskad, vilket bekräftade att det saknade PY‑motivet gjorde SMAD2 mer stabilt och mindre nedbrytbart.
Överkänsliga muskelceller och fördröjd reparation
För att förstå vad detta innebar på cellnivå isolerade forskarna muskelprekursorceller (myoblaster) från de mutantiska mössen. När dessa myoblaster exponerades för TGF‑beta i en odlingsskål visade de starkare aktivering av SMAD2 och större induktion av TGF‑beta‑responsiva gener än celler från normala möss. Samtidigt var deras förmåga att förena sig till långa, flerkärniga muskelfibrer—ett viktigt steg i muskelväxt och regeneration—påverkad. Liknande förändringar sågs i fibroblaster, bindvävscellerna som finns mellan muskelfibrerna: mutanta fibroblaster svarade starkare på TGF‑beta och uttryckte lättare gener kopplade till ärrbildande myofibroblaster. Tillsammans tyder dessa fynd på att utan PY‑motivet blir både muskelbildande celler och stödjeceller överkänsliga för TGF‑beta, vilket tippar balansen mot mindre fibrer och mer fibrotisk vävnad.
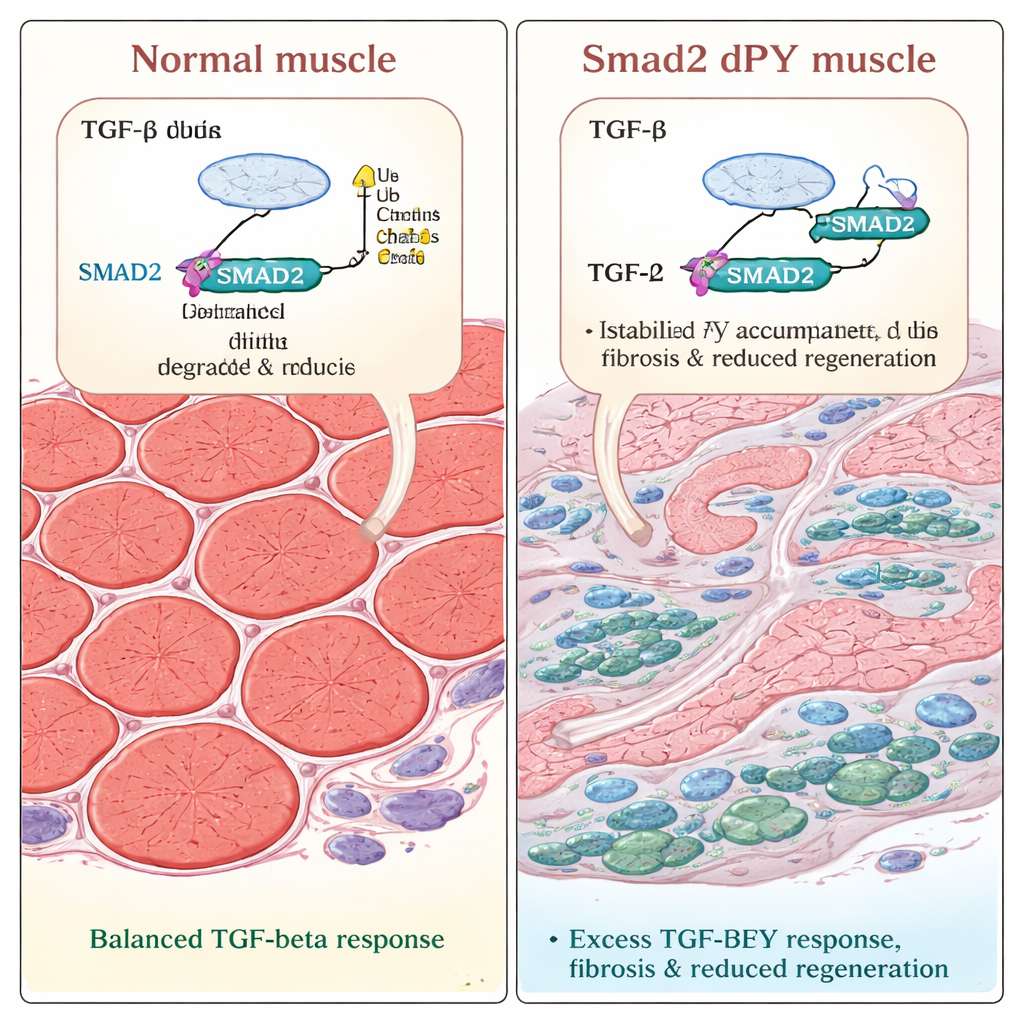
När skadan inträffar vinner ärrbildningen
Teamet testade sedan hur dessa förändrade muskler hanterar skada. De injicerade ett toxin i benmuskler för att utlösa skada och reparation, en väletablerad modell för regeneration. I både normala och mutanta möss bröts skadade fibrer initialt ner och började sedan växa ut igen. Men tre veckor efter skadan var de regenererade fibrerna i Smad2dPY‑möss märkbart tunnare. Mikroskopi avslöjade större områden fyllda med kollagen, huvudkomponenten i ärrvävnad, och fler alfa‑sletta muskelaktin‑positiva myofibroblaster, celler kända för att driva fibros. Dessa resultat visar att när SMAD2 inte kan märkas och omsättas korrekt, förskjuts reparationsprocessen: istället för att fullt återbygga stark muskel läker vävnaden med ökad ärrbildning och minskad kontraktil massa.
Vad detta betyder för muskelhälsa
För icke‑specialister är huvudbudskapet att en mycket liten molekylär egenskap—PY‑motivet på SMAD2—fungerar som en tyst men viktig skyddsmekanism i skelettmuskulatur. Den låter celler tona ner TGF‑beta‑signalering genom att främja SMAD2‑borttagning, vilket hjälper till att bibehålla normal muskelstorlek och begränsa fibros, särskilt när TGF‑beta‑nivåerna naturligt ökar med ålder eller kronisk skada. När denna skyddsmekanism inaktiveras i möss blir musklerna gradvis mindre och mer ärrbenägna, och de återhämtar sig inte fullt ut efter skada. Även om arbetet ännu är gjort i djur, framhäver det SMAD2‑ubikvitinering som en potentiell måltavla för framtida strategier för att bevara muskelmassa och förebygga fibrotisk degeneration vid åldrande eller sjukdom.
Citering: Yamasaki, Y., Sakamoto, K., Yashiro, S. et al. SMAD2 ubiquitination through PY motif regulates skeletal muscle mass and fibrotic degeneration. Sci Rep 16, 6666 (2026). https://doi.org/10.1038/s41598-026-37582-z
Nyckelord: skelettmuskel, TGF-beta-signalering, SMAD2, ubikvitinering, fibros