Clear Sky Science · sv
Förändringar i EGFR-aktivitet efter CRISPR/Cas9-redigering av EGF-bindningsdomänen
Varför omkoppling av en cancersignal spelar roll
Cervixcancer är ofta beroende av en kraftfull tillväxtomkopplare kallad epidermal tillväxtfaktorreceptor (EGFR). Många tumörer har enorma mängder av dessa receptorer, men läkemedel som syftar till att stänga av dem har bara hjälpt en del av patienterna. Denna studie ställde en grundläggande fråga med stora behandlingsimplikationer: vad händer om du tar bort EGFR:s förmåga att fånga sitt favorit-tillväxtsignal, epidermal tillväxtfaktor (EGF), utan att ta bort receptorn i sig?
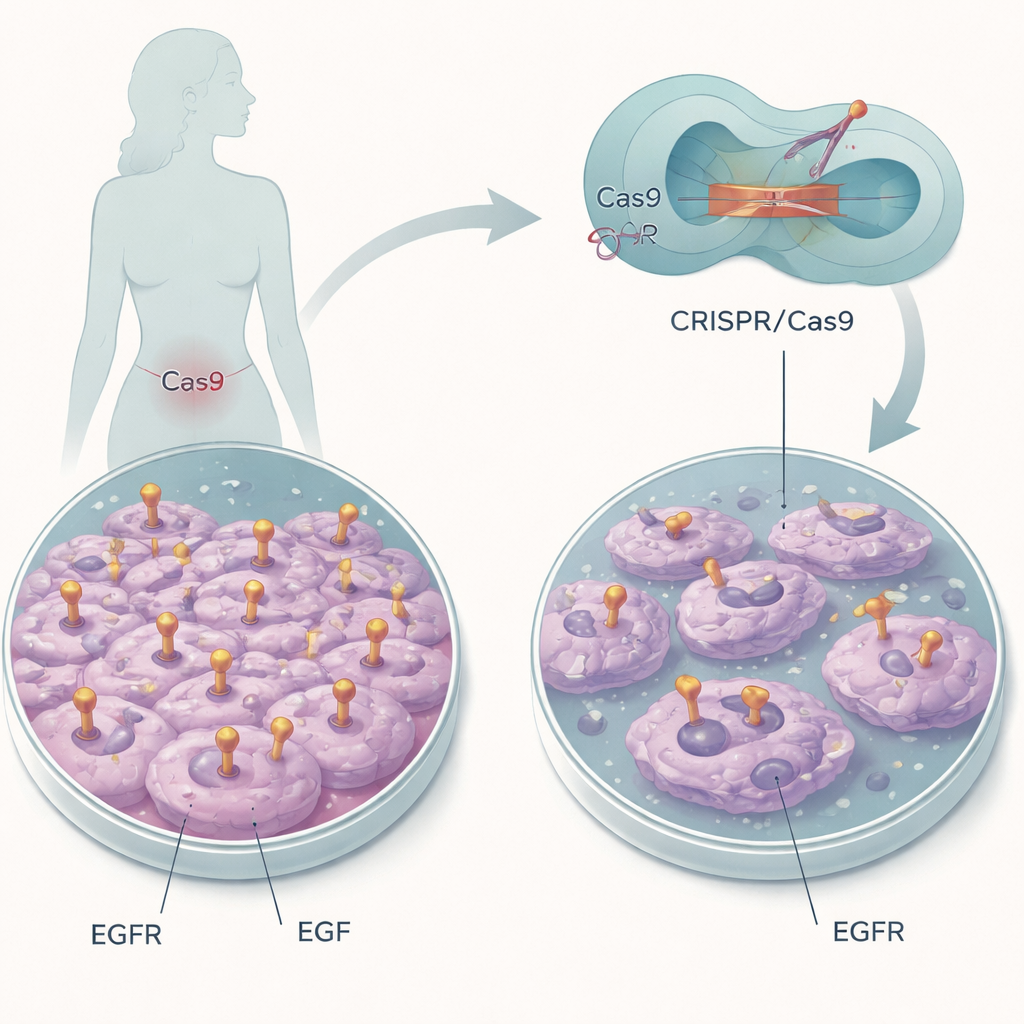
Att stänga av en molekylär “på-knapp”
Forskarna fokuserade på en cervixcancercellinje som uttrycker stora mängder i övrigt normalt EGFR. Istället för att förstöra genen använde de CRISPR/Cas9-genredigering som en molekylär skalpell för att förändra bara några aminosyror i EGFR:s EGF-bindningsficka. Två särskilda positioner, kallade L14 och Y45, hjälper EGF att docka till receptorn. Genom att ersätta dessa byggstenar med andra ville teamet behålla EGFR närvarande men göra det blint för EGF, så att de kunde isolera rollen för denna enda interaktion i cancercellernas beteende.
Att bygga skräddarsydda cancercellinjer
I ett första steg testade teamet dessa mutationer i celler med plasmider som tillfälligt producerade antingen normalt eller förändrat EGFR. Fluorescensmärkta EGF visade att alla mutantformer band mycket mindre ligand än den normala receptorn, särskilt när både L14 och Y45 ändrades tillsammans. Forskarna introducerade sedan dessa förändringar direkt i cancercellernas genom med CRISPR/Cas9 och skapade flera nya cellkloner. Vissa bar en enkel mutation, andra hade dubbelmutation på en EGFR-kopia och inaktiverande förändringar på den andra. Datorbaserade modeller av de resulterande proteinformerna visade att dessa förändringar förvrängde bindningsstället tillräckligt för att försvaga eller avskaffa EGF-dockning, i överensstämmelse med bindningstesterna.
När receptorn flyttas men cellerna överlever
Detaljerad avbildning visade att de redigerade receptorerna uppförde sig mycket annorlunda inne i cellen. I oredigerade cancerceller sitter EGFR på cellmembranet, fångar EGF och rör sig sedan inåt samtidigt som det kemiskt aktiveras via fosforylering. I kloner som bar dubbelmutationen försvann i praktiken EGF-bindningen och EGFR sågs inte längre på membranet; istället ansamlades den lilla mängd receptor som fanns kvar inne i cellens inre. Även en enda förändring i Y45 minskade bindningen avsevärt och sänkte de totala EGFR-nivåerna. Ändå, trots denna störning av den klassiska EGF–EGFR-signalvägen, förblev cancercellerna livskraftiga och fortsatte växa i odling med endast måttliga förändringar i sina cellcykelmönster.
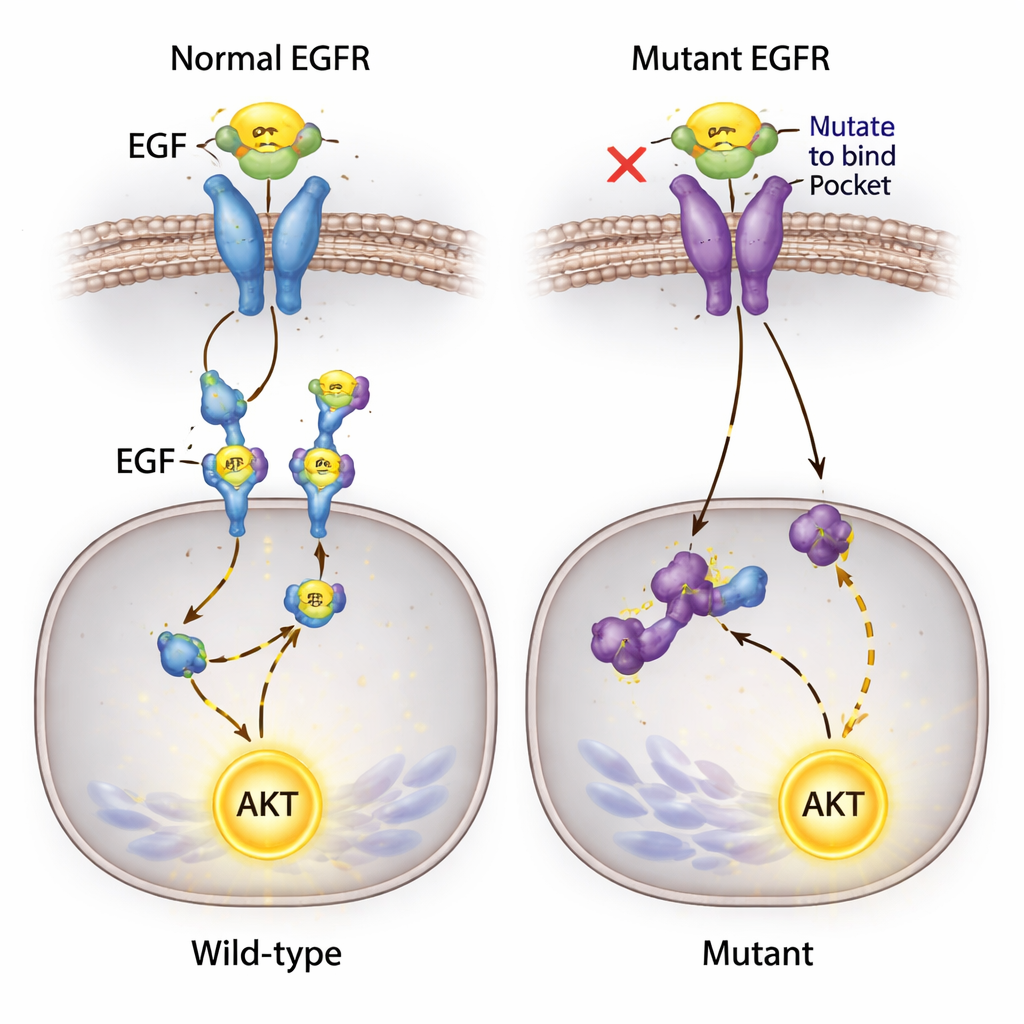
En oväntad signal som inte ger sig
En av de mest överraskande observationerna rörde AKT, ett nyckelprotein som främjar cellsurvival och som vanligtvis aktiveras nedströms om EGFR. Forskarna förväntade sig att blockering av EGF–EGFR-bindningen skulle tysta denna väg. Istället, när de tillsatte EGF i mediet, aktiverades AKT kraftigt i alla cellinjer—inklusive de där EGF inte längre kunde binda EGFR och där receptorfosforylering var omöjlig att upptäcka. Eftersom dessa celler bär på en känd mutation i en annan signaleringsgen, PIK3CA, misstänker teamet att alternativa rutter kan tillåta EGF att mata in i AKT-aktiveringen, möjligen via andra ytreceptorer eller bakgrundsmutationer, och därigenom kringgå det redigerade EGFR.
Dolda genetiska förändringar och framtida terapier
För att säkerställa att CRISPR inte orsakade omfattande oavsiktliga förändringar sekvenserade forskarna hela genomet i de nya cellinjerna. De bekräftade att de önskade EGFR-mutationerna var närvarande och fann inga tecken på klipp vid förutspådda off-target-ställen för CRISPR-guiderna. De upptäckte dock många spontana mutationer spridda över genomet, varav några kan påverka cellernas beteende. Detta understryker att även när CRISPR träffar sitt avsedda mål kan cancercellernas naturligt instabila DNA komplicera tolkningen av experimentella resultat och utformningen av precisa genbaserade terapier.
Vad detta betyder för patienter
För en lekman är huvudbudskapet att det helt enkelt inte räcker att avbryta handslaget mellan EGF och EGFR—även mycket precist på atomnivå—för att automatiskt stoppa cancerceller från att få ”väx och överlev”-kommandon. Studien visar att cancerceller kan dirigera om viktiga signaler som AKT-aktivering runt en blockad receptor, och att CRISPR-redigering i sig måste utvärderas noggrant i sådana instabila genom. Dessa konstruerade cellinjer utgör nu en kraftfull laboratoriemodell för att söka efter backup‑vägar som upprätthåller EGFR‑beroende tumörer, information som i sista hand kan leda till kombinationsbehandlingar som riktar både EGFR och dess dolda medhjälpare.
Citering: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Nyckelord: EGFR, cervixcancer, CRISPR, EGF-signalering, AKT-vägen