Clear Sky Science · sv
Ökad kopietal driver IFI30-överuttryck och koordinerad immunaktivering, vilket identifierar en ny diagnostisk och terapeutisk måltavla vid gastriskt adenom
Varför ett magprotein är viktigt
Magcancer är en av världens dödligaste cancerformer, främst därför att den ofta upptäcks sent och kan vara svår att behandla. Denna studie fokuserar på ett relativt okänt protein kallat IFI30, som finns i celler som hjälper immunsystemet att känna igen hot. Genom att spåra hur IFI30 förändras i magtumörer och hur det formar kroppens försvar föreslår forskarna att det kan bli ett kraftfullt verktyg för tidigare diagnos och för att välja mer effektiva, personligt anpassade behandlingar.
En dold signal i magtumörer
Teamet började med att ställa en grundläggande fråga: förekommer IFI30 i olika mängder i frisk respektive cancersjuk magsäcksvävnad? Genom att använda stora offentliga databaser som sammanfogar genaktivitetsdata från tusentals prover fann de att IFI30 konsekvent är mycket högre i gastriskt adenom—den vanligaste typen av magcancer—än i normalt magslemhinna. Detta gällde över flera oberoende patientgrupper och både på RNA- och proteinnivå. När författarna testade hur väl IFI30 ensam kunde skilja tumörvävnad från frisk vävnad var dess prestanda slående: en diagnostisk noggrannhet (AUC) på 0,92, vilket betraktas som utmärkt för en enstaka markör. Mikroskopibilder placerade också IFI30 i cellens interna återvinningssystem, där antigen bearbetas för immunigenkänning.
DNA-förändringar som skruvar upp IFI30
Nästa steg var att undersöka varför IFI30 är så förhöjt i dessa tumörer. Genom att skanna cancergenom från The Cancer Genome Atlas fann de att extra kopior av IFI30-genen—kända som kopietalsamplifieringar—var den främsta drivkraften bakom dess överuttryck. Tumörer med amplifierat IFI30 tenderade att uppvisa större övergripande genomisk instabilitet och bar ofta välkända cancerrmutationer såsom TP53 och PIK3CA. När IFI30:s kopietal ökade steg även dess RNA-nivåer, vilket antyder en direkt koppling mellan strukturella DNA-förändringar och den ökade produktionen av detta protein. Det målar upp IFI30 inte som en passiv åskådare, utan som en del av ett bredare mönster av aggressiv tumörbiologi.
Immunologiskt korsprat kring tumören
Eftersom IFI30 är involverat i bearbetning av material som immunceller presenterar som ”wanted posters” för T‑celler, utforskade teamet exakt var det befinner sig i tumörmikromiljön. Ensamscellssekvensering, som avläser genuttryck i enskilda celler, visade att IFI30 är särskilt rikt i dendritiska celler, makrofager och CD8‑T‑celler—nyckelspelare i att initiera och upprätthålla anti‑tumörimmunitet. Nätverksanalyser avslöjade tät kommunikation mellan IFI30‑rika immunceller och omgivande tumör‑ och stödjeceller. Tumörer med högt IFI30 visade stark aktivering av vägar kopplade till antigenpresentation, inflammatoriska signaler och kommunikationsmolekyler som attraherar och organiserar immunceller. Samtidigt uppvisade dessa tumörer drag av invasion och stress, såsom accelererad cellcykel, vävnadsombyggnad och anpassning till låg syrehalt, vilket framhäver IFI30:s roll i skärningspunkten mellan anfall och försvar inom cancern.
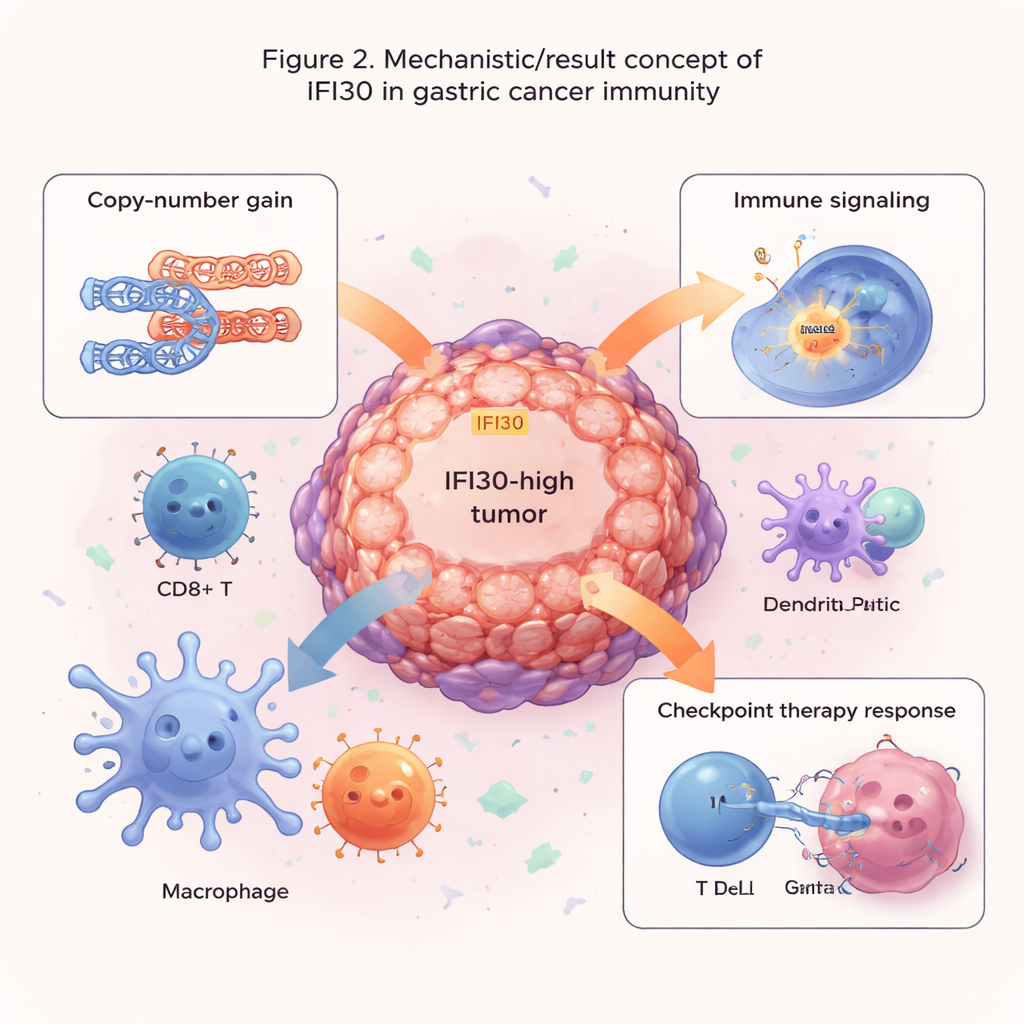
Ledtrådar för läkemedelsval och immunterapi
Författarna frågade därefter om IFI30 kunde hjälpa till att förutsäga hur tumörer svarar på behandling. Genom att para ihop IFI30‑nivåer med stora läkemedelsresponssdatabaser fann de att IFI30‑höga tumörer tenderar att vara resistenta mot vissa läkemedel som riktar sig mot celldelning eller en vanlig tillväxtsignalväg (MAPK), men verkar mer känsliga för läkemedel som blockerar EGFR och PI3K/AKT‑signalering. Noterbart var att IFI30‑nivåer följde PD‑L1 nära, en viktig broms på T‑celler som dagens checkpoint‑hämmare riktar sig mot. I flera immunterapistudier var patienter vars tumörer hade högre IFI30‑uttryck mer benägna att svara på checkpoint‑blockad än de med låga nivåer. En IFI30‑baserad poäng överträffade etablerade mått såsom tumörmutationsbörda och PD‑L1 ensam, och var särskilt förhöjd i tumörer med hög mikrosatellitinstabilitet, en undergrupp som redan är känd för att svara bättre på immunterapi.
Från bänk till möjlig ny måltavla
För att testa om IFI30 bara är en markör eller också bidrar till cancers tillväxt sänkte teamet dess nivåer i magcancercellinjer med genetiska verktyg. När IFI30 knockades ner växte cancercellerna långsammare, vilket pekar på en direkt roll i att upprätthålla tumörproliferation. Sammanfattningsvis tyder data på att IFI30 både är en avläsning av immunaktivitet och en bidragande faktor till malignt beteende. För patienter innebär detta att en enkel mätning av IFI30 en dag skulle kunna hjälpa läkare att upptäcka magcancer mer tillförlitligt, förutsäga vem som kan dra nytta av vissa målinriktade läkemedel eller immunterapier, och kanske vägleda nya behandlingar som direkt eller indirekt blockerar IFI30:s tumörfrämjande effekter.
Citering: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Nyckelord: magcancer, IFI30, biomarkör, tumörimmunitet, immunterapi