Clear Sky Science · sv
En delad biotinligasmetod avslöjar proteiner associerade med oligomert alfa‑synuklein under aggregering
Varför hopklumpade hjärnproteiner spelar roll
Vid Parkinsons sjukdom och närliggande tillstånd kan ett normalt hjälpsamt hjärnprotein som kallas alfa‑synuklein klumpa ihop sig till klibbiga avlagringar kända som Lewy‑kroppar. Dessa avlagringar dyker upp decennier före symtom och är ett kännetecken vid obduktion, men vi vet fortfarande inte vilka andra proteiner som bidrar till att föra alfa‑synuklein från ett ofarligt tillstånd till skadliga aggregat. Denna studie använder en smart molekylär "proximity‑tagg" för att kartlägga vilka proteiner som sitter nära alfa‑synuklein när det övergår från enskilda molekyler till små kluster, vilket ger nya ledtrådar till hur sjukdomen börjar och vilka vägar som kan riktas för att bromsa eller förebygga den.
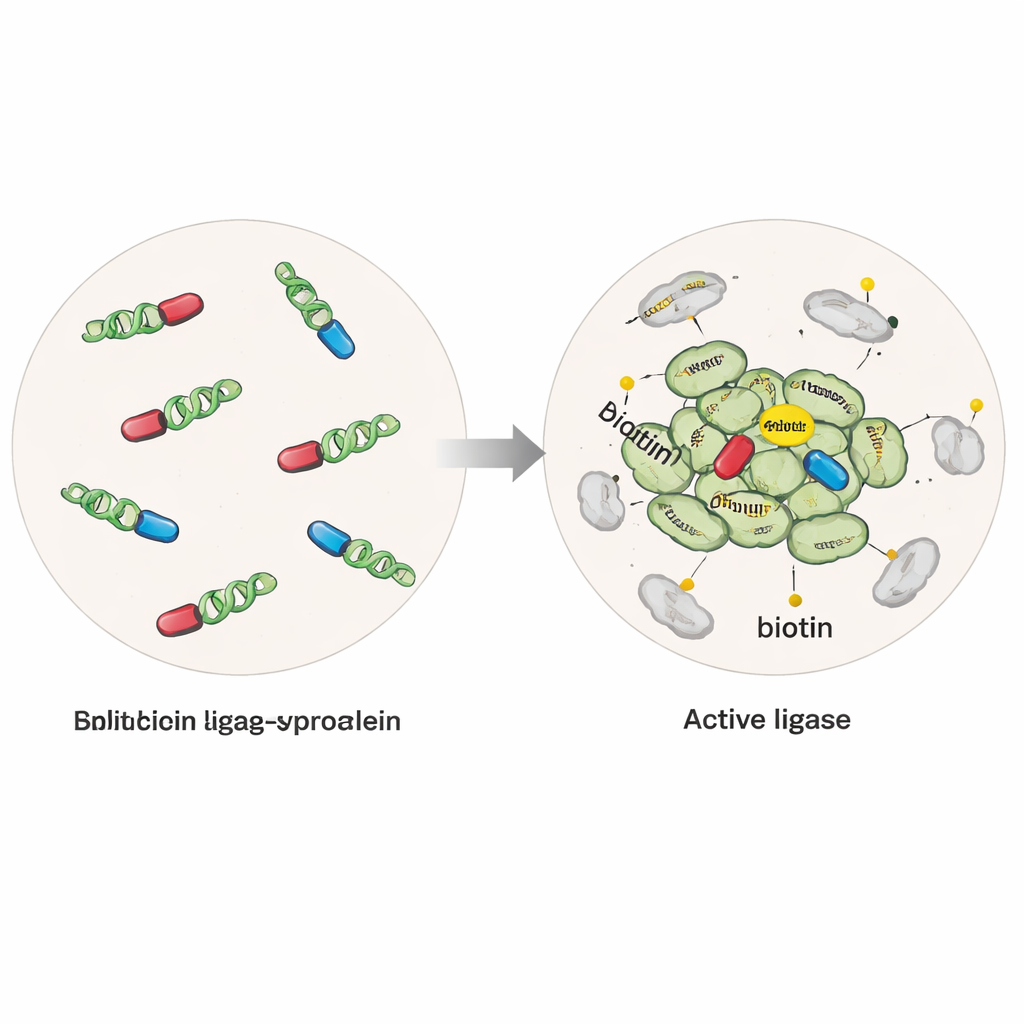
En molekylär “tagg” som lyser upp grannar
Forskarna konstruerade mänskliga celler för att tillverka alfa‑synuklein fuserat med ett modifierat enzym som kan fästa en liten biotintagg på vilket protein som helst inom några miljarder delar av en meter. I en version var enzymet intakt och aktivt närhelst alfa‑synuklein fanns, vilket fångade proteiner nära både enskilda molekyler och kluster. I en andra, mer selektiv "delad" version, klipptes enzymet i två inaktiva halvor, vardera kopplad till en separat alfa‑synukleinmolekyl. Endast när alfa‑synukleinmolekyler kom ihop sig till multimärer eller oligomerer återförenades halvorna till ett aktivt enzym, vilket slog på taggningen specifikt runt dessa tidiga aggregat. Genom att tillsätta renat alfa‑synuklein‑fibriller till cellerna kunde teamet också driva fram sjukdomslik aggregering och jämföra normala kontra patologiska tillstånd.
Att bygga en karta över närliggande proteiner
Efter att ha tillåtit tid för taggning drog teamet ner alla biotinmärka proteiner och identifierade dem med masspektrometri, en teknik som väger och räknar proteiner med hög precision. I samtliga betingelser fann de 1 277 distinkta proteiner, och efter noggrann filtrering begränsade de detta till 581 som sannolikt faktiskt låg nära alfa‑synuklein. Genom att jämföra det intakta och delade enzymesystemet kunde de skilja proteiner som främst associerar med enskilda molekyler från dem som föredrar multimärer. De jämförde också celler med och utan tillsatta fibriller för att se hur det lokala proteinmiljön kring alfa‑synuklein förändras när aggregering utlöses.
Viktiga cellulära vägar som dras in i klumparna
Det resulterande interaktomet pekar på flera stora biologiska teman. Under normala förhållanden låg multimeriskt alfa‑synuklein nära många membran‑trafikproteiner och proteinmodifierande enzymer—i linje med dess föreslagna roll i att hjälpa nervceller hantera synaptiska vesiklar och upprätthålla proteinkvalitetskontroll. Flera enzymer som adderar fosfatgrupper, inklusive kinaserna PAK4, RIPK2 och MAP4K4, var rikliga nära friska multimärer men verkade förlora kontakten när aggregat bildades, vilket antyder att störning av dessa relationer kan gynna sjukdomsassocierade former av proteinet. Teamet detekterade också proteiner kopplade till insulinliknande tillväxtfaktor‑signalering, vilket stöder kliniska kopplingar mellan insulinresistens och Parkinsons sjukdom, och fann att aggregering rekryterar proteiner involverade i borttagning av skadade proteiner, såsom 14‑3‑3‑chaperonfamiljen och specifika komponenter i cellulära nedbrytningsvägar.
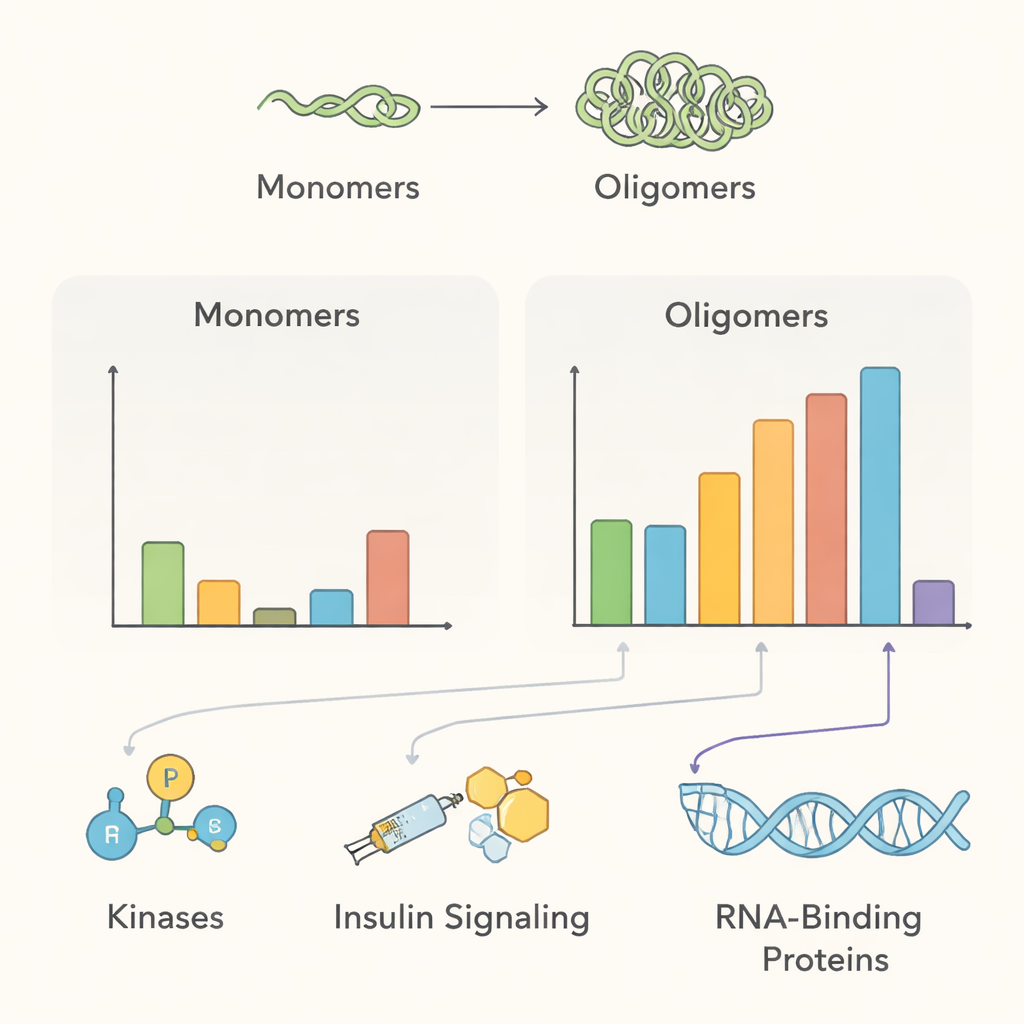
Oväntade broar till andra hjärnsjukdomar
Bortom Parkinsons sjukdom framhäver datan en överraskande koppling till amyotrofisk lateralskleros (ALS) och frontotemporal demens (FTD). Ett RNA‑bindande protein kallat FUS, som felaktigt lokaliseras och aggregerar i dessa tillstånd, syntes nära multimeriskt alfa‑synuklein både under normala och aggregeringsdrivna förhållanden. Andra RNA‑relaterade proteiner ändrade också sin närhet när alfa‑synuklein aggregerade. Dessa fynd väcker möjligheten att små alfa‑synukleinassemblage kan fånga RNA‑hanterande proteiner på fel plats i cellerna, vilket potentiellt länkar biologin i Lewy‑kroppsjukdomar med den i ALS och FTD, även om direkta fysiska interaktioner fortfarande behöver verifieras.
Vad detta betyder för förståelsen av sjukdom
För icke‑specialister är huvudpoängen att detta arbete tillhandahåller en tidig "kontaktlista" över proteiner som följer med alfa‑synuklein när det går från en normal hjälpare till en skadlig klump. Studien antyder att förlusten av vissa skyddande relationer—såsom med specifika kinaser eller kvalitetskontrollenzymer—kan vara lika viktig som att vinna nya toxiska partners. Medan experimenten utfördes i en förenklad cellmodell och ännu inte bevisar orsak och verkan, lyfter de fram konkreta kandidater och vägar för framtida tester i neuroner och hjärnvävnad. I längden kan kartläggning av dessa skiftande protein‑grannskap vägleda strategier för att återställa skyddande interaktioner, stödja insulinrelaterad signalering eller förhindra fångst av RNA‑bindande proteiner, vilket potentiellt bromsar steget från subtila molekylära förändringar till fullskaliga Lewy‑kroppsjukdomar.
Citering: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Nyckelord: alfa‑synuklein, Lewy‑kroppsjukdom, proteinformering, proximity‑proteomik, Parkinsons sjukdom