Clear Sky Science · sv
Insikter i strukturella skillnader mellan homo- och heterodimerer berikade från en cocktail av monoklonala antikroppar mot SARS-CoV-2
Varför blandning av antikroppar kan ge överraskningar
Under covid-19-pandemin användes antikroppsbaserade läkemedel som REGEN-COV-cocktailen för att blockera viruset som orsakar sjukdomen, SARS-CoV-2. Dessa läkemedel är noggrant utformade, men när de väl blandas i ett provrör kan de bilda sällsynta parbildningar kallade heterodimerer — två olika antikroppar förenade som ett par. Denna studie ställer en praktisk fråga med stora konsekvenser för säkerhet och effektivitet: när dessa ovanliga par bildas, beter de sig då annorlunda än de mer välbekanta paren av identiska antikroppar, och kan det förändra hur väl läkemedlet fungerar?
Ovanliga par i ett kraftfullt covid-19-läkemedel
REGEN-COV kombinerar två monoklonala antikroppar, casirivimab och imdevimab, vardera designad för att fästa vid SARS-CoV-2:s spikeprotein på olika sätt. När båda formuleras tillsammans, hakar en mycket liten andel av antikropparna i hop som par. En del par är homodimerer (två kopior av samma antikropp); andra är heterodimerer (en casirivimab plus en imdevimab). Heterodimerer betraktas som en förorening eftersom de inte ingår i den ursprungliga läkemedelsdesignen, och deras beteende i kroppen har till största delen varit okänt. Författarna använde först en flerstegsreningsprocess för att isolera flera distinkta homodimerarter och heterodimeren från samma REGEN-COV-parti, vilket gav dem en sällsynt möjlighet att jämföra alla dessa sammansättningar sida vid sida.
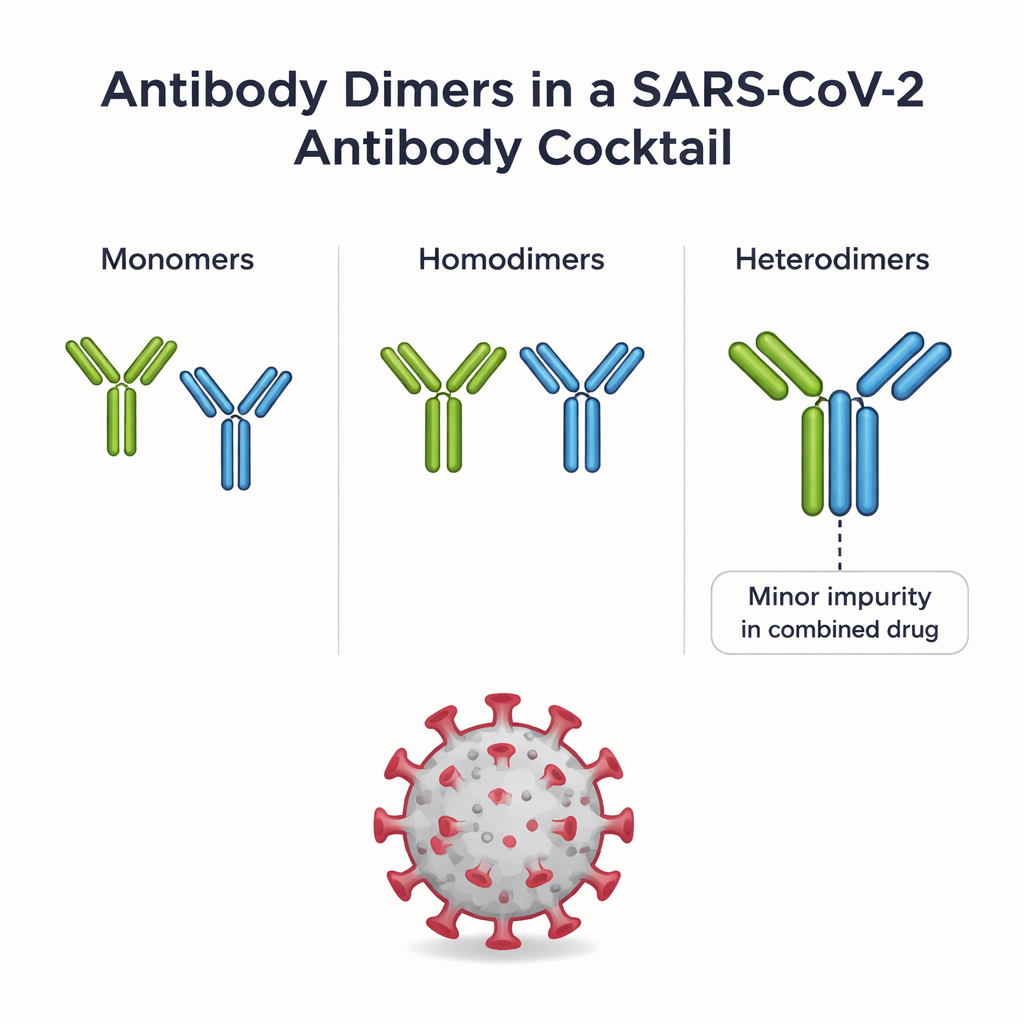
Undersöka form, klibbighet och kemiska bindningar
För att förstå vad som gör varje dimer-typ unik kombinerade teamet flera avancerade analytiska verktyg. Kromatografiexperiment visade hur dimererna skiljer sig i ytans "klibbighet" (hydrofobicitet), medan kapillärelektrofores och en specialiserad form av masspektrometri visade om de två antikropparna i en dimer hålls ihop av svaga attraktioner eller av starkare kovalenta bindningar. Elektronmikroskopi och analytisk ultracentrifugering gav sedan inblick i den övergripande formen — om en dimer är förlängd och flexibel eller kompakt och tätt packad. Tillsammans visade dessa metoder att casirivimab och imdevimab bildar flera distinkta homodimerer med olika former och bindningsmönster, och att heterodimeren är särskilt kompakt och rik på kovalenta länkar som involverar olika delar av antikropparnas armar och stammar.
Hur struktur kopplas till virusblockering och celldöd
Forskarna frågade sedan hur dessa strukturella skillnader påverkar det som verkligen räknas: att stoppa viruset och engagera immunsystemet. De testade varje dimer i ett pseudovirus-neutraliseringsprov, som mäter hur väl antikropparna blockerar inträde av en viruslik partikel, och i ett antikroppsberoende cellulärt cytotoxicitetsprov (ADCC), som mäter hur effektivt antikropparna rekryterar immunceller för att förstöra infekterade mål. Överraskande nog var de flesta dimerformer åtminstone lika bra som, och ibland bättre än, sina individuella monomer-motsvarigheter vid neutralisering av virus. Särskilt visade imdevimab-homodimerer "hyperpotent" neutralisering, troligen eftersom deras geometri tillåter dem att överbrygga flera spike-proteiner på virusets yta. Vissa casirivimab-homodimerer gav särskilt starka ADCC-signaler, uppenbarligen eftersom deras orientering lämnar svansregionerna (Fc-delarna) väl exponerade för immuncellsreceptorer.
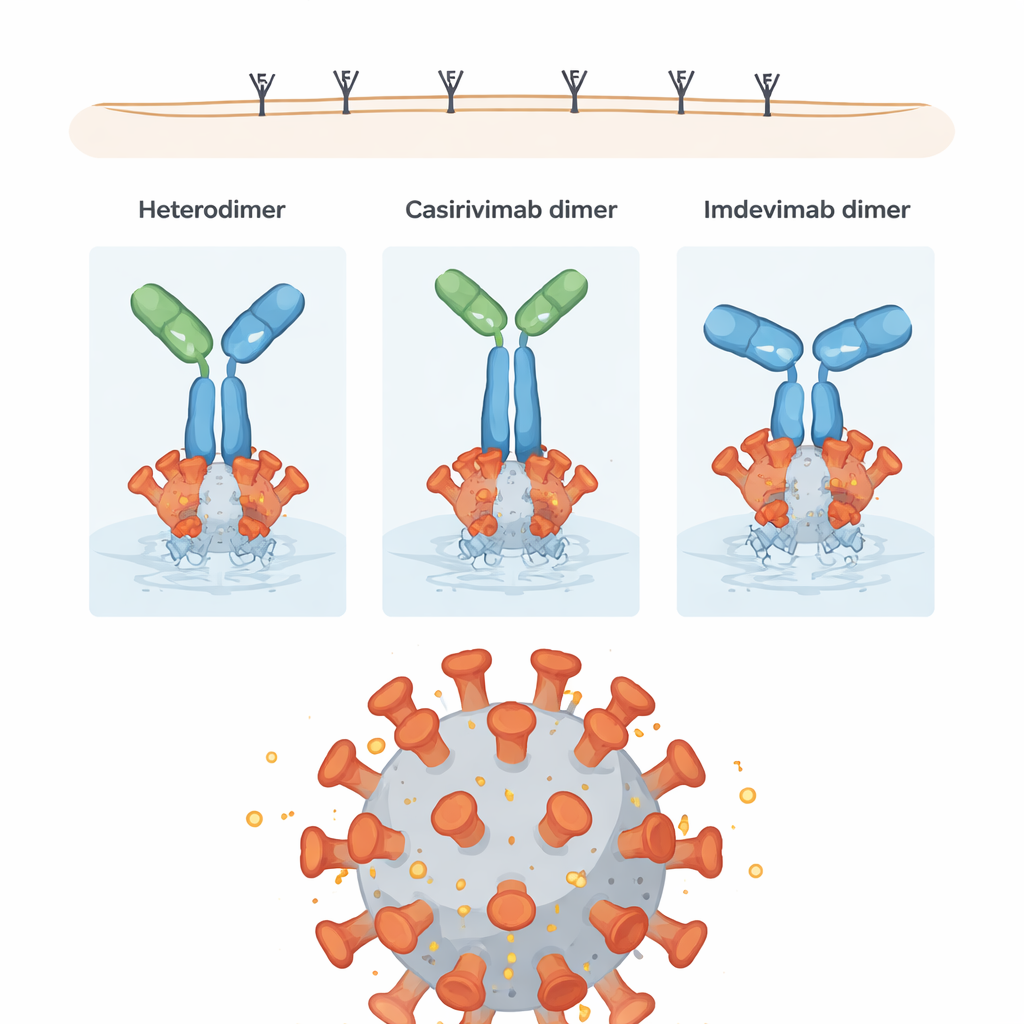
En kompakt förorening med blandad prestanda
Heterodimeren, trots att den var rik på starka, kompakta kopplingar mellan sina två olika antikroppar, visade något nedsatt prestanda: ungefär 70 % av neutraliserings- och ADCC-aktiviteten hos den avsedda co-formulerade blandningen. Den omfattande korsbindningen mellan dess armar och stammar verkar begränsa hur fritt molekylen kan rotera och omorientera sig när den binder till spike-proteinet, vilket i sin tur kan begränsa både blockeringen av viruset och signaleringen till immunceller. Många av dess bindningar är dock av en typ som långsamt kan brytas under fysiologiska förhållanden, vilket gör heterodimeren relativt instabil över tid och benägen att falla tillbaka till individuella antikroppar.
Vad detta betyder för antikroppsmediciner
För patienter och läkemedelsutvecklare är huvudbudskapet lugnande men nyanserat. Denna djupdykning i REGEN-COV-dimerer tyder på att de flesta dimerformer, inklusive den ovanliga heterodimer-föroreningen, behåller betydande antiviral aktivitet, och det finns ingen tydlig signal om ökad säkerhetsrisk från högre ordningens aggregat i detta system. Samtidigt visar arbetet att finstilta detaljer — var antikroppar rör vid varandra, hur hårt de är korslänkade och hur kompakta eller förlängda de är — kan betydligt påverka potensen. Författarna menar att liknande strukturell och funktionell profilering av dimerer i andra antikroppsläkemedel kan bli ett kraftfullt prekliniskt sätt att förstå och hantera föroreningar, och kanske till och med inspirera nya, avsiktligt konstruerade multimeriska antikroppar som utnyttjar geometri för att bättre passa och neutralisera virus.
Citering: Nguyen, J.B., Liu, S., Yan, Y. et al. Insights into the structural differences between homo- and heterodimers enriched from a cocktail of monoclonal antibodies against SARS-CoV-2. Sci Rep 16, 7024 (2026). https://doi.org/10.1038/s41598-026-37545-4
Nyckelord: antikroppsdimerer, REGEN-COV, SARS-CoV-2-spike, cocktails av monoklonala antikroppar, proteinaggregat