Clear Sky Science · sv
TIPE2 fungerar som en gynnsam prognostisk biomarkör och hämmar kolangiokarcinomets progression genom att rikta in sig på RAC1‑medierad transport av integrin αvβ6
Varför denna sällsynta gallgångscancer är viktig
Kolangiokarcinom, en cancer i gallgångarna i och kring levern, är ovanlig men förödande. De flesta patienter diagnostiseras sent, kirurgi är sällan möjlig och färre än en av tjugo överlever fem år. Läkare behöver snabbt bättre verktyg för att förutsäga vilka patienter som kommer att få sämre utfall och nya angreppssätt för behandling. Denna studie identifierar en molekyl kallad TIPE2 som både hjälper till att prognostisera och verkar sakta cancerns tillväxt och spridning.
En inbyggd broms som försvinner
TIPE2 är ett protein mest känt för att dämpa immunsystemet och förhindra okontrollerad inflammation. Författarna undrade om det också kan fungera som en naturlig broms i gallgångsceller som blir cancerösa. De undersökte tumörprover från en stor grupp om 218 patienter som opererats för kolangiokarcinom och från en andra, oberoende grupp om 95 patienter. Med immunohistokemi, en färgningsmetod som visar hur mycket av ett visst protein som finns i vävnad, mätte de TIPE2‑nivåer i tumörer och i närliggande icke‑cancerös gallgångsvävnad.
Mindre TIPE2, mer aggressiva tumörer
I båda patientgrupperna var TIPE2 konsekvent lägre i cancervävnaden än i normala gallgångar. Dessutom tenderade tumörer med mindre TIPE2 att vara mer avancerade och aggressiva. Låg TIPE2 kopplades till större tumörer, spridning till närliggande lymfkörtlar, invasion av blodkärl och högre övergripande cancerstadium. När teamet följde patienterna över tid dog de med låg TIPE2 snabbare än de vars tumörer fortfarande uttryckte högre mängder. Statistiska analyser visade att TIPE2 var en oberoende prediktor för överlevnad, även efter att man tagit hänsyn till konventionella mått som tumörstorlek och lymfkörtelstatus.
Att göra en biomarkör kliniskt användbar
För att göra resultaten användbara i kliniken byggde forskarna en ‘‘nomogram’’—ett visuellt poängverktyg som kombinerar flera riskfaktorer till en enskild prognos. I detta diagram översätts varje patients tumörstorlek, lymfkörtelengagemang, blodkärlsinvasion och TIPE2‑nivå till poäng som uppskattar chansen att vara vid liv ett, tre eller fem år efter operation. Modellen presterade bättre än det konventionella TNM‑stadieindelningen ensam, vilket tyder på att tillägg av TIPE2‑färgning i rutinpatologi kan förbättra läkares förmåga att ge råd och välja uppföljande behandlingar.
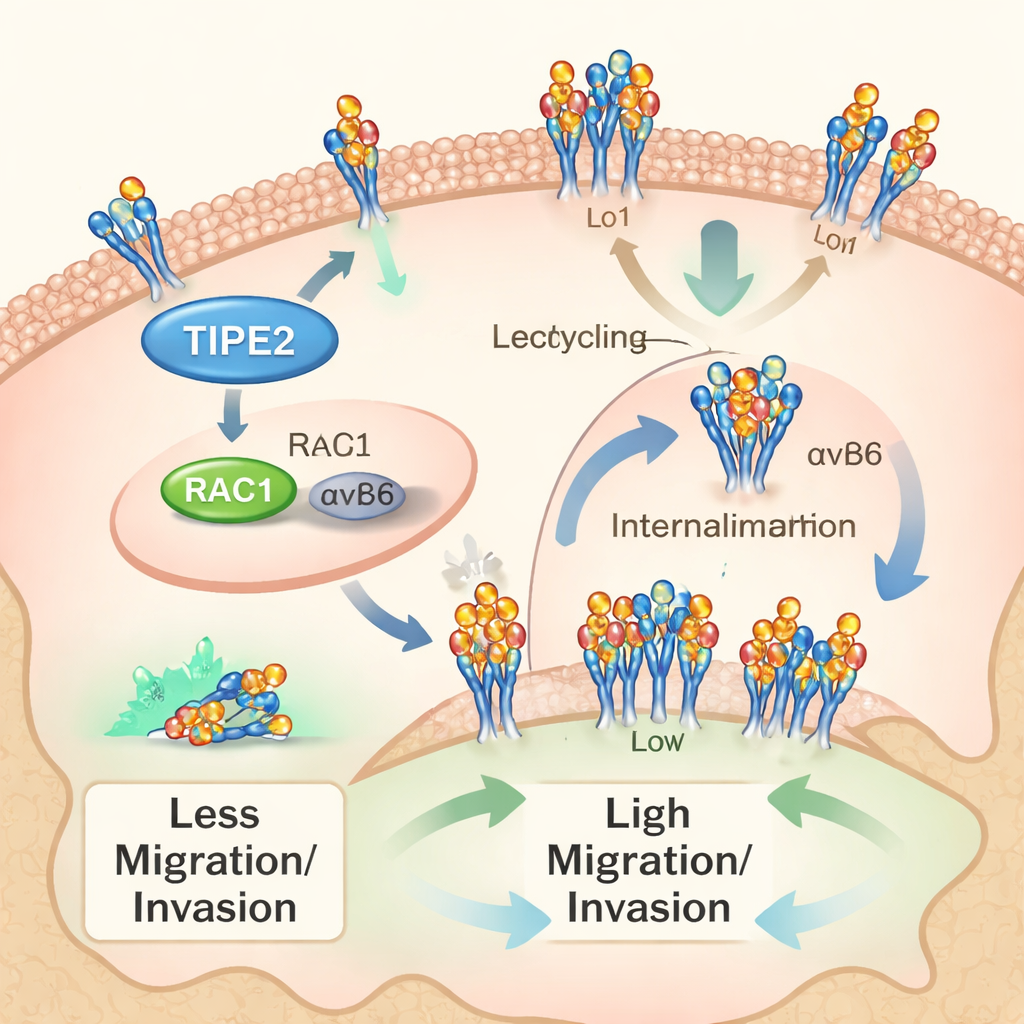
Hur TIPE2 hejdar cancerceller
Utöver prognos utforskade teamet hur TIPE2 påverkar cancercellernas beteende. I laboratorieförsök med humana kolangiokarcinomcellinjer gjorde artificiellt sänkta TIPE2‑nivåer att cellerna växte snabbare och rörde sig och invaderade lättare genom artificiella membran. Att öka TIPE2 gav motsatt effekt, saktade ner celldelning och dämpade deras förmåga att migrera och tränga igenom barriärer. I möss som implanterats med gallgångscellinjer minskade direkt leverans av extra TIPE2 tumörernas storlek och vikt, vilket visar att TIPE2 kan hämma tumörtillväxt både i levande djur och i odlingsskålar.
Ett trafikproblem på cellsurface
Studien fokuserade på en annan aktör kallad integrin αvβ6, ett ytmolekylärt adhesionsprotein som hjälper cancerceller att fästa vid och omforma sin omgivning, vilket underlättar invasion och spridning. Forskarna hade tidigare visat att αvβ6 är rikligt förekommande och skadligt i kolangiokarcinom. Här undersökte de ‘‘trafikeringen’’ av αvβ6—dess ständiga internalisering i cellen och återcirkulation tillbaka till ytan. Med biokemiska spårningsassays fann de att denna transportprocess är aktiv i gallgångsceller och att blockering av internalisering dämpar celltillväxt och invasivitet. TIPE2 visade sig störa både internalisering och återcirkulation av αvβ6, vilket minskar antalet och rörligheten hos dessa molekyler på cellsurface.
En nyckelmolekyl: RAC1
Sambandet mellan delarna är RAC1, en liten molekylär brytare som kontrollerar cellrörelse och förflyttning av membranproteiner. Författarna visade att hämning av RAC1 saktar ner αvβ6‑trafikeringen, på samma sätt som TIPE2 gör. Tidigare arbete hade visat att TIPE2 kan binda RAC1 och hålla det i schack. Beräkningsmodellering i denna studie föreslog fysiska kontakter mellan TIPE2, RAC1 och svansen på αvβ6‑integrinet. När teamet använde en muterad form av TIPE2 som inte kan interagera korrekt med RAC1 försvann dess förmåga att bromsa cancercellernas tillväxt och invasion i hög grad. På samma sätt gav tillsats av extra TIPE2 avsevärt mindre effekt om cellerna förbehandlats med ett RAC1‑blockerande läkemedel. Tillsammans stöder dessa fynd en väg där TIPE2 lugnar RAC1, vilket i sin tur minskar αvβ6‑trafikering och det aggressiva beteendet hos kolangiokarcinomceller.
Vad detta betyder för patienter
För icke‑specialister är budskapet tvådelat. För det första kan TIPE2‑färgning i tumörprover ge läkare en tydligare bild av hur farlig en given gallgångscancer är och förbättra riskprognosen utöver nuvarande stadieindelningar. För det andra pekar TIPE2 självt och den RAC1–αvβ6‑väg den reglerar mot nya behandlingsidéer: att öka TIPE2‑aktivitet eller att rikta in sig direkt på RAC1 eller αvβ6 kan hjälpa till att bromsa denna annars dödliga cancer. Även om sådana terapier kräver mer forskning och kliniska prövningar, kartlägger detta arbete en lovande väg mot mer precis och effektiv vård för patienter med kolangiokarcinom.
Citering: Wang, S., Jia, W., Sun, Y. et al. TIPE2 serves as a favorable prognostic biomarker and suppresses cholangiocarcinoma progression by targeting RAC1-mediated integrin αvβ6 trafficking. Sci Rep 16, 6638 (2026). https://doi.org/10.1038/s41598-026-37540-9
Nyckelord: kolangiokarcinom, TIPE2, biomarkör, integrin αvβ6, RAC1