Clear Sky Science · sv
Interaktion mellan pulserat lågfrevent elektromagnetiskt fält (PEMF) och mitokondrier
Mjuka fält och cellens kraftverk
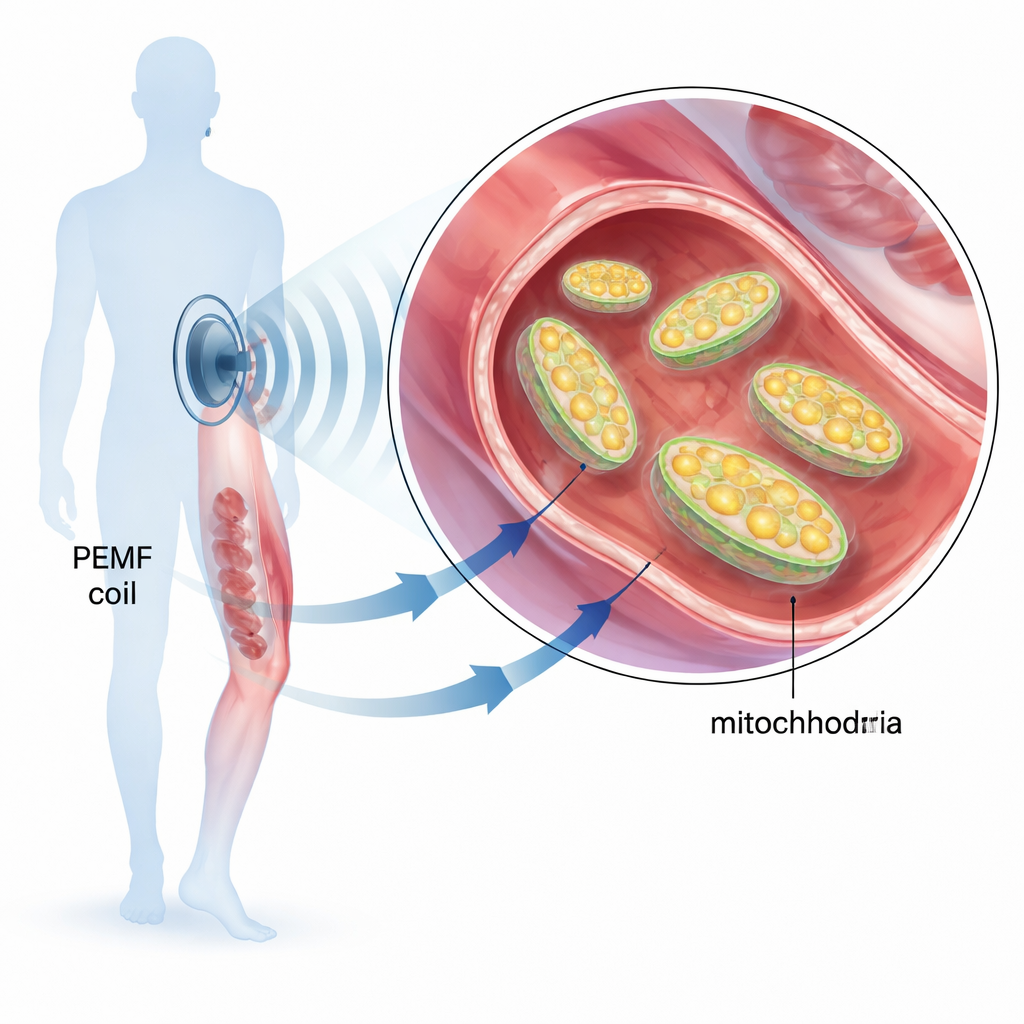
Pulsad elektromagnetisk fältterapi (PEMF) används redan i kliniker för att hjälpa brutna ben att läka, lindra ledsmärta och påskynda återhämtning efter operation. Vi förstår dock fortfarande inte helt hur dessa milda, låg‑frekventa fält verkar inne i kroppen. Denna studie ställer en enkel men viktig fråga: påverkar PEMF‑signaler mitokondrierna direkt — de små kraftverken i våra celler som genererar större delen av vår energi — och i så fall hur?
Varför mitokondrier är viktiga för vardaglig hälsa
Mitokondrier omvandlar mat och syre till molekylen ATP, cellernas universella "energivaluta". När mitokondrier sviktar läker vävnader långsammare, muskler blir tröttare och sjukdomar kopplade till nedsatt ämnesomsättning kan förvärras. Eftersom tidigare forskning antytt att PEMF‑behandlingar förbättrar energimetabolismen och stödjer vävnadsreparation, fokuserade författarna på om en specifik PEMF‑anordning kunde finjustera mitokondriell aktivitet. De använde en väldefinierad magnetisk signal: korta, millisekund‑långa pulser av en 30 kHz sinusvåg med låg ingångsenergi, applicerad på muskelceller i odling, på råttvävnader och på renade mitokondrier.
Närmare in i levande celler
I humana muskelceller odlade i labbet mätte teamet tre nyckelindikatorer efter PEMF‑exponering: den elektriska potentialen över mitokondriens inre membran (en sorts liten batteripotential), nivåer av reaktiva syreföreningar (höga nivåer kan vara skadliga) och kväveoxid, en gas som tillfälligt kan blockera mitokondriell andning. Cirka 90 minuter efter behandling var mitokondriernas membranpotential måttligt lägre, medan kväveoxidnivåerna hade minskat; reaktiva syreföreningar ökade inte. Ett litet fall i membranpotential kan signalera antingen skada eller ökad ATP‑produktion. Eftersom cellerna inte visade stressmarkörer misstänkte författarna att mitokondrierna helt enkelt jobbade lite snabbare och förbrukade den lagrade spänningen över sitt inre membran.
Test av hur mitokondrier "andas"
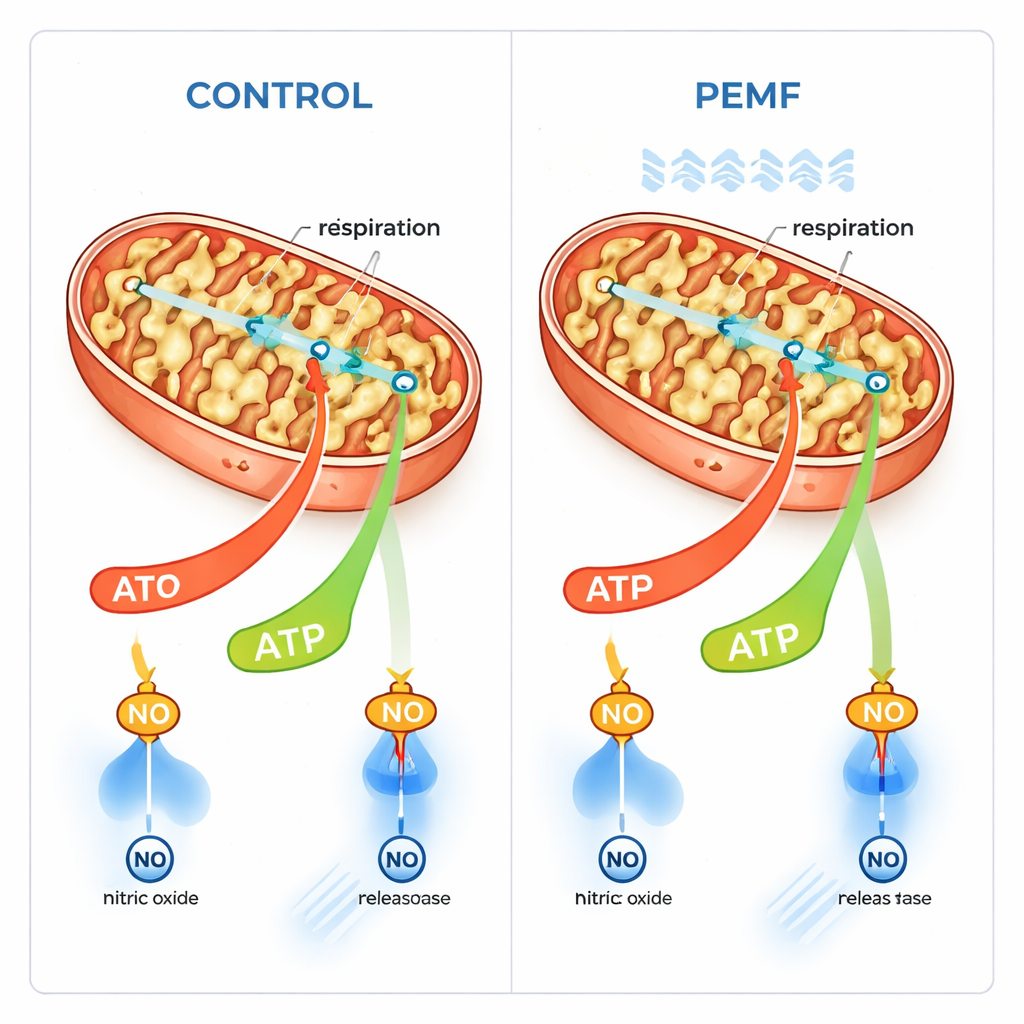
För att testa denna idé mer direkt perforerade forskarna försiktigt det yttre cellmembranet så att de kunde exakt tillföra olika bränslen till mitokondrierna och mäta syreförbrukning. De såg konsekvent en tendens till högre respiration kopplad till ATP‑produktion efter PEMF, särskilt när glutamat, ett vanligt mitokondriellt bränsle, var närvarande. Statistisk analys över många prover antydde att kombinationen av PEMF‑exponering och bränsleval signifikant påverkade hur snabbt mitokondrier förbrukade syre. Viktigt är att det inte fanns några tecken på att PEMF skadade cellerna eller deras mitokondrier. Istället verkade fälten selektivt stimulera den "kopplade" respirationsläget, där syreförbrukning är tätt knuten till ATP‑produktion, utan att öka den slösaktiga, okopplade förbränningen av bränsle.
Inflammation, kväveoxid och en överraskning från blått ljus
Eftersom kväveoxid kan ansamlas under inflammation och blockera ett nyckelsteg i mitokondriell andning, undersökte teamet om PEMF kunde hjälpa mitokondrier att återhämta sig från sådan hämning. De tillsatte en kemisk kväveoxiddonor till muskel‑ och levervävnadshomogenat samt till isolerade levermitokondrier, vilket kraftigt saktade ner respirationen. Under dessa förhållanden återställde inte PEMF mitokondriernas funktion, även när mitokondrierna var högt koncentrerade. För att se om blockeringen överhuvudtaget var reversibel belyste de de kväveoxid‑hämmade mitokondrierna med blått ljus, med en metod som är känd för att lossa kväveoxid från dess bindningsställe. Blått ljus återställde respirationen delvis, vilket bekräftade att systemet kunde återhämta sig, men PEMF tillförde ingen ytterligare nytta. Detta visade att PEMF:s positiva effekter inte beror på att avlägsna kväveoxid under inflammationsliknande förhållanden.
Membranportar och energiflöde
Med en analogi mellan celler och elektriska kretsar föreslår författarna att PEMF främst kan verka på biologiska membran. Mitokondrier är omslutna av ett yttre membran som innehåller ett nyckelprotein, VDAC, som tillåter energirelaterade molekyler att passera in och ut. Till skillnad från det inre membranets mycket höga spänning har det yttre membranet en mindre, lättare påverkbar potential. Författarna föreslår att PEMF subtilt ändrar denna yttre membranpotential, vilket skiftar hur ofta VDAC‑portarna är öppna och därigenom underlättar flödet av bränsle och förbrukat ATP över membranet. Detta skulle naturligtvis öka den kopplade, ATP‑producerande respirationen utan att ändra den maximala kapaciteten hos elektrontransportkedjan i sig.
Vad detta betyder för framtida behandlingar
Sammanfattningsvis finner studien inga bevis för att denna typ av PEMF är skadlig för mitokondrier. Tvärtom förbättrar PEMF försiktigt den del av mitokondriell respiration som producerar ATP, samtidigt som maximal respiratorisk kapacitet och oxidativ stress förblir oförändrade. Däremot räddar den inte mitokondrier som är blockerade av hög kväveoxid, vilket tyder på att dess fördelar i inflammerade vävnader måste uppstå via andra mekanismer. För patienter och kliniker stöder dessa resultat idén att noggrant inställda elektromagnetiska fält kan putta cellens kraftverk mot ett mer effektivt, energi‑producerande tillstånd — vilket ger en plausibel, mekanistisk förklaring till några av de läkningseffekter som rapporterats vid benläkning, sårvård och postoperativ återhämtning.
Citering: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
Nyckelord: pulsat elektromagnetiskt fältterapi, mitokondrier, cellulär energi, kväveoxid, ATP‑produktion