Clear Sky Science · sv
Validering av en ny genomisk biomarkör för mesenkymala stamcells skalbarhet och konsekvenser av genotypstatus för cellulära senescensfenotyper
Varför det blir svårare att odla stamceller med tiden
Stamceller från vuxen benmärg är en grundpelare i många experimentella terapier, från att reparera skadade ben till att dämpa inflammation. Men det finns en hake: för att behandla en patient måste laboratorierna odla dessa celler utanför kroppen, och ju längre de expanderas desto mer saktar de ner och beter sig som "åldrade" celler. I denna studie undersöks varför vissa människors stamceller åldras långsammare i skålen, och om en liten saknad bit DNA kan hjälpa forskare att välja de mest robusta cellerna för framtida behandlingar.
En saknad gen som ändrar spelreglerna
Forskarna fokuserade på en gen som kallas GSTT1, vilken hjälper celler att avgifta skadliga molekyler som bildas under normal metabolism och stress. Överraskande nog saknar en betydande andel människor helt denna gen – de är "GSTT1-null." Tidigare arbete antydde att benmärgsstamceller från dessa individer kan växa snabbare och behålla sina skyddande kromosomändar, så kallade telomerer, längre. I det här projektet undersökte teamet stamceller från sex friska donatorer, delade in dem i GSTT1-positiva och GSTT1-null, och följde sedan hur cellerna betedde sig under många expansionsvarv och efter exponering för röntgenstrålning, en stark utlösare av cellulär åldrande.
Snabbväxande celler som motstår ålderssignaler
När forskarna följde cellantalet över flera dagar multiplicerade GSTT1-null-stamceller snabbare vid tidiga passager än celler som bar genen. Vid mycket lång expansion blev tillväxthastigheterna mellan grupperna mer lika, men fördelen i början var tydlig. För att undersöka åldrande direkt använde teamet en klassisk färgning som gör senescenta, eller "åldrade", celler blå. Efter många delningscykler, och igen efter bestrålning, innehöll GSTT1-null-kulturer konsekvent färre blå, senescenta celler än GSTT1-positiva kulturer. Viktigt är att denna skillnad inte berodde på långsammare förkortning av telomerer eller på högre aktivitet hos enzymet som upprätthåller telomererna (hTERT); båda måtten såg liknande ut oberoende av GSTT1-status, vilket tyder på att en annan mekanism var i spel.
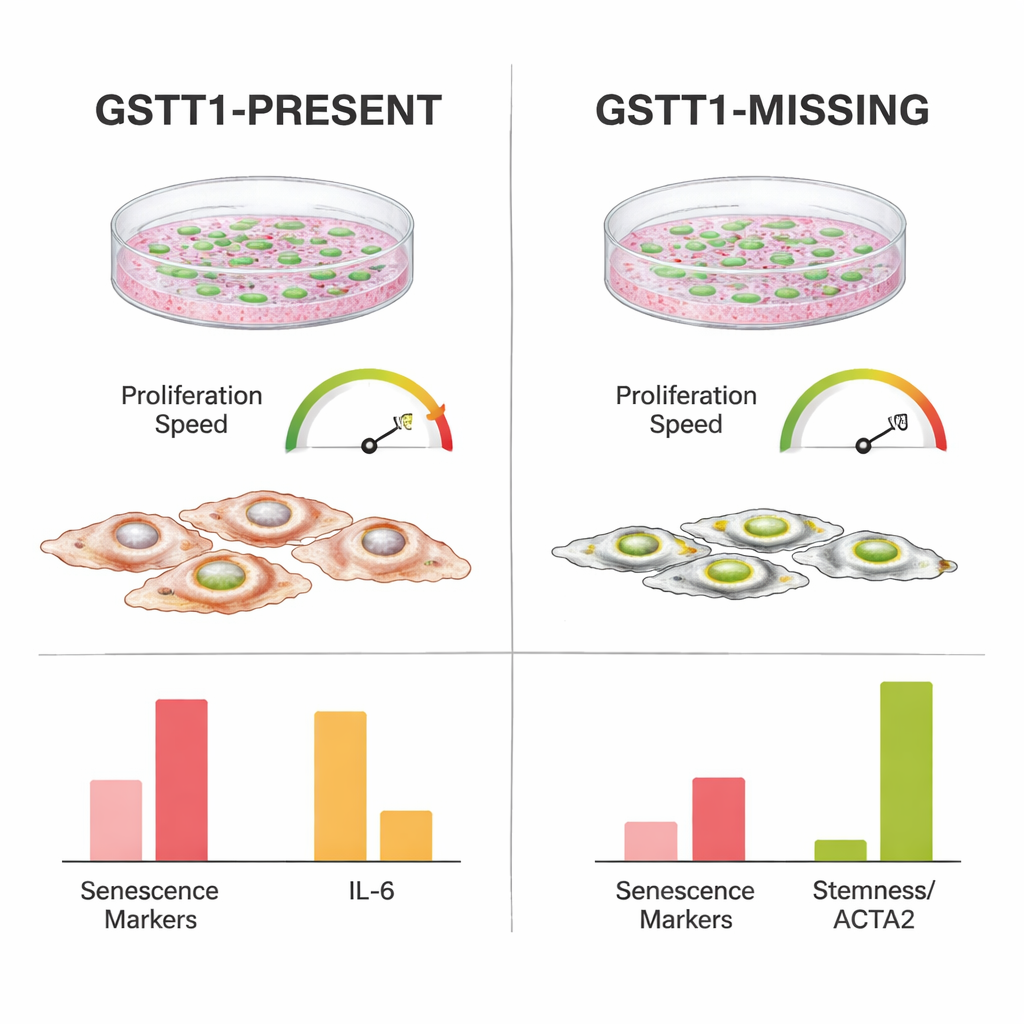
Lugnare stress och inflammation i odlingen
För att förstå vad som gjorde GSTT1-null-celler mer motståndskraftiga mätte forskarna aktivitet i gener kopplade till cellcykelstopp, DNA-skada och den så kallade senescensassocierade sekretoriska fenotypen — en blandning av inflammatoriska och stressrelaterade signaler som åldrande celler släpper ut. Celler med GSTT1 närvarande visade högre nivåer av nyckelns "stopp"-signaler som p21 och p14, särskilt vid senare passager och efter bestrålning. De ökade också IL-6, en potent inflammatorisk molekyl, och andra stressrelaterade gener mer än GSTT1-null-cellerna. I kontrast upprätthöll GSTT1-null-stamceller lägre nivåer av dessa ålders- och inflammationsmarkörer, samtidigt som de behöll högre nivåer av ACTA2 och TWIST1, gener kopplade till strukturell integritet och stamcellsliknande beteende. Noterbart är att båda genotyperna bibehöll liknande förmåga att differentiera till benceller och fettceller, vilket innebär att den skyddande effekten inte helt enkelt berodde på förlust av normal stamcellsfunktion.
Vad detta kan innebära för framtida cellterapier
Tillsammans tyder fynden på att benmärgsstamceller som saknar GSTT1 delvis är skyddade från det vanliga slitage som följer av laboratorieexpansion och bestrålning. De växer snabbare i början, samlar på sig färre uppenbart åldrade celler och behåller en mindre inflammatorisk profil, även om deras kromosomer förkortas i liknande takt. För företag och kliniker som tillverkar stora mängder stamceller skulle GSTT1-null-status kunna fungera som en praktisk genetisk markör för att identifiera donatorer vars celler tolererar expansion bättre, vilket potentiellt ger mer konsekventa och potenta terapier. Självklart användes ett litet donatorunderlag och icke-kliniska odlingsförhållanden i studien, så större, noggrant kontrollerade studier behövs. Ändå belyser arbetet hur en enda ärftlig skillnad kan rubba balansen mellan ungdomligt och åldrande beteende hos stamceller som odlas för regenerativ medicin.
Citering: Ardana, I.K.K.G., Maldonado, V.V., Barnes, C.L. et al. Validation of a novel genomic biomarker of mesenchymal stem cell scalability and implications of genotype status on cellular senescence phenotypes. Sci Rep 16, 6219 (2026). https://doi.org/10.1038/s41598-026-37517-8
Nyckelord: mesenkymala stamceller, cellulär senescens, biomarkörer, cellsjukdomsproduktion, GSTT1-polymorfi